(2023) Đề thi thử Hóa THPT Chuyên Võ Nguyên Giáp, Quảng Bình ( Lần 1) có đáp án
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
Glyxin (H2N-CH2-COOH) tác dụng với chất nào dưới đây thu được muối có môi trường axit?
Cho 0,015 mol anilin tác dụng vừa đủ với dung dịch brom. Khối lượng kết tủa thu được là
Tơ nào dưới đây thuộc loại tơ thiên nhiên?
Phát biểu không đúng là
Kim loại không phản ứng được với H2SO4 đặc, nguội là
Kim loại điều chế bằng phương pháp điện phân nóng chảy là
Kim loại có tính khử mạnh hơn kim loại Mg là
Cho 0,78 gam hỗn hợp gồm Mg và Al tan hoàn toàn trong dung dịch H2SO4 loãng thu được 0,896 lít khí H2 và dung dịch chứa m gam muối. Giá trị của m là
Trong cùng một điều kiện, Cr là kim loại có tính khử mạnh hơn
Kim loại nào sau đây là kim loại kiềm?
Chất nào sau đây là chất điện li yếu?
Hợp chất mà trong phân tử có chứa 3 nguyên tử cacbon là
Phản ứng của ancol và axit cacboxylic (xúc tác H2SO4 đặc) tạo thành este có tên gọi là
Công thức phân tử của axit linoleic là
Este X có công thức phân tử C4H6O2. Thủy phân X trong môi trường axit thu được sản phẩm gồm ancol metylic và axit hữu cơ Y. Công thức của Y là
Cho 11,1 gam este đơn chức no E tác dụng hết với 150 ml dung dịch KOH 1M thu được 12,6 gam muối. Công thức cấu tạo của E là
Chất không bị thủy phân trong môi trường axit là
Lên men dung dịch chứa 225 gam glucozơ, thu được 92 gam ancol etylic. Hiệu suất quá trình lên men là
Chất X có vị ngọt, dung dịch X tác dụng được với Cu(OH)2 ở nhiệt độ thường và không tham gia phản ứng tráng bạc. X là
Tên gốc chức của C2H5-NH-C2H5 là
Chất nào dưới đây tác dụng với kim loại Na sinh ra khí H2?
Kim loại Ca tác dụng với H2O thu được dung dịch có chứa chất tan là
Hợp chất của canxi được dùng để đúc tượng, bó bột khi gãy xương là
C. Thạch cao nung (CaSO4.H2O).
Chất nào sau đây tác dụng với dung dịch NaOH sinh ra khí H2?
Hợp chất có tính lưỡng tính là
Kim loại Fe bị thụ động bởi dung dịch
Đem khử hoàn toàn m gam hỗn hợp X gồm FeO và CuO cần lượng vừa đủ V lít khí CO. Mặt khác để hòa tan hết m gam hỗn hợp X cần 150 ml dung dịch H2SO4 2M. Giá trị của V là
Trường hợp nào sau đây không xảy ra phản ứng hóa học?
Trong khí thải công nghiệp thường chứa các khí: SO2, NO2, HF. Có thể dùng chất nào (rẻ tiền) sau đây để loại các khí đó?
Tiến hành các thí nghiệm sau:
(a) Cho Mg dư vào dung dịch FeCl3.
(b) Cho Ba vào dung dịch CuSO4.
(c) Cho Zn vào dung dịch CuSO4.
(d) Nung nóng hỗn hợp Al và Fe2O3 (không có không khí) đến khi phản ứng xảy ra hoàn toàn.
(e) Nhỏ từ từ cho đến dư dung dịch NaOH vào dung dịch FeCl3.
Số thí nghiệm thu được kim loại là
A. 5
B. 4
C. 2
D. 3
Một loại etxăng có chứa 4 ankan với thành phần số mol như sau: heptan (10%), octan (50%), nonan (30%) và đecan (10%). Khi dùng loại etxăng này để chạy động cơ ôtô và môtô cần trộn lẫn hơi etxăng và không khí theo tỉ lệ thể tích như thế nào để phản ứng cháy xảy ra vừa hết?
Hỗn hợp X gồm triglixerit Y, axit oleic, axit panmitic và có tỉ lệ mol tương ứng là 1 : 2 : 3. Đốt cháy hoàn toàn m gam X thu được CO2 và 35,91 gam H2O. Mặt khác, m gam X tác dụng vừa đủ với 240 ml dung dịch NaOH 0,5M, đun nóng thu được glixerol và hỗn hợp chỉ chứa hai muối. Khối lượng của Y trong m gam hỗn hợp X là
Ở điều kiện thường, thực hiện thí nghiệm với khí NH3 như sau: Nạp đầy khí NH3 vào bình thủy tinh rồi đậy bình bằng nắp cao su. Dùng ống thủy tinh vuốt nhọn đầu nhúng vào nước, xuyên ống thủy tinh qua nắp cao su rồi lắp bình thủy tinh lên giá như hình vẽ.
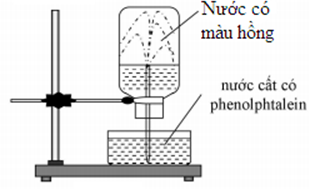
Cho các phát biểu sau liên quan đến thí nghiệm trên:
(a) Thí nghiệm trên để chứng minh tính tan tốt của khí NH3 trong nước.
(b) Tia nước phun mạnh vào bình thủy tinh do áp suất trong bình cao hơn áp suất không khí.
(c) Trong thí nghiệm trên, nếu thay dung dịch phenolphtalein bằng dung dịch quỳ tím thì nước trong bình sẽ không có màu.
(d) So với điều kiện thường, khí X tan trong nước tốt hơn ở 60°C.
(e) Nếu thay thế NH3 bằng HCl thì các hiện tượng xảy ra tương tự.
Số phát biểu sai là
A. 1
B. 2
C. 3
D. 4
Đốt cháy hoàn toàn 0,33 mol hỗn hợp X gồm metyl propionat, metyl axetat và hai hiđrocacbon mạch hở cần vừa đủ 1,27 mol O2, tạo ra 14,4 gam H2O. Nếu cho 0,33 mol X tác dụng với dung dịch Br2 dư thì số mol Br2 phản ứng tối đa là
Cho các phát biểu sau:
(1) Chất béo là trieste của etylen glycol với axit béo.
(2) Các dung dịch protein đều có phản ứng màu biure.
(3) Chỉ có một este đơn chức tham gia phản ứng tráng bạc.
(4) Để điều chế nilon-6 có thể thực hiện phản ứng trùng hợp hoặc trùng ngưng.
(5) Có thể phân biệt glucozơ và fructozơ bằng vị giác.
(6) Thủy phân bất kì chất béo nào cũng thu được glixerol.
(7) Triolein tác dụng được với H2 (xúc tác Ni, t°), dung dịch Br2, Cu(OH)2.
(8) Phần trăm khối lượng nguyên tố hiđro trong tripanmitin là 12,16%.
Số phát biểu đúng là
A. 3
B. 5
C. 4
D. 6
Điện phân (với điện cực trơ, màng ngăn) dung dịch chứa x mol CuSO4 và y mol NaCl (x > y) bằng dòng điện một chiều có cường độ 2,68A, sau thời gian t giờ, khối lượng dung dịch Y có khối lượng giảm 20,45 gam so với dung dịch ban đầu. Thêm tiếp Al dư vào Y, thấy thoát ra 3,36 lít khí H2 và dung dịch sau phản ứng chứa 2 chất tan có số mol bằng nhau. Giả thiết hiệu suất điện phân là 100%, các khí sinh ra không tan trong nước và nước không bay hơi trong quá trình điện phân. Giá trị của t gần nhất với giá trị nào sau đây?
Cho sơ đồ các phản ứng sau:
(1) A + X + H2O → Ca(AlO2)2 + H2
(3) Ca(AlO2)2 + CO2 + H2O → G + E
(2) A + H2SO4 → Z + H2
(4) Z + Y → G + Na2SO4
(5) E + Y → CaCO3 + NaHCO3 + H2O
Nhận định về các chất ứng với các chữ cái A, X, Z, G, E như sau:
(a) A là chất có tính lưỡng tính.
(b) X là một bazơ mạnh dùng để sản xuất clorua vôi (CaOCl2), vật liệu xây dựng,
(c) Z là hợp chất có thành phần chính trong phèn chua.
(d) G là hợp chất kết tủa ở dạng keo và có tính lưỡng tính.
(e) E là hợp chất bền không bị phân hủy khi đun nóng và nguyên nhân làm cho nước có tính cứng tạm thời.
Số nhận định đúng là
A. 3
B. 4
C. 5
D. 2
Cho các phát biểu sau:
(a) Hỗn hợp Cu, Fe3O4 có số mol bằng nhau tan hết trong lượng dung dịch HCl dư.
(b) Cho bột Cu vào lượng dư dung dịch FeCl3, thu được dung dịch chứa hai muối.
(c) Dung dịch amoniac làm phenolphtalein từ không màu chuyển sang màu hồng.
(d) Cho Mg tác dụng với lượng dư dung dịch FeCl3 thu được kim loại Fe.
(e) Kim loại vàng có tính dẻo kém hơn kim loại Al.
(g) Đun nóng có thể làm mềm nước có tính cứng tạm thời.
(f) Cho dung dịch KHSO4 dư vào dung dịch Ba(HCO3)2 thu được 2 kết tủa và 1 khí thoát ra.
Số phát biểu đúng là
A. 6
B. 5
C. 3
D. 4
Hòa tan hoàn toàn hỗn hợp X gồm 0,35 mol Mg, 0,1 mol Fe, MgCO3 và Mg(NO3)2 trong hỗn hợp dung dịch chứa 0,05 mol HNO3 và 1,49 mol NaHSO4. Sau khi phản ứng kết thúc, thu được dung dịch Y chỉ chứa 198,21 gam các muối trung hòa và 0,3 mol hỗn hợp khí Z gồm 4 khí không màu không hóa nâu trong không khí và có tỉ khối so với hidro là 539/30. Cho dung dịch NaOH cho đến dư vào dung dịch Y, sau đó lấy lượng kết tủa đun nóng trong không khí đến khối lượng không đổi thu được 32 gam chất rắn. Các phản ứng xảy ra hoàn toàn. Phần trăm về khối lượng của MgCO3 trong hỗn hợp X là
Hai chất E và F là đồng phẩn cấu tạo của nhau. Đốt cháy hoàn toàn E (no, mạch hở, ME < 180), thu được số mol CO2 bằng với số mol O2 đã tham gia phản ứng. Từ E, F thực hiện sơ đồ phản ứng sau:
E + NaOH → X + Y (1)
F + NaOH → X + Z + T (2)
Biết: E, F chỉ chứa chức este trong phân tử. Y, T đều là ancol trong đó chỉ có Y hòa tan được Cu(OH)2 và trong Z số nguyên tử cacbon bằng số nguyên tử oxi.
Cho các phát biểu sau:
(a) T tan ít trong nước nhưng tan nhiều trong dung môi hữu cơ.
(b) 1 mol X tác dụng với dung dịch AgNO3 trong NH3 dư, thu được tối đa 2 mol Ag.
(c) E là este no, hai chức, mạch hở.
(d) Có 3 đồng phân cấu tạo thỏa mãn chất Z.
(e) Sục khí propilen vào dung dịch KMnO4, thu được chất hữu cơ Y.
Số phát biểu đúng là
A. 3
B. 5
C. 4
D. 2