(2023) Đề thi thử Hóa THPT theo đề minh họa của Bộ Giáo dục có đáp án (Đề 24)
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
Chất nào sau đây là chất điện li yếu?
Dung dịch chất nào sau đây không làm đổi màu quỳ tím?
A. Axit fomic. B. Axit glutamic. C. Alanin. D. Lysin.
Kim loại nào sau đây thuộc nhóm IA trong bảng tuần hoàn?
Khi làm thí nghiệm với HNO3 đặc thường sinh ra khí NO2 có màu nâu đỏ, độc và gây ô nhiễm môi trường. Tên gọi của NO2 là
Polime X có công thức cấu tạo như sau:
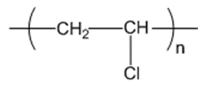
Tên gọi của X là
Kim loại Fe tác dụng với đơn chất nào sau đây sinh ra oxit?
Axit panmitic là một axit béo có trong mỡ động vật và dầu cọ. Công thức của axit panmitic là
Kim loại nào sau đây điều chế được bằng phương pháp thủy luyện?
Số oxi hóa của sắt trong hợp chất Fe2(SO4)3 là
Chất nào sau đây tác dụng với kim loại Na sinh ra khí H2?
Kim loại nào sau đây dẻo nhất trong tất cả các kim loại là
Kim loại Fe tan hết trong lượng dư dung dịch nào sau đây?
Nhôm bền trong không khí và nước do trên bề mặt của nhôm được phủ kín lớp chất X rất mỏng, bền. Chất X là
Số nguyên tử hiđro trong phân tử metyl fomat là
A. 6
B. 8
C. 4
D. 2
Phân tử chất nào sau đây chứa nguyên tử nitơ?
Glucozơ là chất dinh dưỡng và được dùng làm thuốc tăng lực cho người già, trẻ em và người ốm. Số nguyên tử cacbon trong phân tử glucozơ là
A. 6
Kim loại nào sau đây tan hoàn toàn trong nước dư?
Tính cứng tạm thời của nước do các muối canxi hiđrocacbonat và magie hiđrocacbonat gây nên. Công thức của canxi hiđrocacbonat là
Trong dung dịch, ion nào sau đây oxi hóa được kim loại Fe?
Phèn chua được dùng trong ngành thuộc da, công nghiệp giấy, làm trong nước,.. Công thức phèn chua là
Este X có công thức phân tử C4H8O2. Thủy phân X trong dung dịch NaOH dư, thu được sản phẩm gồm natri propionat và ancol Y. Công thức của Y là
Phát biểu nào sau đây đúng?
Nhiệt phân hoàn toàn m gam NaHCO3, thu được Na2CO3, H2O và 3,36 lít CO2. Giá trị của m là
Thủy phân m gam tinh bột sau một thời gian thu được m gam glucozơ (giả sử chỉ xảy ra phản ứng thủy phân tinh bột thành glucozơ). Hiệu suất của phản ứng thủy phân là
Chất nào sau đây tác dụng với dung dịch HCl sinh ra muối FeCl3?
Cho các tơ sau: visco, xenlulozơ axetat, nilon-6, nilon-6,6. Số tơ nhân tạo là
A. 1
B. 2
C. 4
D. 3
Để khử hoàn toàn 16,0 gam Fe2O3 thành kim loại Fe ở nhiệt độ cao (không có oxi) cần tối thiểu m gam kim loại Al. Giá trị của m là
Đốt cháy hoàn toàn m gam glyxin trong O2 thu được N2, H2O và 6,72 lít CO2. Giá trị của m là
Thí nghiệm nào sau đây chỉ xảy ra ăn mòn hóa học?
Este X đơn chức, trong X nguyên tử oxi chiếm 26,229% khối lượng. Cho 0,1 mol X phản ứng với dung dịch NaOH vừa đủ, thu được 18,4 gam muối. Nhận xét nào sau đây về X là đúng?
Hỗn hợp E gồm hai triglixerit X và Y (tỉ lệ mol tương ứng là 2 : 3). Xà phòng hóa hoàn toàn E bằng dung dịch NaOH dư, thu được hỗn hợp muối gồm C15H31COONa, C17H31COONa và C17H33COONa. Khi cho m gam E tác dụng với H2 dư (xúc tác Ni, to) thì số mol H2 phản ứng tối đa là 0,07 mol. Mặt khác, đốt cháy hoàn toàn m gam E, thu được 2,65 mol CO2 và 2,48 mol H2O. Khối lượng của X trong m gam E là
Tiến hành đồng thời 3 thí nghiệm sau với cùng một khối lượng bột nhôm như nhau:
Thi nghiệm 1 : Cho bột nhôm vào dung dịch HCl dư, thu được V1 lít khí H2.
Thí nghiệm 2 : Cho bột nhôm vào dung dịch NaOH dư, thu được V2 lít H2.
Thí nghiệm 3 : Cho bột nhôm vào dung dịch HNO3 loãng dư, thu được khí V3 lít khí NO (sản phẩm khử duy nhất). Các thể tích V1,V2 và V3 đo ở cùng điều kiện.
Mối quan hệ giữa V1,V2 và V3 nào sau đây là đúng?
Thực hiện phản ứng giữa axit cacboxylic và ancol theo sơ đồ sau (theo đúng tỉ lệ mol):
(1) X + Y E (C3H6O3) + H2O
(2) X + Z F (C4H8O4) + H2O
Giả sử E, F chỉ là sản phẩm hữu cơ của phản ứng este hoá (ME < MF); các axit cacboxylic và ancol đều mạch hở, phân tử chỉ chứa một loại nhóm chức. Cho các phát biểu sau:
(a) Hai chất Y, Z thuộc cùng một dãy đồng đẳng.
(b) E là hợp chất chỉ chứa một loại nhóm chức duy nhất.
(c) Z và E có cùng số nguyên tử cacbon trong phân tử.
(d) Chất X tan vô hạn trong nước, là một thành phần chính của giấm ăn.
(e) Từ etilen có thể điều chế trực tiếp chất Y bằng một phản ứng.
Số phát biểu đúng là
A. 2
B. 4
C. 1
D. 3
Để điều chế hai kim loại người ta hòa tan hỗn hợp X gồm muối khan E và muối tinh thể ngậm nước F (đều tạo bởi cùng một loại gốc axit) với tỉ lệ mol là 4 : 5 vào nước được dung dịch Y. Điện phân Y với cường độ dòng điện không đổi là 4,5 ampe trong thời gian 9650 giây thu được dung dịch Z. Dung dịch Z có khối lượng giảm 26,19 gam so với dung dịch Y và hòa tan được tối đa 7,14 gam Al2O3. Biết trong X thì nguyên tố nitơ chiếm 10,37% về khối lượng. Phần trăm khối lượng của E trong X có giá trị gần nhất với giá trị nào sau đây?
Cho các phát biểu sau:
(a) Glyxin phản ứng được với dung dịch NaOH.
(b) Khử glucozơ bằng H2 (xúc tác Ni, to) thu được sobitol.
(c) Etanol phản ứng được với Cu(OH)2 tạo thành dung dịch màu xanh lam.
(d) Triolein có ba liên kết π trong phân tử.
(e) Polime thường là chất rắn, không bay hơi nhưng có nhiệt độ nóng chảy xác định.
Số phát biểu đúng là
A. 3
B. 4
C. 2
D. 5
Nung nóng a mol hỗn hợp X gồm C2H6 (0,05 mol), C2H2, C4H2 (mạch hở) và H2 với xúc tác Ni trong bình kín (chỉ xảy ra phản ứng cộng H2), sau một thời gian thu được hỗn hợp khí Y có tỉ khối so với X là 1,4. Biết Y phản ứng tối đa với 0,08 mol brom trong dung dịch. Mặt khác, đốt cháy hết a mol X trên thu được H2O và 9,68 gam CO2. Giá trị của a là
Cho các phát biểu sau:
(a) Từ Li đến Cs khả năng phản ứng với nước tăng dần.
(b) Cho dung dịch KOH vào dung dịch Ca(HCO3)2 thu được kết tủa.
(c) Thạch cao nung có công thức hóa học là CaSO4.2H2O.
(d) Các đồ vật bằng sắt khó bị ăn mòn hơn sau khi được quét sơn lên bề mặt.
(e) Độ dinh dưỡng của phân đạm được đánh giá theo tỉ lệ phần trăm về khối lượng của nguyên tố nitơ.
Số phát biểu đúng là
A. 5
B. 2
C. 4
D. 3
Hỗn hợp X gồm Cu(NO3)2, Fe(NO3)2, Fe(NO3)3, Mg(NO3)2. Nung nóng 13,6 gam hỗn hợp X thu được chất rắn Y, khí O2 và 0,16 mol khí NO2. Cho 13,6 gam X vào dung dịch NaOH dư, lọc kết tủa, nung trong không khí đến khối lượng không đổi thu được 5,2 gam chất rắn. Mặt khác, hòa tan 27,2 gam hỗn hợp X vào dung dịch H2SO4 loãng dư, thu được a mol khí NO. Biết NO là sản phẩm khử duy nhất của N+5, các phản ứng xảy ra hoàn toàn. Giá trị của a là
Tiến hành hai thí nghiệm (1), (2) riêng biệt: Hấp thụ hoàn toàn khí CO2 vào 2 cốc, mỗi cốc đều chứa 200 ml dung dịch gồm NaOH 0,2M và Ba(OH)2 0,2M. Kết quả thí nghiệm được mô tả qua bảng số liệu dưới đây:
|
Giá trị |
Thí nghiệm 1 |
Thí nghiệm 2 |
|
Thể tích khí CO2 (lít) |
V |
V + 0,672 |
|
Khối lượng chất tan (gam) trong dung dịch thu được |
2,74 |
8,54 |
Giá trị của V và tổng khối lượng kết tủa (gam) thu được sau hai thí nghiệm lần lượt là
Hỗn hợp E gồm ba este mạch hở đều tạo bởi axit cacboxylic với ancol: X (no, đơn chức), Y (không no, đơn chức, phân tử có hai liên kết pi) và Z (no, hai chức). Cho 0,2 mol E phản ứng vừa đủ với dung dịch NaOH, thu được 12,88 gam hỗn hợp ba ancol cùng dãy đồng đẳng và 24,28 gam hỗn hợp T gồm ba muối của ba axit cacboxylic. Đốt cháy toàn bộ T cần vừa đủ 0,175 mol O2, thu được Na2CO3, CO2 và 0,055 mol H2O. Phần trăm khối lượng của X trong E có giá trị gần nhất với giá trị nào sau đây?
A. 9
B. 12
C. 5
D. 6