(2023) Đề thi thử Hóa THPT theo đề minh họa của Bộ Giáo dục có đáp án (Đề 37)
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
Trong hợp chất, kim loại kiềm có số oxi hóa là
Al2O3 phản ứng được với cả hai dung dịch
Trong phân tử chất nào sau đây có 2 nhóm amino (NH2) và 1 nhóm cacboxyl (COOH)?
Trong các kim loại Na; Mg; Fe và Cu. Kim loại nào sau đây có tính khử mạnh nhất?
Trong tự nhiên, canxi sunfat tồn tại dưới dạng muối ngậm nước (CaSO4.2H2O) được gọi là
Kim loại Fe tác dụng với lượng dư dung dịch nào sau đây tạo hợp chất sắt (III) ?
Ở điều kiện thường, kim loại nào sau đây không phản ứng với nước?
Đun nóng este CH3COOC2H5 với một lượng vừa đủ dung dịch NaOH, sản phẩm thu được là
Trong công nghiệp, kim loại nào sau đây được điều chế bằng phương pháp điện phân nóng chảy?
Trùng hợp chất nào sau đây thu được poli (vinyl clorua)?
Trong các chất sau (ở dạng dung dịch) chất nào là chất điện li yếu?
Kim loại nhôm phản ứng với dung dịch nào sau đây?
Khí X tạo ra trong quá trình đốt cháy nhiên liệu hóa thạch, gây hiệu ứng nhà kính. Trồng nhiều cây xanh sẽ làm giảm nồng độ khí X trong không khí. Khí X là
Khi xà phòng hóa triolein ( (C17H33COO)3C3H5) thì thu được sản phẩm là
Kim loại X là kim loại cứng nhất, được sử dụng để mạ các dụng cụ kim loại, chế tạo các loại thép chống gỉ, không gỉ…Kim loại X là?
Ancol nào sau đây tác dụng với Cu(OH)2/NaOH tạo dung dịch màu xanh lam?
Công thức cấu tạo của etylamin là
Dung dịch HCl, H2SO4 loãng sẽ oxi hóa crom đến mức oxi hóa nào sau đây?
Ở nhiệt độ thường, kim loại Na phản ứng với nước tạo thành
Saccarozo được biết đến nhiều vì vai trò của nó trong khẩu phần dinh dưỡng của con người và được gọi với nhiều tên như đường kính (đường có độ tinh khiết cao), đường ăn, đường cát, đường trắng, đườngnâu (đường có lẫn tạp chất màu), đường mía (đường trong thân cây mía), đường phèn (đường ở dạng kết tinh), đường củ cải (đường trong củ cải đường), đường thốt nốt. Số nguyên tử cacbon trong phân tử saccarozo là
Cho luồng H2 đi qua 8 g CuO nung nóng. Sau phản ứng thu được 6,72g chất rắn. Hiệu suất khử CuO thành Cu là
Dãy gồm những polime nào sau đây đều là sản phẩm của phản ứng trùng hợp?
Thí nghiệm nào sau đây không xảy ra phản ứng?
Cho dung dịch chứa m gam glucozơ tác dụng với lượng dư AgNO3 trong dung dịch NH3, sau phản ứng hoàn toàn thu được 43,2 gam Ag. Giá trị của m là
Đốt cháy hoàn toàn 13,5 gam etylamin, thu được H2O, N2 và x mol CO2. Giá trị của x là
Rót 1 - 2 ml dung dịch chất X đậm đặc vào ống nghiệm đựng 1 - 2 ml dung dịch Na2CO3. Đưa que diêm đang cháy vào miệng ống nghiệm thì que diêm tắt. Chất X là
Cho m gam Al tác dụng với 2,688 lit O2 (đktc) thì thu được rắn X. Cho rắn X tác dụng với dung dịch HCl dư thì thu được 0,672 lít H2(đktc). Giá trị m là là ( O= 16; Al = 27)
Chất nào sau đây khi đun nóng với dung dịch NaOH thu được sản phẩm có anđehit?
Cho Fe lần lượt tác dụng với lượng dư các chất sau: Dung dịch HCl; Cl2; dung dịch H2SO4 loãng; dung dịch HNO3 loãng, dung dịch AgNO3. Số trường hợp tạo muối sắt (III) là
A. 2
B. 3
C. 4
D. 5
Đun 6,0 gam CH3COOH với C2H5OH dư (xúc tác H2SO4 đặc), thu được 6,6 gam este. Hiệu suất của phản ứng este hóa là
Cho các phát biểu sau:
(1) Thủy tinh hữu cơ (plexiglas) được ứng dụng làm cửa kính ô tô.
(2) Quá trình làm rượu vang từ quả nho xảy ra phản ứng lên men rượu của glucozơ.
(3) Khi ngâm trong nước xà phòng có tính kiềm, vải lụa làm bằng tơ tằm sẽ nhanh hỏng.
(4) Khi rớt axit sunfuric đặc vào vải cotton (sợi bông) thì chỗ vải đó sẽ bị đen rồi thủng.
(5) Dầu mỡ động thực vật bị ôi thiu do liên kết C=C của chất béo bị oxi hóa.
Số phát biểu đúng là
A. 2
B. 5
C. 4
D. 3
Cho các phát biểu sau:
(a) Phân đạm amophot có thành phần chính là: NH4H2PO4 và KNO3.
(b) Điện phân dung dịch NaCl thu được khí Cl2 ở catot.
(c) Sục khí NH3 tới dư vào dung dịch AlCl3 có xuất hiện kết tủa.
(d) Để bảo vệ các vật dụng bằng sắt người ta thường sơn lên bề mặt sắt.
Số phát biểu đúng là
A. 3
B. 1
C. 2
D. 4
Cocain được tách từ lá cây “coca” lần đầu tiên năm 1860. Cocain là một chất gây nghiện, được xếp vào loại ma túy mạnh. Để xác định công thức phân tử của cocain, người ta tiến hành thí nghiệm như sau: Trộn 3,636 gam cocain với 40 gam CuO (dư) rồi nung nóng. Sau phản ứng xảy ra hoàn toàn thấy khối lượng chất rắn còn lại 32,224 gam. Dẫn toàn bộ sản phẩm khí và hơi qua dung dịch H2SO4 đặc, dư, thấy khối lượng dung dịch tăng 2,268 gam và có 4,704 lít hỗn hợp khí thoát ra. Khối lượng phân tử của cocain nhỏ hơn 400 đvC. Biết rằng khi nung nóng hợp chất hữu cơ với CuO xảy ra phản ứng:
Trong phân tử cocain chứa các nguyên tố C, H, O và N. Hãy cho biết công thức phân tử của cocain là:
A.
B.
C.
D.
Đốt cháy hoàn toàn 8,58 gam triglixerit X, thu được H2O và 0,55 mol CO2. Cho 8,58 gam X tác dụng với dung dịch KOH vừa đủ, thu được glixerol và m gam muối. Mặt khác, 8,58 gam X tác dụng được tối đa với 0,02 mol Br2 trong dung dịch. Giá trị của m là ( H =1; C = 12; O = 16; K = 39)
Trong y học, glucozơ làm thuốc tăng lực cho người bệnh, dễ hấp thu và cung cấp khá nhiều năng lượng. Dung dịch glucozơ (C6H12O6) 5% có khối lượng riêng là 1,02 g/ml, phản ứng oxi hóa 1 mol glucozơ tạo thành CO2 và H2O tỏa ra một nhiệt lượng là 2803,0 kJ. Một người bệnh được truyền một chai chứa 500 ml dung dịch glucozơ 5%. Năng lượng tối đa từ phản ứng oxi hóa hoàn toàn glucozơ mà bệnh nhân đó có thể nhận được là
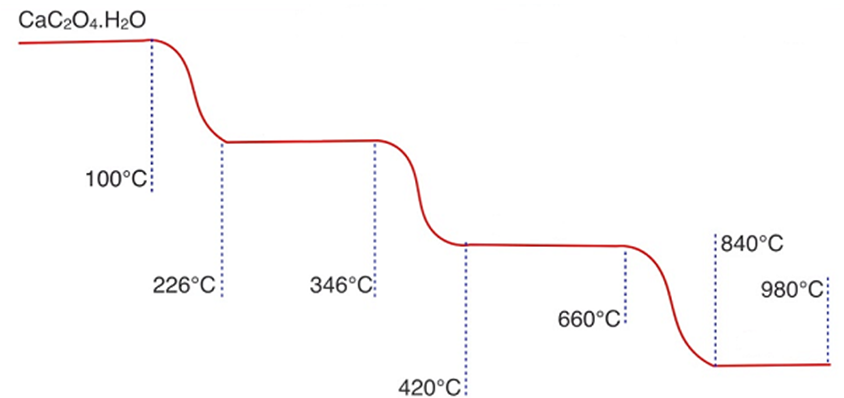
Trong phương pháp phân tích nhiệt, một chất rắn khối lượng m1 được gia nhiệt, thu được chất rắn mới khối lượng m2 và chất khí hoặc hơi. Giản đồ phân tích nhiệt hình dưới cho biết sự biến đổi khối lượng của canxi oxalat ngậm nước CaC2O4.H2O trong môi trường khí trơ theo nhiệt độ:
|
Nhiệt độ |
2260C |
4200C |
8400C |
|
Lượng m2 còn lại so với m1 |
87,7% |
68,5% |
38,4% |
Cho các phương trình hóa học (theo đúng tỉ lệ mol) ứng với ba giai đoạn phân ứng có kèm theo thay đổi khối lượng của các chất rắn như sau:
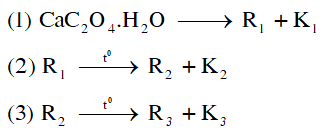
Hỗn hợp E gồm ba este mạch hở, đều tạo bởi axit cacboxylic và ancol. Đốt cháy hoàn toàn 16,12 gam E cần dùng 0,58 mol O2 thu được 0,6 mol CO2. Mặt khác thủy phân hoàn toàn 16,12 gam E bằng dung dịch NaOH dùng dư 20% so với lượng phản ứng thu được dung dịch X và 0,15 mol hỗn hợp Y (gồm hai ancol A và B với tỉ lệ mol 2:1, trong đó MA < MB ). Cô cạn dung dịch X thu được 18,92 gam chất rắn. Phần trăm khối lượng của este có phân tử khối lớn nhất trong E gần nhất giá trị nào sau đây?
Điện phân dung dịch chứa x mol CuSO4, y mol H2SO4 và z mol NaCl (với điện cực trơ, có màng ngăn xốp, hiệu suất điện phân là 100%). Lượng khí sinh ra từ quá trình điện phân và khối lượng Al2O3 bị hòa tan tối đa trong dung dịch sau điện phản ứng với mỗi thí nghiệm được cho ở bảng dưới đây:
|
|
Thí nghiệm 1 |
Thí nghiệm 2 |
Thí nghiệm 3 |
|
Thời gian điện phân (giây) |
t |
2,4t |
3t + 3088 |
|
Lượng khí sinh ra từ bình điện phân (mol) |
0,36 |
1,2 |
p |
|
Khối lượng Al2O3 bị hòa tan tối đa (gam) |
14,28 |
0 |
12,24 |
Biết tại catot ion Cu2+ điện phân hết thành Cu trước khi ion H+ điện phân tạo thành khí H2; có cường độ dòng điện I = 2,5A và không đổi trong các thí nghiệm trên. Giá trị của p gần nhất với giá trị nào sau đây?
Cho sơ đồ chuyển hóa: . Biết: X, Y, Z, E, F là các hợp chất khác nhau, mỗi mũi tên ứng với một phương trình hóa học khác nhau của phản ứng xảy ra giữa hai chất tương ứng. Các chất E, F thỏa mãn sơ đồ trên lần lượt là
Chất hữu cơ E mạch hở có công thức phân tử C6H10O5. Cho E tác dụng với NaOH, thu được ancol X và hai chất hữu cơ Y và Z (MX < MY < MZ và X, Y, Z có cùng số nguyên tử cacbon). Cho chất Z tác dụng với HCl, thu được NaCl và chất hữu cơ T (C2H4O3). Cho các phát biểu sau:
(a) Cho a mol chất T tác dụng với Na dư, thu được a mol khí H2.
(b) Dung dịch chất X tác dụng với Cu(OH)2 ở nhiệt độ thường.
(c) Nung chất Y với NaOH và CaO ở nhiệt độ cao, thu được khí metan.
(d) Chất E tác dụng với Na, giải phóng khí H2.
(e) Từ chất X có thể điều chế trực tiếp được axit axetic.
Số phát biểu đúng là
A. 5
B. 4
C. 3
D. 2