Bộ đề thi thử THPT Quốc gia năm 2022 môn Hóa có lời giải (Đề 20)
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
A. Tính khử: Mg > Cu > Ag.
B. Tính khử: Al > Zn > Fe2+.
C. Tính oxi hóa: Al3+ < Fe2+ < Cu2+.
D. Tính oxi hóa: Mg2+ < Fe3+ < Pb2+.
Cho vài giọt nước brom vào dung dịch phenol, lắc nhẹ thấy xuất hiện
A. có khí thoát ra.
B. dung dịch màu xanh.
C. kết tủa màu trắng.
D. kết tủa màu nâu đỏ.
Để chứng tỏ nhóm -OH đã ảnh hưởng đến vòng benzen trong phenol (C6H5OH) có thể sử dụng phản ứng của phenol với
A. NaOH.
B. nước brom.
C. Na.
D. (CH3CO)2O.
Chất khí nào sau đây không cháy trong khí oxi?
H2S không tác dụng được với chất nào sau đây?
A. dd NaOH.
B. dd CuCl2.
C. SO2.
D. dd MgSO4.
Dãy chất nào sau đây đều làm quỳ tím đổi màu?
A. Phenol, lysin, alanin.
B. Lysin, metylamin, axit glutamic.
C. Glyxin, phenylamin, axir fomic.
D. Anilin, etylamin, axit axetic.
Cho dãy các dung dịch: fructozơ, saccarozơ, Lys-Gly-Ala, Ala-Ala-Gly-Ala, glixerol, propan-1,3-diol. Số dung dịch trong dãy phản ứng được với Cu(OH)2 ở nhiệt độ thường tạo thành dung dịch có màu xanh lam là
A. 3.
B. 4.
C. 2.
D. 5.
Cho m gam axit glutamic tác dụng vừa đủ với 300 ml dung dịch KOH 1M. Giá trị của m là
A. 44,1.
B. 22,05.
C. 21,9.
D. 43,8.
Cho 16,2 gam kim loại M (có hoá trị n không đổi) tác dụng với 3,36 lít O2 (đktc). Hoà tan chất rắn sau phản ứng bằng dung dịch HCl dư thấy thoát ra 13,44 lít H2 (đktc). Kim loại M là
A. Mg.
B. Ca.
C. Fe.
D. Al.
Cho dãy các chất sau: CO2, CO, SiO2, NaHCO3, NH4Cl, FeCl3, P2O5. Số chất trong dãy tác dụng với dung dịch NaOH loãng, ở nhiệt độ thường là
A. 7.
B. 6.
C. 4.
D. 5.
Đốt cháy hoàn toàn m gam một amino axit X mạch hở, thu được V lít khí N2 (đktc). Mặt khác, cho m gam X tác dụng vừa đủ với dung dịch chứa 0,4 mol HCl. Giá trị của V là
A. 17,92.
B. 8,96.
C. 4,48.
D. 2,24.
Trường hợp nào sau đây không xảy ra phản ứng hoá học?
A. Sục khí Cl2 vào dung dịch FeSO4.
B. Cho Fe vào dung dịch H2SO4 loãng nguội.
C. Cho BaCl2 vào dung dịch NaHCO3.
D. Hoà tan P2O5 vào nước.
Để điều chế các kim loại Na, Mg, Al từ hợp chất của chúng, người ta dùng phương pháp
A. thủy luyện.
B. nhiệt luyện.
C. điện phân nóng chảy.
D. điện phân dung dịch.
Kim loại nào sau đây có tính dẫn nhiệt, dẫn điện tốt nhất?
A. Ag.
B. Na.
C. Al.
D. Cu.
Chất nào dưới đây khi tham gia phản ứng trùng ngưng tạo thành tơ nilon–6?
Số nguyên tử Oxi trong phân tử Ala – Gly – Ala – Gly – Glu là
A. 6.
B. 7.
C. 9.
D. 8.
Ở nhiệt độ cao, khí hiđro khử được oxit nào sau đây?
A. CaO.
B. Na2O.
C. CuO.
D. MgO.
Trong phòng thí nghiệm, người ta điều chế CO từ chất nào sau đây?
Phản ứng nào sau đây có phương trình ion rút gọn là: + 2H+ → CO2 + H2O?
A. NaHCO3 + HNO3 → NaNO3 + CO2 + H2O.
B. CaCO3 + 2HCl → CaCl2 + CO2 + H2O.
C. Na2CO3 + H2SO4 → Na2SO4 + CO2 + H2O.
D. NaHCO3 + CH3COOH → CH3COONa + CO2 + H2O.
Cho chuỗi phản ứng sau: N2 → NH3 → NO → NO2 → HNO3 → Cu(NO3)2 → Cu(OH)2. Số phản ứng oxi hóa – khử tối đa có trong chuỗi trên là
A. 2.
B. 3.
C. 4.
D. 5.
Cho m gam glucozơ tác dụng với H2 dư (xúc tác Ni, to, hiệu suất 80%) thu được 36,4 gam sobitol. Giá trị của m là
A. 28,8.
B. 36,0.
C. 45,5.
D. 45,0.
Cho hỗn hợp N2, CO, CO2 và hơi nước. Nhận định nào sau đây là chưa đúng?
A. Hỗn hợp có thể làm xanh muối CuSO4 khan.
B. Hỗn hợp này nặng hơn không khí.
C. Hỗn hợp có thể làm đục nước vôi trong.
D. Hỗn hợp có thể khử được CuO khi nung nóng.
Cho X, Y, Z và T là các chất khác nhau trong số bốn chất sau đây: C2H5NH2, NH3, C6H5OH (phenol), C6H5NH2 (anilin) và các tính chất được ghi trong bảng sau:
|
Chất |
X |
Y |
Z |
T |
|
Nhiệt độ sôi (oC) |
182,0 |
-33,4 |
16,6 |
184,0 |
|
pH (dung dịch nồng độ 0,1 mol/l) |
8,8 |
11,1 |
11,9 |
5,4 |
Nhận xét nào sau đây là đúng?
A. Z là C2H5NH2.
B. Y là C6H5OH.
C. X là NH3.
D. T là C6H5NH2.
So sánh nào sau đây là đúng?
A. Nhiệt độ nóng chảy của anilin lớn hơn alanin.
B. C3H9N có nhiều hơn C3H8O một đồng phân.
C. Lực bazơ của amoniac yếu hơn phenylamin.
D. Nhiệt độ sôi của axit axetic lớn hơn glyxin.
Dẫn 0,6 mol hỗn hợp gồm hơi nước và khí CO2 qua than nung đỏ, thu được 0,9 mol hỗn hợp X gồm CO, H2 và CO2. Cho X hấp thụ hết vào 200 ml dung dịch NaOH 2M, thu được dung dịch Y. Cho từ từ dung dịch Y vào 150 ml dung dịch HCl 1M, thu được V lít khí CO2 (đktc). Giá trị của V là
A. 2,24.
B. 2,52.
C. 4,48.
D. 2,80.
Hỗn hợp X gồm H2, C2H4 và C3H6 có tỉ khối so với H2 là 9,25. Cho 22,4 lít X (đktc) vào bình kín có sẵn một ít bột Ni. Đun nóng bình một thời gian, thu được hỗn hợp khí Y có tỉ khối so với H2 bằng 10. Tổng số mol H2 đã phản ứng là
Cho các phát biểu sau:
(a) Bơ nhân tạo được điều chế bằng phản ứng hiđro hóa chất béo lỏng.
(b) Thành phần chính của sợi bông, gỗ, nứa là xenlulozơ.
(c) Ở nhiệt độ thường, các amin đều là các chất lỏng.
(d) Tơ visco, tơ xenlulozơ axetat đều là các polime bán tổng hợp.
(e) Đốt cháy một mẩu lòng trắng trứng thấy xuất hiện mùi khét như mùi tóc cháy.
(f) Tinh bột khi thủy phân hoàn toàn trong môi trường kiềm thu được glucozơ.
(g) “Đường mía” là thương phẩm có chứa thành phần hoá học là saccarozơ.
(h) Hợp chất H2N–CH(CH3)–COOH3N–CH3 là este của alanin.
Số phát biểu đúng là
A. 5.
B. 4.
C. 3.
D. 2.
Trong sơ đồ thực nghiệm theo hình vẽ sau đây?
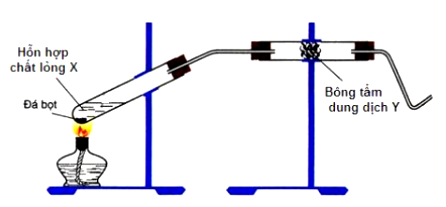
Cho các phát biểu sau:
(1) Chất khí sau khi đi qua bông tẩm NaOH đặc có thể làm mất màu nước brom hoặc KMnO4.
(2) Vai trò chính của bông tẩm NaOH đặc là hấp thụ lượng C2H5OH chưa phản ứng bị bay hơi.
(3) Vai trò chính của H2SO4 đặc là oxi hóa C2H5OH thành H2O và CO2.
(4) Phản ứng chủ yếu trong thí nghiệm là 2C2H5OH (170°C - 180°C) → (C2H5)2O + H2O.
(5) Đá bọt được thêm vào với mục đích làm cho dung dịch sôi đều.
Số phát biểu đúng là
A. 1.
B. 3.
C. 4.
D. 2.
Cho 43,675 gam hỗn hợp X gồm Fe3O4, Fe(NO3)2, Zn tan hoàn toàn trong dung dịch chứa 1,7125 mol KHSO4 loãng. Sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch Y chỉ chứa 258,0625 gam muối sunfat trung hòa và 4,06 lít (đktc) khí Z gồm 2 khí trong đó có một khí hóa nâu ngoài không khí. Biết tỉ khối của Z so với H2 là 365/29. Khối lượng của Zn trong hỗn hợp X là
A. 4,725.
B. 3,675.
C. 4,875.
D. 4,525.
Tiến hành các thí nghiệm sau:
(a) Hấp thụ hết 3 mol khí CO2 vào dung dịch chứa 2 mol Ca(OH)2.
(b) Cho KMnO4 vào dung dịch HCl dư.
(c) Cho Fe3O4 vào dung dịch HCl dư.
(d) Cho dung dịch FeCl2 tác dụng với dung dịch AgNO3 dư.
(e) Cho KHS vào dung dịch NaOH (vừa đủ).
(f) Dẫn khí NO2 vào dung dịch NaOH.
(g) Cho Zn tác dụng với dung dịch chứa FeCl3 dư.
Số thí nghiệm thu được dung dịch có chứa hai muối là
A. 5.
B. 3.
C. 4.
D. 6.
Đốt cháy 19,2 gam Mg trong oxi một thời gian thu được m gam hỗn hợp rắn X. Hòa tan hoàn toàn X cần dùng V lít dung dịch chứa HCl 1M và H2SO4 0,75M thu được dung dịch chứa (3m + 20,8) gam muối. Mặt khác cũng hòa tan X trong dung dịch HNO3 loãng dư thu được 2,24 lít (đktc) hỗn hợp khí Y gồm NO và N2 có tỉ khối so với H2 là 14,4. Số mol HNO3 đã phản ứng là
A. 1,88.
B. 1,92.
C. 1,78.
D. 1,98.
Hỗn hợp X gồm một ancol đơn chức; một axit cacboxylic đơn chức và một axit cacboxylic hai chức (đều no, mạch hở). Đun nóng 15,34 gam X (có H2SO4 đặc, xúc tác), sau một thời gian thu được 2,34 gam H2O và hỗn hợp Y gồm các hợp chất hữu cơ. Đốt cháy hoàn toàn Y thu được 18,92 gam CO2 và 7,20 gam H2O. Nếu cho toàn bộ Y tác dụng với dung dịch KOH dư thì lượng KOH phản ứng là 11,20 gam và thu được m gam muối. Giá trị của m là
A. 19,82.
B. 17,50.
C. 22,94.
D. 12,98.
Điện phân dung dịch X chứa đồng thời 0,04 mol HCl và a mol NaCl (điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi, hiệu suất điện phân 100%) trong thời gian t giây thì thu được 1,344 lít hỗn hợp hai khí trên các điện cực trơ. Mặt khác, khi điện phân X trong thời gian 2t giây thì thu được 1,12 lít khí (đktc) hỗn hợp khí trên anot. Giá trị của a là
A. 0,04.
B. 0,02.
C. 0,06.
D. 0,01.
Cho 1 mol chất X (C6H8O6) mạch hở, tác dụng tối đa với 3 mol NaOH trong dung dịch, thu được các chất có số mol bằng nhau lần lượt là Y, Z, T và H2O. Trong đó, Y đơn chức; T có duy nhất một loại nhóm chức và hoà tan được Cu(OH)2 tạo dung dịch màu xanh lam; Y và Z không cùng số nguyên tử cacbon. Phát biểu nào sau đây đúng?
A. X có hai công thức cấu tạo thỏa mãn.
B. Y có phản ứng tráng bạc.
C. Z và T đều có cùng số nguyên tử cacbon.
D. T có mạch cacbon phân nhánh.
Chất hữu cơ X mạch hở có công thức phân tử C8H12O4. Từ X thực hiện các phản ứng sau:
(a) X + 2NaOH → Y + Z + T (b) X + H2 → E
(c) E + 2NaOH → 2Y + T (d) Y + HCl → NaCl + F
Chất F là
Thực hiện các thí nghiệm sau:
(1) Cho hỗn hợp gồm a mol FeCO3 và a mol Mg vào dung dịch HCl dư, thu được V1 lít khí.
(2) Cho a mol Mg vào dung dịch HNO3 dư, thu được V2 lít khí.
(3) Cho hỗn hợp gồm a mol FeCO3 và a mol Mg vào dung dịch HNO3 dư, thu được V3 lít khí.
Biết khí NO là sản phẩm khử duy nhất của HNO3 trong các thí nghiệm trên và các khí đều đo ở cùng điều kiện. So sánh nào sau đây là đúng?
A. V1 > V2 > V3.
B. V1 = V3 > V2.
C. V1 > V3 > V2.
D. V1 = V3 < V2.
Cho X là este của α-aminoaxit có công thức phân tử C5H11O2N, Y và Z là hai peptit mạch hở được tạo bởi glyxin và alanin có tổng số liên kết peptit là 7. Đun nóng 63,5 gam hỗn hợp E chứa X, Y, Z với dung dịch NaOH vừa đủ, thu được hỗn hợp chứa 2 muối và 13,8 gam ancol T. Đốt cháy toàn bộ hỗn hợp muối cần dùng 2,22 mol O2, thu được Na2CO3, CO2, H2O và 7,84 lít khí N2 (đktc). Phần trăm khối lượng của peptit có khối lượng phân tử nhỏ trong hỗn hợp E là
A. 59,8%.
B. 45,35%.
C. 46,0%.
D. 50,39%.
Hỗn hợp T gồm ba este X, Y, Z mạch hở (MX < MY < MZ và nX = 2nY). Cho 58,7 gam T tác dụng vừa đủ với dung dịch chứa 0,9 mol NaOH, thu được hai muối của axit cacboxylic đơn chức A, B (phân tử hơn kém nhau một nguyên tử cacbon) và một ancol no, mạch hở Z. Dẫn toàn bộ Z qua bình đựng Na dư, thấy bình tăng 27 gam. Phần trăm khối lượng của este Y trong T là
A. 22,48%.
B. 40,20%.
C. 37,30%.
D. 41,23%.
Đốt cháy hoàn toàn a mol chất hữu cơ X (chứa C, H, O) thu được x mol CO2 và y mol H2O với x = y + 5a. Hiđro hóa hoàn toàn 0,2 mol X thu được 43,2 gam chất hữu cơ Y. Đun nóng Y với dung dịch NaOH vừa đủ, cô cạn dung dịch sau phản ứng thu được hỗn hợp E chứa hai muối natri của 2 axit cacboxylic có cùng số nguyên tử cacbon và phần hơi chứa ancol Z. Đốt cháy toàn bộ E thu được CO2, 12,6 gam H2O và 31,8 gam Na2CO3. Số nguyên tử H có trong X là
A. 14.
B. 8.
C. 12.
D. 10.
Cho các phát biểu sau:
(a) Oxi hoá glucozơ bằng hiđro (xúc tác Ni, t°) thu được sobitol.
(b) Cho Cu tác dụng với dung dịch hỗn hợp NaHSO4 và KNO3 thấy có khí thoát ra.
(c) Hỗn hợp Cu và Fe3O4 có số mol bằng nhau có thể tan hết trong dung dịch HCl dư.
(d) Cho dung dịch AgNO3 dư vào dung dịch FeCl2 sau phản ứng thu được hai chất kết tủa.
(e) Muối natri hoặc kali của axit béo được dùng để sản xuất xà phòng.
(f) Để khử mùi tanh của cá trước khi nấu ăn, ta dùng dung dịch giấm ăn.
(g) Đa số các polime không tan trong các dung môi thông thường.
Số phát biểu đúng là
A. 8.
B. 5.
C. 6.
D. 7.