Bộ đề thi thử THPT Quốc gia năm 2022 môn Hóa có lời giải (Đề 29)
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
Đốt cháy hoàn toàn 5,6 gam bột Fe trong bình chứa khí clo dư thu được m gam muối. Giá trị của m là
A. 12,70.
B. 10,65.
C. 16,25.
D. 7,10.
Kim loại nào sau đây không phải là kim loại kiềm?
A. Be.
B. K.
C. Li.
D. Na.
Khi điện phân dung dịch CuSO4 (với các điện cực trơ), ở anot xảy ra
A. sự oxi hóa nước.
B. sự khử nước.
C. sự khử ion Cu2+.
D. sự oxi hóa ion
Số electron lớp ngoài cùng của các nguyên tử kim loại kiềm là
Dẫn khí CO dư qua ống sứ nung nóng đụng hỗn hợp X gồm MgO, Al2O3, Fe3O4 và CuO thu được chất rắn Y (các phản ứng xảy ra hoàn toàn). Thành phần của chất rắn Y là
A. MgO, Al2O3, Fe3O4, Cu.
B. MgO, Al2O3, Fe, Cu.
C. Mg, Al2O3, Fe, Cu.
D. Mg, Al, Fe, Cu.
Este nào sau đây khi thực hiện phản ứng thủy phân thu được sản phẩm không tham gia phản ứng tráng gương?
A. Phenyl fomat.
B. Propyl fomat.
C. Metyl acrylat.
D. Vinyl axetat.
Chất ở thể lỏng trong điều kiện thường là
A. etylamin.
B. axit axetic.
C. phenol.
D. anđehit fomic.
Dãy dung dịch các chất đều làm quỳ tím hóa xanh là
A. amoniac; glyxin; anilin.
B. trimetylamin, lysin, natri axetat.
C. valin, phenol; metylamin.
D. etylamin; anilin; lysin.
Thạch cao nung là muối sunfat ngậm nước của kim loại nào sau đây?
A. Na.
B. Ca.
C. Mg.
D. K.
Thuốc thử để phân biệt glucozơ và fructozơ là
A. nước brom.
C. dung dịch H2SO4
C. dung dịch H2SO4.
D. dung dịch AgNO3 trong NH3.
Để phân biệt ba kim loại K, Ba, Ag chỉ cần dùng dung dịch loãng của
A. KOH.
B. HCl.
C. HNO3.
D. H2SO4.
Kim loại tác dụng được với nước ở nhiệt độ thường là
A. Na.
B. Al.
C. Fe.
D. Ag.
Tích số ion của nước trong dung dịch NaOH 0,01M là
A. [OH-] = 1.10-12
B. [H+][OH-] > 1.10-14
C. [H+][OH-] = 1.10-14.
D. [H+][OH-] < 1.10-14
Polime có cấu trúc mạch phân nhánh là
A. tơ capron.
B. amilopectin.
C. poli(vinyl clorua).
D. cao su lưu hóa.
Công thức phân tử của saccarozơ và tinh bột lần lượt là
A. C12H22O11 và (C6H10O5)n
B. C12H22O11 và C6H10O5
C. C11H22O11 và C6H12O6.
D. C6H12O6 và C12H22O11
A. KCrO2.
B. K2Cr2O12
C. K2CrO4.
D. K2Cr2O7.
Cho thí nghiệm như hình vẽ sau:
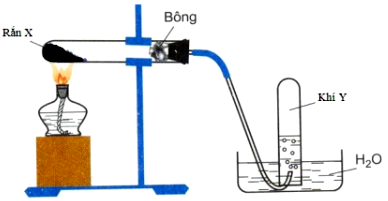
Dãy các khí đều có thể là khí Y trong thí nghiệm trên là
Phát biểu nào sau đây sai?
A. Các ống dẫn nước cứng lâu ngày bị đóng cặn, làm giảm lưu lượng của nước.
B. Nước chứa nhiều ion Ca2+, Mg2+ được gọi là nước cứng.
C. Nguyên tắc làm mềm nước cứng là làm giảm nồng độ các ion Ca2+, Mg2+ trong nước cứng.
D. Tính cứng toàn phần của nước là tính cứng gây nên bởi các muối sunfat, clorua của canxi và magie.
A. 4
B. 3
C. 2
D. 5
Khối lượng bột Al ít nhất cần dùng để khử hoàn toàn 8 gam bột Fe2O3 là
A. 1,35 gam.
B. 2,70 gam.
C. 4,05 gam.
D. 5,40 gam.
Cấu hình electron của nguyên tử Fe (Z = 26) là
Cho 25,6 gam hỗn hợp A ở dạng bột gồm Fe và kim loại M (M có hoá trị không đổi). Chia A thành 2 phần bằng nhau. Cho phần 1 tác dụng với dung dịch HCl dư thu được 0,4 mol khí H2. Cho phần 2 tác dụng hết với dung dịch HNO3 đặc, nóng, dư thấy thoát ra 0,9 mol khí NO2 (là sản phẩm khử duy nhất). Kim loại M là
A. Zn
B. Ni.
C. Cu
D. Mg
Hiện nay, công nghệ sản xuất giấm bằng phương pháp lên men từ các loại tinh bột đang được sử dụng rộng rãi theo sơ đồ sản xuất như sau: Tinh bột → glucozơ → rượu etylic → axit axetic (thành phần chính của giấm). Từ 16,875 tấn bột sắn chứa 90% tinh bột sản xuất được 200 tấn dung dịch axit axetic có nồng độ a%. Biết hiệu suất chung của cả quá trình sản xuất là 80%. Giá trị của a là
A. 5,0
B. 4,5
C. 2,25.
D. 5,6
Xét các phát biểu sau:
(1) Tính bazơ của các amin đều mạnh hơn amoniac.
(2) Tơ visco; tơ nilon-6,6; tơ lapsan thuộc loại tơ hóa học.
(3) Glucozơ bị oxi hóa bởi khí hiđro tạo thành sobitol.
(4) Vinyl axetat được điều chế bằng phản ứng giữa axit axetic và etilen.
(5) Tất cả protein và peptit đều tham gia phản ứng màu biure.
Số phát biểu không đúng là
A. 2
B. 5
C. 3
D. 4
Xét các thí nghiệm sau:
(1) Cho fructozơ vào dung dịch AgNO3 trong NH3 dư, đun nóng.
(2) Cho anilin vào nước brom dư ở nhiệt độ thường.
(3) Cho etyl axetat vào dung dịch H2SO4 20%, đun nóng.
(4) Sục metylamin đến dư vào dung dịch AlCl3.
(5) Cho glyxylalanylvalin dư vào ống nghiệm chứa Cu(OH)2 trong dung dịch NaOH.
(6) Cho metyl fomat vào dung dịch AgNO3 trong NH3 dư, đun nóng.
Sau khi các phản ứng xảy ra hoàn toàn, các thí nghiệm thu được chất rắn không tan là
A. 1, 2, 4, 6
B. 2, 3, 4, 6.
C. 1, 2, 6
D. 1, 2, 4, 5, 6
Cho các chất sau: etylen glicol; Ala-Gly-Val; saccarozơ; anbumin (lòng trắng trứng); glucozơ, axit axetic; Gly-Ala. Số chất có phản ứng với Cu(OH)2 trong môi trường kiềm ở nhiệt độ thường tạo ra hợp chất màu tím là
A. 2.
B. 5
C. 3
D. 6
Cho các phát biểu sau:
(a) Một dung dịch hỗn hợp chứa a mol NaAlO2 và a mol NaOH tác dụng với dung dịch chứa b mol HCl. Để thu được kết tủa sau phản ứng thì a < b < 5a.
(b) Dung dịch A chứa a mol CuSO4 và b mol FeSO4. Thêm c mol Mg vào dung dịch A. Để sau phản ứng dụng dịch thu được chỉ chứa 2 muối thì a ≤ c < a + b.
(c) Cho rất từ từ dung dịch A chứa x mol HCl vào dung dịch B chứa y mol Na2CO3. Sau khi cho hết A vào B thu được dung dịch C. Nếu x < y thì dung dịch C chứa 2 muối.
(d) Có thể tồn tại AgNO3 và Fe(NO3)2 trong cùng một dung dịch.
Số phát biểu sai là
A. 3.
B. 2.
C. 4.
D. 1.
Tiến hành thí nghiệm các dung dịch X1; X2; X3 và X4 với thuốc thử theo bảng sau:
|
Mẫu thử |
Thuốc thử |
Hiện tượng |
|
X1 |
Cu(OH)2 trong môi trường kiềm |
Có màu tím |
|
X2 |
Dung dịch I2 |
Có màu xanh đặc trưng |
|
X3 |
Dung dịch AgNO3 trong NH3 dư, đun nóng |
Kết tủa trắng bạc |
|
X4 |
Dung dịch KMnO4 |
Mất màu thuốc tím |
Dung dịch X1, X2, X3, X4, lần lượt là
A. lòng trắng trứng, hồ tinh bột, saccarozơ, glucozơ.
B. lòng trắng trứng, fructozơ, glucozơ, saccarozơ.
C. hồ tinh bột, saccarozơ, lòng trắng trứng, glucozơ.
D. lòng trắng trứng, hồ tinh bột, fructozơ, glucozơ.
Cho 6,23 gam hỗn hợp gồm CH3COOCH3; CH2=CH-COOCH3; CH3OCOC2H5 phản ứng vừa đủ với dung dịch KOH, đun nóng. Cô cạn dung dịch sau phản ứng thu được m gam chất rắn khan và 2,4 gam hơi ancol. Giá trị của m là
Cho phenyl axetat tác dụng với dung dịch NaOH dư, đun nóng thu được sản phẩm là
A. CH3COOH, C6H5OH.
B. CH3COONa, C6H5OH.
C. CH3COONa, C6H5ONa, H2O.
D. CH3COONa, C6H5CH2OH.
Cho 42,0 gam hỗn hợp X gồm các kim loại Ag và Cu tác dụng hết với dung dịch HNO3 loãng dư thu được 4,48 lít khí NO (đktc, là sản phẩm khử duy nhất). Phần trăm khối lượng của Cu trong hỗn hợp X là
A. 22,86%
B. 66,67%
C. 33,33%
D. 77,14%
Đốt cháy hoàn toàn m gam hỗn hợp X gồm tinh bột, xenlulozơ, saccarozơ, glucozơ, fructozơ trong oxi dư. Hỗn hợp khí và hơi thu được sau phản ứng được sục vào 300 gam dung dịch Ca(OH)2 25,9% thu được 90 gam kết tủa và dung dịch muối có nồng độ phần trăm là 8,65%. Mặt khác, thủy phân hoàn toàn m gam hỗn hợp X trong dung dịch H2SO4 dư, đun nóng, sau đó trung hòa axit bằng dung dịch NaOH thu được dung dịch Y. Cho dung dịch Y vào dung dịch AgNO3 dư trong NH3, đun nóng thu được a gam kết tủa Ag. Giá trị của m và a lần lượt là
A. 70,8 và 21,6.
B. 32,4 và 21,6.
C. 70,8 và 43,2.
D. 32,4 và 43,2.
X1; X2 và X3 là ba peptit mạch hở có . Đốt cháy hoàn toàn x mol mỗi peptit X1, X2, hoặc X3, đều thu được số mol CO2 nhiều hơn số mol H2O là 2x mol. Mặt khác, nếu đun nóng 219 gam hỗn hợp E gồm X1, X2 và 0,3 mol X3 (trong đó số mol X1 nhỏ hơn số mol X2) với dung dịch NaOH dư, thu được dung dịch chỉ chứa muối của glyxin và valin có tổng khối lượng muối là 341,1 gam. Phát biểu nào sau đây là đúng?
A. Trong phân tử X1 có 21 nguyên tử cacbon.
B. Đốt cháy hoàn toàn 0,1 mol X1 thu được số mol CO2 không vượt quá 2,4 mol.
C. Phần trăm khối lượng của X1 trong 219 gam hỗn hợp E là 20,09%.
D. Phần trăm khối lượng của oxi trong X1 là 23,05%.
Cho 36,0 gam hỗn hợp X gồm Al, Mg, ZnO và Fe(NO3)2 tan hết trong dung dịch loãng chứa 0,87 mol H2SO4. Sau khi các phản ứng kết thúc thu được dung dịch Y chỉ chứa 108,48 gam muối sunfat trung hòa (không chứa muối Fe3+) và 4,704 lít (đktc) (ứng với 1,98 gam) hỗn hợp khí X gồm N2 và H2. Thành phần % theo khối lượng của Mg trong hỗn hợp X là
A. 28,0%.
B. 18,0%.
C. 20,0%.
D. 24,0%.
Hỗn hợp A gồm chất X (C5H15N3O5) và chất Y (C6H16N2O4, là muối amoni của axit đa chức, trong phân tử Y không có nhóm COOH tự do). Cho m gam hỗn hợp A phản ứng vừa đủ với dung dịch chứa 32 gam NaOH. Cô cạn dung dịch sau phản ứng thu được hỗn hợp chất rắn khan chứa 3 muối (trong đó có 2 muối hữu cơ có cùng số nguyên tử cacbon và 1 muối vô cơ) và 15,68 lít (đktc) hỗn hợp hơi B gồm 2 amin kế tiếp nhau trong cùng một dãy đồng đẳng, B có tỉ khối so với khí hiđro là 19,5. Giá trị của m là
A. 95,1
B. 65,6
C. 66,4.
D. 73,7
Điện phân dung dịch X (chứa a gam chất tan gồm CuSO4 và NaCl) với cường độ dòng điện không đổi (điện cực trơ, có màng ngăn xốp). Thể tích khí thoát ra ở cả 2 điện cực V lít (đktc) theo thời gian t (s) được biểu diễn trên đồ thị sau:
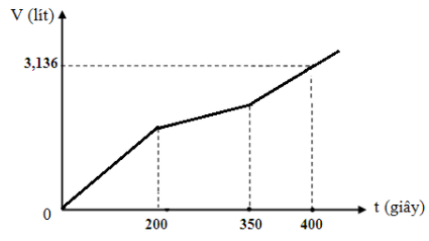
A. 26,53
B. 31,76
C. 28,56
D. 30,59
- Cho phần 1 tác dụng với lượng dư dung dịch HCl, thu được 12,88 lít H2 (đktc).
- Hòa tan phần 2 trong 250 gam dung dịch HNO3 63% đun nóng. Sau khi các phản ứng xảy ra hoàn toàn thì thu được dung dịch Y (không có NH4NO3) và 8,96 lít (đktc) hỗn hợp khí X gồm NO, NO2, N2 và NO (trong đó NO và N2O có phần trăm số mol bằng nhau). Tỉ khối của Z So với hiđro là 19,625. Dung dịch Y tác dụng tối đa với V lít dung dịch NaOH 1M. Giá trị của V là
A. 2,00.
B. 1,95.
C. 2,20.
D. 2,25.
Hòa tan a gam Mg vào 1 lít dung dịch A chứa Fe(NO3)2 0,1M và Cu(NO3)2 0,15M. Sau khi kết thúc các phản ứng thu được dung dịch X và b gam chất rắn Y. Cho dung dịch NaOH tới dư vào X, lọc lấy kết tủa đem nung nóng trong không khí tới khối lượng không đổi thu được 12 gam chất rắn khan Z. Giá trị a và b lần lượt là
A. 6,0 và 15,2.
B. 4,8 và 12,4.
C. 5,4 và 13,8.
D. 3,6 và 9,6.
Cho 9,38 gam hỗn hợp X gồm: đimetyl ađipat; anlyl axetat; glixerol triaxetat và phenyl benzoat thủy phân hoàn toàn trong dung dịch KOH dư, đun nóng, thu được a gam hỗn hợp muối và 2,43 gam hỗn hợp X gồm các ancol. Cho toàn bộ hỗn hợp X, thu được ở trên tác dụng với K dư, thu được 0,728 lít H2 (ở đktc). Mặt khác, đốt cháy hoàn toàn 9,38 gam hỗn hợp X bằng O2 dư, thu được 11,312 lít CO2 (ở đktc) và 5,4 gam H2O. Giá trị a gần nhất với giá trị nào sau đây?