Đề thi thử THPT môn Hóa năm 2022 có đáp án (Mới nhất) - Đề 9
Đây là bản xem thử, hãy nhấn Luyện tập ngay để bắt đầu luyện tập với Sinx
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
Câu 1:
Trong các ion sau đây, ion nào có tính oxi hóa mạnh nhất?
A. Ag+.
B. Zn2+.
C. Ca2+.
D. Cu2+.
Câu 2:
Chất thuộc loại polisaccarit là
A. Xenlulozơ.
B. Glucozơ.
C. Saccarozơ.
D. Fructozơ.
Câu 3:
Amin nào sau đây thuộc loại amin bậc hai?
A. Metylamin.
B. Trimetylamin.
C. Phenylamin.
D. Đietylamin.
Câu 4:
Chất nào sau đây là tripeptit?
A. Ala-Gly.
B. Ala-Ala-Gly.
C. Gly-Gly.
D. Gly-Ala.
Câu 5:
Polime nào dưới đây có tính dẻo là đặc trưng?
A. Poli(vinyl clorua).
B. Cao su.
C. Xenlulozơ.
D. Tơ tằm.
Câu 6:
Etyl fomat có công thức là
A. CH3COOCH3.
B. HCOOCH3.
C. HCOOC2H5.
D. HCOOCH=CH2.
Câu 7:
Số electron lớp ngoài cùng của nguyên tử Na là
A. 2.
B. 4.
C. 3.
D. 1.
Câu 8:
Kim loại nào sau đây tan được trong dung dịch HCl?
A. Ag.
B. Cu.
C. Zn.
D. Au.
Câu 9:
Kim loại nào sau đây tác dụng với Cl2 và dung dịch HCl tạo ra cùng một muối là
A. Fe.
B. Mg.
C. Ag.
D. Cu.
Câu 10:
Tên gọi của chất béo có công thức (CH3[CH2]16COO)3C3H5 là
A. Trilinolein.
B. Tristearin.
C. Triolein.
D. Tripanmitin.
Câu 11:
Kim loại có độ cứng lớn nhất là
A. Vàng.
B. Sắt.
C. Nhôm.
D. Crom.
Câu 12:
Chất nào sau đây là este đơn chức?
A. CH3COOC2H5.
B. CH3COOH.
C. CH2(COOCH3)2.
D. (HCOO)2C2H4.
Câu 13:
Dung dịch H2SO4 có pH = 2. Vậy nồng độ của dung dịch đó bằng
A. 0,5M.
B. 0,005M.
C. 0,02M.
D. 0,01M.
Câu 14:
Tên gọi của peptit H2N-CH2-CONH-CH2-CONHCH(CH3)COOH là
A. Gly-Ala-Ala.
B. Gly-Ala-Gly.
C. Gly-Gly-Ala.
D. Ala-Gly-Gly.
Câu 15:
Trong công nghiệp, kim loại nào sau đây chỉ được điều chế bằng phương pháp điện phân nóng chảy?
A. Cu.
B. Ag.
C. Fe.
D. K.
Câu 16:
Dãy chất nào sau đây là hợp chất hữu cơ
A. C2H4, CH4, C2H6O, C3H9N.
B. NH4HCO3, CH3OH, CH4, CCl4.
C. CO2, K2CO3, NaHCO3, C2H5Cl.
D. (NH4)2CO3, CO2, CH4, C2H6.
Câu 17:
Cho dãy kim loại: Na, Ca, Cu, Fe, K. Số kim loại trong dãy tác dụng với H2O tạo dung dịch bazơ là
A. 2.
B. 4.
C. 3.
D. 1.
Câu 18:
Este nào sau đây khi đun nóng với lượng dư dung dịch NaOH, thu được các sản phẩm hữu cơ đều không làm mất màu nước brom?
A. CH3COOCH=CH2.
B. CH2=CHCOOCH=CH2.
C. CH3COOCH2CH=CH2.
D. CH3CH2COOCH3.
Câu 19:
Vào mùa đông, nhiều gia đình sử dụng bếp than đặt trong phòng kín để sưởi ấm gây ngộ độc khí, có thể dẫn tới tử vong. Nguyên nhân gây ngộ độc là do khí nào sau đây?
A. H2.
B. O2.
C. N2.
D. CO.
Câu 20:
Kali hidrocabonat là một loại thuốc hiệu quả chống lại bệnh nấm mốc được sử dụng trong canh tác hữu cơ. Công thức hóa học của kali hidrocacbonat là
A. K2SO3.
B. K2CO3.
C. KHCO3.
D. KHSO4.
Câu 21:
Trong số các chất sau: xenlulozơ, saccarozơ, fructozơ, glucozơ, tinh bột. Các chất khi thủy phân đến cùng chỉ thu được glucozơ là
A. Tinh bột, xenlulozơ.
B. Tinh bột, saccarozơ.
C. Xenlulozơ.
D. Tinh bột, xenlulozơ.
Câu 22:
Đường fructozơ có nhiều trong mật ong, ngoài ra còn có trong các loại hoa quả và rau xanh như ổi, cam, xoài, rau diếp xoắn, cà chua…rất tốt cho sức khỏe. Công thức phân tử của fructozơ là
A. CH3COOH.
B. C6H12O6.
C. C12H22O11.
D. C6H10O5.
Câu 23:
Cho các polime: (1) polietilen, (2) poli(metyl metacrylat), (3) polibutađien, (4) polistiren, (5) poli(vinyl axetat) và (6) tơ nilon-6,6. Số polime thủy phân trong cả dung dịch axit và dung dịch kiềm là
A. 5.
B. 3.
C. 2.
D. 4.
Câu 24:
Tiến hành thí nghiệm phản ứng tráng gương của glucozơ theo các bước sau đây:
Bước 1: Cho vào ống nghiệm sạch 1ml dung dịch AgNO3 1%, cho thêm một vài giọt dung dịch NaOH 10%, sau đó thêm từng giọt dung dịch NH3 5% và lắc đều cho đến khi kết tủa tan hết
Bước 2: Thêm tiếp 1ml dung dịch glucozơ, hơ nóng nhẹ ống nghiệm trên ngọn lửa đèn cồn trong vài phút
Nhận định nào sau đây là sai?
Bước 1: Cho vào ống nghiệm sạch 1ml dung dịch AgNO3 1%, cho thêm một vài giọt dung dịch NaOH 10%, sau đó thêm từng giọt dung dịch NH3 5% và lắc đều cho đến khi kết tủa tan hết
Bước 2: Thêm tiếp 1ml dung dịch glucozơ, hơ nóng nhẹ ống nghiệm trên ngọn lửa đèn cồn trong vài phút
Nhận định nào sau đây là sai?
A. Sau bước 1, thu được dung dịch trong suốt.
B. Mục đích của việc thêm NaOH vào là để tránh phân hủy sản phẩm.
C. Trong phản ứng trên, glucozơ đóng vai trò là chất khử.
D. Sau bước 2, thành ống nghiệm trở nên sáng bóng như gương.
Câu 25:
Cho m gam Al tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí H2 (đktc). Giá trị của m là
A. 4,05.
B. 2,7.
C. 5,4.
D. 1,35.
Câu 26:
Cho hỗn hợp kim loại Mg, Al, Fe vào dung dịch AgNO3 và Cu(NO3)2. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch chứa 3 muối gồm
A. Mg(NO3)2, Al(NO3)3 và Cu(NO3)2.
B. Mg(NO3)2, Al(NO3)3 và Fe(NO3)2.
C. Mg(NO3)2, Al(NO3)3 và Fe(NO3)3.
D. Mg(NO3)2, Fe(NO3)3 và AgNO3.
Câu 27:
Đốt cháy hoàn toàn 30,96 gam hỗn hợp X gồm glucozơ, saccarozơ và xenlulozơ cần dùng 1,08 mol O2, sản phẩm cháy dẫn qua dung dịch Ca(OH)2 dư thu được dung dịch có khối lượng giảm m gam so với dung dịch ban đầu. Giá trị của m là
A. 38,88.
B. 42,48.
C. 22,28.
D. 46,08.
Câu 28:
Cho 8,76 gam lysin và 22,5 gam glyxin vào dung dịch chứa 0,4 mol KOH, thu được dung dịch Y. Cho Y tác dụng hoàn toàn với dung dịch HCl dư, thu được m gam muối. Giá trị của m là
A. 61,2.
B. 83,59.
C. 82,25.
D. 76,39.
Câu 29:
Cho các phát biểu sau:
1. Thủy tinh hữu cơ plexiglas có thành phần chính là poli(metyl metacrylat)
2. Xenlulozơ triaxetat là polime nhân tạo
3. Polietilen được điều chế bằng phản ứng trùng ngưng
4. Các peptit đều dễ bị thủy phân trong môi trường axit hoặc kiềm
5. Xenlulozơ là nguyên liệu để sản xuất tơ nhân tạo, chế tạo phim ảnh, thuốc súng không khói
1. Thủy tinh hữu cơ plexiglas có thành phần chính là poli(metyl metacrylat)
2. Xenlulozơ triaxetat là polime nhân tạo
3. Polietilen được điều chế bằng phản ứng trùng ngưng
4. Các peptit đều dễ bị thủy phân trong môi trường axit hoặc kiềm
5. Xenlulozơ là nguyên liệu để sản xuất tơ nhân tạo, chế tạo phim ảnh, thuốc súng không khói
Số phát biểu đúng là
A. 5.
B. 3.
C. 4.
D. 2.
Câu 30:
Cho các phát biểu sau:
1. Điện phân dung dịch NaCl, ở anot xảy ra quá trình oxi hóa ion clorua
2. Hợp kim natri-kali dùng làm chất trao đổi nhiệt trong một số lò phản ứng hạt nhân
3. Trong nhóm IA, từ Li đến Cs, khả năng phản ứng với nước giảm dần
4. Nhôm dẫn điện tốt hơn đồng
5. Li được dùng để chế tạo tế bào quang điện
6. Các kim loại Na, Ba, Be đều tác dụng với nước ở nhiệt độ thường
1. Điện phân dung dịch NaCl, ở anot xảy ra quá trình oxi hóa ion clorua
2. Hợp kim natri-kali dùng làm chất trao đổi nhiệt trong một số lò phản ứng hạt nhân
3. Trong nhóm IA, từ Li đến Cs, khả năng phản ứng với nước giảm dần
4. Nhôm dẫn điện tốt hơn đồng
5. Li được dùng để chế tạo tế bào quang điện
6. Các kim loại Na, Ba, Be đều tác dụng với nước ở nhiệt độ thường
Những phát biểu không đúng là
A. (2), (4), (5), (6).
B. (1), (2), (3).
C. (3), (4), (5), (6).
D. (1), (3), (4), (5), (6).
Câu 31:
Tiến hành các thí nghiệm sau:
1. Cho dung dịch AgNO3 dư vào dung dịch FeCl2
2. Sục khí Cl2 vào dung dịch FeCl2
3. Dẫn khí H2 dư qua bột CuO nung nóng
4. Nhiệt phân AgNO3
5. Điện phân dung dịch CuSO4 với điện cực trơ
6. Cho Ba vào dung dịch CuCl2 (dư)
7. Cho bột Cu và FeCl3 theo tỉ lệ mol 1:1 vào nước dư
Sau khi kết thúc phản ứng, số thí nghiệm thu được kim loại là
1. Cho dung dịch AgNO3 dư vào dung dịch FeCl2
2. Sục khí Cl2 vào dung dịch FeCl2
3. Dẫn khí H2 dư qua bột CuO nung nóng
4. Nhiệt phân AgNO3
5. Điện phân dung dịch CuSO4 với điện cực trơ
6. Cho Ba vào dung dịch CuCl2 (dư)
7. Cho bột Cu và FeCl3 theo tỉ lệ mol 1:1 vào nước dư
Sau khi kết thúc phản ứng, số thí nghiệm thu được kim loại là
A. 4.
B. 3.
C. 6.
D. 5.
Câu 32:
Hấp thụ hết a mol khí CO2 vào dung dịch NaOH 1,5M và Ba(OH)2 0,45M. Sau khi kết thúc các phản ứng, thu được 17,73 gam kết tủa và dung dịch X. Cho từ từ dung dịch HCl 1,2M vào X đến khi bắt đầu có khí thoát ra thì đã dùng 200ml. Giá trị của a là
A. 0,15.
B. 0,12.
C. 0,16.
D. 0,20.
Câu 33:
Cho sơ đồ phản ứng theo đúng tỉ lệ mol
(1) X + 2NaOH (t°) → X1 + X2 + X3
(2) 2X1 + H2SO4 → Na2SO4 + 2X4
(3) 2X2 + H2SO4 → Na2SO4 + 2X5
(4) X3 + CuO (t°) → X6 + Cu + H2O
Biết X (C6H10O4) chứa hai chức este, các phân tử X3, X4, X5 có cùng số nguyên tử cacbon. Phát biểu nào sau đây sai?
(1) X + 2NaOH (t°) → X1 + X2 + X3
(2) 2X1 + H2SO4 → Na2SO4 + 2X4
(3) 2X2 + H2SO4 → Na2SO4 + 2X5
(4) X3 + CuO (t°) → X6 + Cu + H2O
Biết X (C6H10O4) chứa hai chức este, các phân tử X3, X4, X5 có cùng số nguyên tử cacbon. Phát biểu nào sau đây sai?
A. Chất X6 bị H2 (xúc tác Ni, t°) oxi hóa, thu được X3.
B. Dung dịch nước của X4 và X5 đều tác dụng với CaCO3.
C. Nhiệt độ nóng chảy của X4 và X5 đều cao hơn X3.
D. Các chất X3, X4, X5 đều tan tốt trong nước.
Câu 34:
Cho m gam hỗn hợp Y gồm 4,2 gam Fe và 1,215 gam Al vào 300ml dung dịch X chứa AgNO3 và Cu(NO3)2. Khi phản ứng kết thúc thu được dung dịch Z và 12,18 gam chất rắn T gồm 3 kim loại. Cho rắn T tác dụng với dung dịch HCl dư thì được 1,008 lít H2 (đktc). Nồng độ mol các chất trong dung dịch X lần lượt là
A. 0,05 và 0,05.
B. 0,10 và 0,20.
C. 0,15 và 0,25.
D. 0,50 và 0,50.
Câu 35:
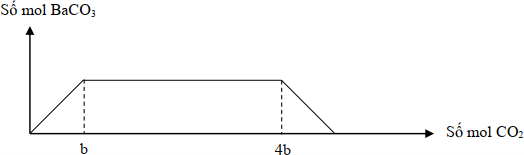
Giá trị của b là
Hòa tan 41,4 gam hỗn hợp gồm Na, Na2O, Ba và BaO vào H2O dư, thu được dung dịch X và b mol H2. Sục từ từ khí CO2 vào X, kết quả thí nghiệm được biểu diễn trên đồ thị sau:

Giá trị của b là
A. 0,225.
B. 0,15.
C. 0,27.
D. 0,18.
Câu 36:
Nung nóng a mol hỗn hợp X gồm propen, axetilen và hidro với xúc tác Ni trong bình kín (giả sử chỉ xảy ra phản ứng cộng H2) thu được hỗn hợp khí Y có tỉ khối so với O2 là 1,0875. Đốt cháy hết Y, thu được 0,024 mol CO2 và 0,03 mol H2O. Biết các phản ứng xảy ra hoàn toàn. Giá trị của a là
A. 0,05.
B. 0,055.
C. 0,022.
D. 0,065.
Câu 37:
Hỗn hợp X gồm glyxin, alanin và axit glutamic. Hỗn hợp Y gồm tristearin và tripanmitin. Đốt cháy hoàn 0,75 mol hỗn hợp Z gồm a gam X và b gam Y cần dùng 217,56 lít O2 ở đktc, sản phẩm cháy gồm N2, CO2 và 128,25 gam H2O. Cho a gam X phản ứng vừa đủ với V ml dung dịch HCl 0,9M. Giá trị của V là
A. 500.
B. 550.
C. 400.
D. 450.
Câu 38:
Cho hỗn hợp bột A gồm Fe, Mg, Al2O3 và một oxit của kim loại X hóa trị 2 không đổi. Lấy 19,74 gam A cho tan hết trong dung dịch HCl thì thu được khí B. Đốt cháy hoàn toàn B bằng một thể tích không khí thích hợp, sau khi đưa về đktc thể tích còn lại 14,784 lít (biết trong không khí thể tích O2 chiếm 20%). Lấy 19,74 gam A cho tác dụng hết với HCl tạo ra H2, trong đó thể tích H2 do Mg tạo ra bằng 1,2 lần do Fe sinh ra. Lấy m gam Mg và m gam X cùng cho tác dụng với dung dịch H2SO4 loãng dư thì thể tích khí H2 sinh ra do Mg nhiều hơn trên 2,5 lần do X sinh ra. Để hòa tan hoàn toàn lượng oxit trong 19,74 gam A phải dùng hết 60ml dung dịch NaOH 2,5M. Xác định phần trăm khối lượng của oxit kim loại X trong A?
A. 12,16%.
B. 31,69%.
C. 12,31%.
D. 18,47%.
Câu 39:
Cho P và Q là hai axit cacboxylic đơn chức, mạch hở; X là este mạch hở tạo từ P, Q và ancol Y. Chia 108,5 gam hỗn hợp Z gồm (P, Q, X) thành 2 phần. Đốt cháy phần 1 cần vừa đủ 47,04 lít O2 (đktc). Cho phần 2 tác dụng vừa đủ với 825 ml dung dịch KOH 1M, cô cạn dung dịch sau phản ứng, thu được 90,6 gam muối và m gam ancol Y. Cho m gam Y vào bình đựng natri dư, sau phản ứng thấy khối lượng bình tăng 13,5 gam. Biết các phản ứng xảy ra hoàn toàn; khối lượng phần 2 gấp 1,5 lần khối lượng phần 1 và MP < MQ. Phần trăm khối lượng của P trong hỗn hợp Z là
A. 19,82%.
B. 42,185%.
C. 11,710%.
D. 20,74%.
Câu 40:
Hỗn hợp X chứa Mg, Fe, Cu, FeO, Fe2O3 và CuO, trong đó oxi chiếm 4,5% khối lượng. Đun nóng m gam X với 0,336 lít khí CO một thời gian thu được chất rắn Y và hỗn hợp khí Z có tỷ khối hơi so với hidro bằng . Hòa tan hết Y trong dung dịch chứa 1,28 mol HNO3, thu được dung dịch T chứa 83,32 gam muối và 2,688 lít hỗn hợp G chứa NO và N2O. Biết G có tỷ khối hơi đối với hidro bằng . Biết thể tích các khí đều đo ở đktc. Giá trị của m là
A. 32,0.
B. 16,0.
C. 12,8.
D. 19,2.