ĐGNL ĐHQG TP.HCM - Vấn đề thuộc lĩnh vực hóa học - Liên kết cộng hóa trị
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
Liên kết cộng hóa trị là liên kết được hình thành giữa 2 nguyên tử bằng
A. 1 electron chung.
B. sự cho nhận proton.
C. 1 hay nhiều cặp electron chung.
D. lực hút tĩnh điện.
Chất nào chỉ chứa liên kết đơn?
A. N2.
B.CH4.
C. CO2.
D. O2.
Liên kết hóa học trong phân tử Br2 thuộc loại liên kết
A. hiđro
B. ion
C. CHT có cực
D. CHT không cực
Trong phân tử sẽ có liên kết cộng hoá trị phân cực nếu cặp electron chung...
A. ở giữa hai nguyên tử.
B. lệch về một phía của một nguyên tử.
C. chuyển hẳn về một nguyên tử.
D. nhường hẳn về một nguyên tử.
Liên kết cộng hóa trị là liên kết
A. giữa các phi kim với nhau.
B. được tạo nên giữa hai nguyên tử bằng một hay nhiều cặp electron chung.
C. trong đó cặp electron dùng chung bị lệch về một nguyên tử.
D. được hình thành do lực hút tĩnh điện giữa các ion mang điện tích trái dấu.
Trong số các chất sau: HF, CaO, CH4, N2, Số lượng các chất có liên kết cộng hóa trị và liên kết ion lần lượt là
A. 2 và 2.
B. 3 và 1.
C.2 và 1.
D. 1 và 3.
Quá trình hình thành liên kết nào dưới đây được mô tả đúng?
A. ![]()
B. 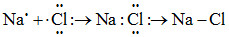
C. 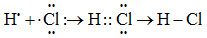
D. 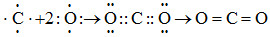
Cho dãy các chất sau: NH3, HCl, O2, Cl2, H2O, CO2. Số chất trong dãy mà phân tử không bị phân cực là
A. 1
B. 4
C. 3
D. 2
Nước đá khô thường được dùng để làm lạnh, giữ lạnh nhằm vận chuyển và bảo quản các sản phẩm dễ hư hỏng vì nhiệt độ. Nước đá khô được dùng nhiều trong các ngành công nghiệp thực phẩm, thủy hải sản và còn được dùng để bảo quản vắc xin, dược phẩm trong ngành Y tế – dược phẩm. Thành phàn nước đá khô là CO2, hãy chỉ ra nội dung sai.
A. Liên kết giữa nguyên tử oxi và cacbon là phân cực
B. Trong phân tử có hai liên kết đôi
C. Phân tử CO2 không phân cực
D. Phân tử có cấu tạo góc
Dãy nào sau đây chỉ gồm những phân tử không phân cực?
A. N2, CO2, Cl2, H2.
B. N2, Cl2, H2, HF.
C. N2, H2O, Cl2, O2.
D. Cl2, HCl, N2, F2.
Liên kết cộng hóa trị trong phân tử HCl có đặc điểm
A. Có một cặp electron chung, là liên kết ba, có phân cực.
B. Có hai cặp electron chung, là liên kết đôi, không phân cực.
C. Có một cặp electron chung, là liên kết đơn, không phân cực.
D. Có một cặp electron chung, là liên kết đơn, phân cực.
Cho dãy các chất : N2, H2, NH3, CO2, HCl, H2O, C2H4. Số chất mà phân tử chỉ chứa liên kết đơn là :
A. 4
B.3
C.1
D. 2
Liên kết hoá học trong phân tử HCl là :
A. liên kết ion.
B. liên kết cộng hoá trị phân cực.
C. liên kết cho - nhận.
D. liên kết cộng hoá trị không phân cực.
Dãy phân tử nào cho dưới đây đều có liên kết cộng hóa trị không phân cực ?
A. N2, SO2, Cl2, H2.
B.N2, Cl2, H2, HCl.
C. N2, HI, Cl2, CH4.
D. Cl2, O2, N2, F2.
Liên kết cộng hóa trị phân cực là liên kết có thể tạo bởi
A. hai nguyên tử của cùng một nguyên tố kim loại.
B. hai nguyên tử của cùng một nguyên tố phi kim.
C. hai nguyên tử của hai nguyên tố phi kim khác nhau.
D. một phân tử kim loại điển hình và một phân tử phi kim điển hình.
Công thức cấu tạo phân tử O2 là
A. O – O
B. O = O
C. O ≡ O
D. O – – O
Cho nguyên tố H (Z = 1) và nguyên tố S (Z = 16). Hợp chất tạo thành từ 2 nguyên tố là
A. HS
B.HS2.
C. H2S.
D. H2S3
Các liên kết trong phân tử nitơ gồm
A. 3 liên kết π.
B.1 liên kết π, 2 liên kết δ.
C. 1 liên kết δ, 2 liên kết π.
D. 3 liên kết δ.
Trong phân tử CH4 có bao nhiêu liên kết ?
A. 4.
B.5.
C. 2.
D. 3.