Tuyển tập 20 đề thi thử THPTQG Hóa Học cực hay có lời giải chi tiết (Đề số 13)
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
Kim loại nào sau đây có nhiệt độ nóng chảy thấp nhất?
A. W
B. Pb
C. Na.
D. Hg
Quặng manhetit là loại quặng giàu sắt nhưng hiếm gặp trong tự nhiên. Thành phần chính của quặng manhetit là:
A. Fe2O3
B. Fe3O4
C. FeS2
D. FeCO3
Phương pháp chủ yếu sản xuất N2 trong công nghiệp là
A. Nhiệt phân muối NH4NO2.
B. Phân hủy protein
C. Nhiệt phân muối NH4NO3
D. Chưng cất phân đoạn không khí lỏng
Benzyl axetat có công thức cấu tạo là
A. CH3COOCH2C6H5
B. HCOOC6H5
C. C6H5CH2COOCH3
D. CH3COOC6H5
Cho sơ đồ: chứng tỏ
A. Ion Cr2O72- tồn tại trong môi trường bazơ
B. Ion CrO42- tồn tại trong môi trường axit
C. Sự chuyển hóa qua lại giữa muối cromat và đicromat
D. Dung dịch từ màu da cam CrO42- chuyển sang dung dịch màu vàng Cr2O72
Số đồng phân amin có công thức phân tử C3H9N là
A. l.
B. 2.
C. 3.
D. 4.
Chất nào sau đây không làm mềm nước cứng tạm thời?
A. Ca(OH)2
B. Na2CO3
C. NaCl
D. NaOH
Công thức của sắt (III) sunfat là
A. Fe2O3
B. FeSO4
C. Fe2(SO4)3
D. Fe(OH)3
Polime nào sau đây được tổng hợp bằng phản ứng trùng hợp?
A. Poli(hexametylen-ađipamit).
B. Poli(etylen-terephtalat).
C. Amilozơ
D. Polistiren
Phương pháp thích hợp điều chế kim loại Ca từ CaCl2 là
A. Điện phân nóng chảy CaCl2
B. Điện phân dung dịch CaCl2.
C. Dùng Na khử Ca2+ trong dung dịch CaCl2
D. Nhiệt phân CaCl2
Cacbohiđrat nào sau đây thuộc loại đisaccarit?
A. Glucozơ
B. Saccarozơ
C. Xenlulozơ
D. Amilozơ
Thí nghiệm nào sau đây thu được muối sắt (II) sau khi kết thúc phản ứng?
A. Fe tác dụng với dung dịch HNO3 loãng dư
B. Fe tác dụng với dung dịch FeCl3
C. Fe, FeO tác dụng với dung dịch HNO3 đặc, nóng, dư
D. Fe tác dụng với dung dịch AgNO3 dư
Cho 2,52 gam kim loại M tác dụng hết với dung dịch H2SO4 loãng, dư; sau phản ứng thu được 6,84 gam muối sunfat trung hoà. Kim loại M là
A. Zn
B. Fe.
C. Mg
D. Al
Hòa tan hoàn toàn m gam hỗn hợp Na và Ba vào nước thu được dung dịch X và 4,48 lít H2 (đktc). Để trung hòa X cần vừa đủ 400ml dung dịch H2SO4 xM. Giá trị của x là
A. 0,5
B. 1,0
C. 0,8
D. 0,4
Cho ba dung dịch riêng biệt: Ala-Ala-Gly; Gly-Ala và hồ tinh bột. Có thể nhận biết được dung dịch Ala-Ala-Gly bằng thuốc thử Cu(OH)2 trong dung dịch NaOH nhờ hiện tượng
A. xuất hiện kết tủa xanh
B. tạo phức màu tím
C. tạo phức màu xanh đậm
D. hỗn hợp tách lớp
Một loại khoai chứa 30% khối lượng là tinh bột được dùng để điều chế ancol etylic bằng phương pháp lên men rượu. Cho biết hiệu suất của toàn quá trình đạt 80%, khối lượng riêng của C2H5OH là 0,8 gam/ml. Khối lượng khoai cần dùng để điều chế được 100 lít ancol etylic 40° là
A. 186,75 kg
B. 191,58 kg
C. 234,78 kg.
D. 245,56 kg
Hỗn hợp X gồm etylamin và đimetylamin. Đốt cháy hoàn toàn m gam X bằng O2, thu được V lít N2 (đktc). Cho m gam X phản ứng vừa đủ với dung dịch HCl, sau phản ứng thu được 16,3 gam muối. Giá trị của V là
A. 4,48
B. 1,12
C. 2,24
D. 3,36
Đặc điểm chung của các phân tử hợp chất hữu cơ là
1. Thành phần nguyên tố nhất thiết phải có C và H.
2. Có thể chứa nguyên tố khác như Cl, N, P, O.
3. Liên kết hóa học chủ yếu là liên kết cộng hóa trị.
4. Liên kết hóa học chủ yếu là liên kết ion.
5. Dễ bay hơi, khó cháy.
6. Phản ứng hóa học xảy ra nhanh.
Nhóm các ý đúng là
A. 4,5,6
B. 1,2,3,5
C. 2,3
D. 2,4,6
Cho các chất nào sau đây: HNO3, NaOH, HClO, NaCl, H2S, CuSO4. Dãy các chất điện ly mạnh là
A. NaCl, H2S, CuSO4
B. HClO, NaCl, CuSO4, H2S
C. NaOH, CuSO4, NaCl, H2S
D. HNO3, NaOH, NaCl, CuSO4
Glucozơ và xenlulozơ có cùng đặc điểm nào sau đây?
A. Là các chất rắn, dễ tan trong nước
B. Tham gia phản ứng tráng bạc
C. Bị thủy phân trong môi trường axit
D. Trong phân tử có nhiều nhóm hiđroxyl (-OH)
Thực hiện các thí nghiệm sau:
(1) Cho dung dịch AgNO3 vào dung dịch HCl.
(2) Cho bột nhôm vào bình kín khí clo.
(3) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3.
(4) Nhỏ ancol etylic vào CrO3.
(5) Sục khí SO4 vào dung dịch thuốc tím.
(6) Ngâm Si trong dung dịch NaOH.
Số thí nghiệm xảy ra phản ứng ở điều kiện thường là
A. 6
B. 4
C. 5
D. 3
Cho dung dịch nước của các chất sau: CH3COOH, C2H4(OH)2, C3H5(OH)3, glucozo, saccarozo, C2H5OH. Số lượng dung dịch có thể hòa tan được Cu(OH)2 là
A. 4
B. 5
C. 1.
D. 3.
Dãy các kim loại được sắp xếp theo chiều giảm dần tính khử (từ trái sang phải) là
A. K, Cu, Fe
B. K, Fe, Cu
C. Fe, Cu, K
D. Cu, K, Fe.
Cho các polime sau: poli(metyl metacrylat), polistiren, poli(etylen terephtalat), teflon, poliacrilonitrin, nilon-6,6. Số polime được tạo thành từ phản ứng trùng hợp là
A.3
B.4
C.2
D.5.
Cho dung dịch chứa hỗn hợp Ba(HCO3)2 và KHCO3 (tỉ lệ mol tương ứng 1:3) vào bình đựng dung dịch Na2CO3 thu được kết tủa X và dung dịch Y. Thêm từ từ dung dịch HCl 1M vào bình đựng đển khi không còn khí thoát ra thì hết 310 ml. Biết toàn bộ Y phản ứng vừa đủ với 300 ml dung dịch NaOH 0,5M. Khối lượng kết tủa của X gần nhất với giá trị nào sau đây?
A. 5,8 gam.
B. 6,8 gam
C. 4,8 gam
D. 7,8 gam
Cho 14,58 gam hỗn hợp X gồm chất béo Y và axit Z (trong đó Y được tạo từ glixerol và axit Z) tác dụng vừa đủ với 0,05 mol NaOH, thu được 0,92 gam glixerol. Khối lượng phân tử của axit Z là
A. 256 đvC
B. 280 đvC
C. 284 đvC
D. 282 đvC
Từ chất X thực hiện các phản ứng (theo đúng tỉ lệ mol):
X + 2NaOH 2Y + Z + H2O
Y+HCl T + NaCl
Z + 2Br2 + H2OCO2 + 4HBr
T + Br2 CO2 + 2HBr
Công thức phân tử của X là
A.C3H4O4
B.C8H8O2
C.C4H6O4
D.C4H4O4
Tiến hành các thí nghiệm sau:
(a) Cho dung dịch AgNO3 vào dung dịch HCl.
(b) Cho Al2O3 vào dung dịch NaOH loãng dư.
(c) Cho Cu vào dung dịch H2SO4 đặc, nóng dư.
(d) Cho Ba(OH) 2 vào dung dịch NaHCO3.
Sau khi kết thúc các phản ứng, số thí nghiệm thu được kết tủa là
A. 1
B. 4.
C. 3
D. 2
Cho các phát biểu sau:
(a) Muối NaHCO3 được dừng làm thuốc chữa đau dạ dày do thừa axit.
(b) Ở nhiệt độ thường, tất cả các kim loại kiềm đều tác dụng được với nước.
(c) Công thức hóa học của thạch cao khan là CaSO4.
(d) Các chất Al(OH)3, NaHCO3, Al2O3 đều lưỡng tính.
(e) Có thể dùng dung dịch NaOH để làm mềm nước cứng tạm thời.
Số phát biểu đúng là
A. 2.
B. 3.
C. 4
D. 5
Hỗn hợp X gồm propin, propen, propan và hiđro. Dẫn 16,8 lít (đktc) hỗn hợp khí X qua Ni (nung nóng) đến phản ứng hoàn toàn, thu được 10,08 lít (đktc) hỗn hợp khí Y. Đốt hoàn toàn Y rồi sục vào dung dịch Ca(OH)2 dư thu được 75 gam kết tủa, đồng thời khối lượng bình chứa tăng thêm m gam. Giá trị của m là
A.54,6
B.96,6
C.51,0
D.21,6
Cho X gam Al tan hoàn toàn dung dịch chứa y mol HCl thu được dung dịch Z chứa 2 chất tan có cùng nồng độ mol. Thêm từ từ dung dịch NaOH vào dung dịch Z thì đồ thị biểu diễn lượng kết tủa phụ thuộc vào lượng OH- như sau:
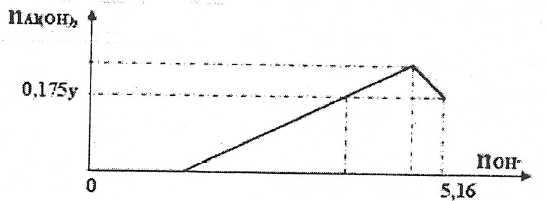
Giá trị của X là
A. 32,4
B. 20,25
C. 26,1
D. 27,0
Cho các phát biểu sau:
(1) Axit axetic có nhiệt độ sôi cao hơn ancol etylic.
(2) Vinyl axetat có khả năng làm mẩt màu nước brom.
(3) Tinh bột khi thủy phân hoàn toàn trong môi trường kiềm chỉ tạo glucozơ.
(4) Dung dịch anbumin của lòng trắng trứng khi đun sôi bị đông tụ.
(5) Phenol dùng để sản xuất thuốc nổ (2,4,6-trinitrophenol).
Số phát biểu đúng là
A. 4
B. 2
C. 3
D. 1
Tiến hành điện phân dung dịch chứa NaCl 0,4M và Cu(NO3) 2 0,5M bằng điện phân điện cực trơ, màng ngăn xốp với cường độ dòng điện không đổi I = 5A trong thời gian 8492 giây thì dừng điện phân, ở anot thoát ra 3,36 lít khí (đktc). Cho m gam bột Fe vào dung dịch sau điện phân, kết thúc phản ứng thấy khí NO thoát ra (sản phẩm khử duy nhất của N+5) và 0,8m gam rắn không tan. Giá trị của m là
A.25,2
B.29,4
C.19,6
D.16,8
Este X đơn chức, mạch hở có tỉ khối hơi so với oxi bằng 3,125. Đốt cháy hoàn toàn 0,3 mol hỗn hợp E chứa X và hai este Y, Z (đều no, mạch hở, không phân nhánh) cần dùng 1,125 mol O2, thu được 1,05 mol CO2. Mặt khác, đun nóng 67,35 gam E với đung dịch KOH vừa đủ thu được hỗn hợp chứa hai ancol có cùng số nguyên tử cacbon và hỗn hợp hai muối có khối lượng m gam. Giá trị của m gần nhất với giá trị nào sau đây?
A.82,9
B.83,9
C.64,9
D.65,0
Cho 86,3 gam hỗn hợp X gồm Na, K, Ba và Al2O3 (trong đó oxi chiếm 19,47% về khối lượng) tan hết trong nước, thu được dung dịch Y và 13,44 lít khí H2 (đktc). Cho V lít dung dịch HCl 0,75M vào dung dịch Y, thu được 23,4 gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị V lớn nhất là
A. 2,4.
B. 3,2.
C. 1,07
D. 1,6
Tiến hành các thí nghiệm với X, Y, Z, T được kết quả theo bảng sau:
|
Mẫu thử |
Thuốc thử |
Hiện tượng |
|
X |
Dung dịch brom |
Tạo kết tủa trắng |
|
Y |
Dung dịch AgNO3 trong NH3 đun nóng |
Tạo kết tủa vàng |
|
Z |
Cu(OH)2 |
Tạo dung dịch màu xanh lam |
|
T |
Quỳ tím |
Hóa đỏ |
X, Y, Z, T lần lượt là
A. anilin, axetilen, saccarozo, axit glutamic
B. axit glutamic, axetilen, saccarozo, anilin
C. anilin, axit glutamic, axetilen, saccarozo
D. anilin, axetilen, axit glutamic, saccarozo
Cho các thí nghiệm sau:
(1) Nhiệt phân Fe(NO3)2.
(2) Cho Mg dư tác dụng với dung dịch FeCl3.
(3) Cho khí NH3 tác dụng với CuO đun nóng.
(4) Đốt cháy HgS bằng O2.
Số thí nghiệm tạo ra đơn chất là
A. 4
B. 5
C. 3.
D. 2.
Hỗn hợp X gồm 3 este đơn chức, tạo thành từ cùng một ancol Y với 3 axit cacboxylic (phân tử chỉ có nhóm -COOH); trong đó, có hai axit no là đồng đẳng kế tiếp nhau và một axit không no (có đồng phân hình học, chứa một liên kết đôi C=C trong phân tử). Thủy phân hoàn toàn 5,88 gam X bằng dung dịch NaOH, thu được hỗn hợp muối và m gam ancol Y. Cho m gam Y vào bình đựng Na dư, sau phản ứng thu được 896 ml khí (đktc) và khối lượng bình tăng 2,48 gam. Mặt khác, nếu đốt cháy hoàn toàn 5,88 gam X thì thu được CO2 và 3,96 gam H2O. Thành phần phần trăm khối lượng của este không no trong X là
A. 40,82%.
B. 34,01%.
C. 29,25%.
D. 38,76%.
Hòa tan hoàn toàn m gam hỗn hợp X chứa Cu, Mg, Fe3O4 và Fe(NO3)2 trong dung dịch chứa 0,61 mol HCl thu được dung dịch Y chỉ chứa (m + 16,195) gam hỗn hợp muối không chứa ion Fe3+ và 1,904 lít hỗn hợp khí Z (đktc) gồm H2 và NO với tổng khối lượng là 1,57 gam. Cho NaOH dư vào Y thấy xuất hiện 24,44 gam kết tủa. Phần trăm khối lượng của Cu có trong X là
A. 22,18%
B. 25,75%
C. 15,92%
D. 26,32%
Cho một octapeptit mạch hở M được tạo từ các aminoaxit (no, mạch hở, phân tử chỉ có 1 nhóm -NH2 và 1 nhóm -COOH). Đốt cháy hoàn toàn m gam M, cần vừa đủ 0,204 mol O2. Cho m gam M tác dụng với dung dịch NaOH vừa đủ, cô cạn dung dịch sau phản ứng thu được hỗn hợp Y chứa muối natri của các aminoaxit. Đốt cháy hoàn toàn Y trong 1,250 mol không khí. Sau khi phản ứng hoàn toàn ngưng tụ hết nước thầy còn 1,214 mol khí. Biết trong không khí O2 chiếm 20% thể tích, còn lại là N2. Giá trị của m gần nhất với giá trị nào sau đây ?
A. 4,3
B. 4,4
C.4,1
D. 4,6