245 Bài tập tổng hợp Hóa vô cơ cực hay có lời giải (P5)
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
Dung dịch của chất nào dưới đây có pH lớn nhất (các dung dịch cùng nồng độ mol) ?
A. K2SO4
B. NaHSO4
C. NaHCO3
D. KH2PO4
Thí nghiệm nào sau đây thu được dung dịch trong suốt và không có chất rắn ?
A. Cho Ba vào dung dịch H2SO4 dư
B. Cho Na vào dung dịch Ca(HCO3)2 dư
C. Cho CrO3 vào dung dịch NaOH loãng dư
D. Cho Cu vào dung dịch AgNO3 dư
Nhận định nào sau đây là không đúng ?
A. Để hạn chế hiện tượng mưa axit gây ra bởi SO2 và NOx ta cần giảm lượng khí thải của các phương tiện giao thông cá nhân và khuyến khích việc sử dụng các phương tiện giao thông công cộng
B. Năng lượng hạt nhân có tiềm năng lớn, là nhóm năng lượng an toàn, bền vững và thân thiện với môi trường
C. Để bảo vệ nguồn tài nguyên biển cần giám sát chặt chẽ quy trình xử lý nước thải công nghiệp trước khi thải ra môi trường
D. Một trong những biện pháp hữu hiệu nhằm giảm bớt tác hại của hiện tượng biến đổi khí hậu là cắt giảm lượng khí CO2 thải ra môi trường
Cho dãy các chất: Ag, Fe3O4, Al(OH)3, PbS, CaCO3 và Fe(NO3)2. Số chất trong dãy tác dụng với dung dịch H2SO4 loãng tạo khí là
A. 1
B. 2
C. 4
D. 3
Cho các phát biểu sau:
1. SiO2 tan tốt trong dung dịch HCl.
2. Tất cả các phản ứng của lưu huỳnh với kim loại đều cần đun nóng.
3. Photpho được bảo quản bằng cách ngâm trong nước.
4. Dung dịch đậm đặc của Na2SiO3 và K2SiO3 được gọi là thủy tinh lỏng.
5. Khí CO2 là chất gây nên hiệu ứng nhà kính, làm cho trái đất bị nóng lên.
6. Phèn chua KAlO2.12H2O dùng để diệt trùng nước trong hệ thống cấp nước sạch.
Số phát biểu không đúng là
A. 5
B. 2
C. 3
D. 4
Trộn V ml dung dịch H3PO4 0,08M với 250 ml dung dịch NaOH 0,32M dư thu được dung dịch X chứa 2 chất tan có cùng nồng độ mol. Giá trị của V là
A. 250 ml.
B. 400 ml
C. 2000 ml.
D.
Cho các phát biểu sau:
a) Các oxit của kim loại kiềm thổ dễ tan trong nước tạo dung dịch bazơ.
b) Các kim loại Cr, Fe, Cu chỉ điều chế được bằng phương pháp nhiệt luyện.
c) SO3 và CrO3 đều là oxit axit, khi tan trong nước cho dung dịch có tính axit mạnh và tính oxi hóa mạnh.
d) Cho Fe vào dung dịch H2SO4 loãng, sau đó thêm tiếp vài giọt dung dịch CuSO4 thấy tốc độ thoát khí tăng.
A. 1
B. 3
C. 2
D. 4
Dung dịch X gồm NaOH xM và Ca(OH)2 yM. Dung dịch Y gồm NaOH yM và Ca(OH)2 xM.
– Hấp thụ 3,136 lít khí CO2 (đktc) vào 200 ml dung dịch X thu được 4 gam kết tủa
– Hấp thụ 3,136 lít khí CO2 (đktc) vào 200 ml dung dịch Y thu được 7 gam kết tủa
Giá trị x : y gần nhất với
A. 1,0
B. 2,0
C. 2,5
D. 1,5
Dung dịch nào sau đây không làm mất màu nước brom ?
A. Metyl fomat
B. Fructozơ
C. Anilin
D. Axit linoleic
Thực hiện thí nghiệm điều chế khí X, khí X được thu vào ống nghiệm theo hình vẽ sau:

Thí nghiệm đó là:
A. Cho Cu vào dung dịch chứa NaHSO4 và Mg(NO3)2.
B. Cho Fe vào dung dịch H2SO4 đặc, nóng.
C. Cho bột CaCO3 vào dung dịch HCl loãng.
D. Cho Al vào dung dịch H2SO4 loãng.
Những nguồn năng lượng nào sau đây là nguồn năng lượng sạch không gây ô nhiễm môi trường?
A. Năng lượng hạt nhân, năng lượng mặt trời
B. Năng lượng than đá, năng lượng mặt trời, năng lượng hạt nhân
C. Năng lượng thuỷ lực, năng lượng gió, năng lượng mặt trời
D. Năng lượng than đá, dầu mỏ, năng lượng thuỷ lực
Tục ngữ có Câu 179Nước chảy đá mòn” trong đó về nghĩa đen phản ánh hiện tượng đá vôi bị hòa tan khi gặp nước chảy. Phản ứng hóa học nào sau đây có thể giải thích hiện tượng này?
A. CaCO3 + CO2 + H2O → Ca(HCO3)2
B. Ca(HCO3)2 → CaCO3 + CO2 + H2O
C. Ca(OH)2 + CO2 → CaCO3 + H2O
D. CaO + CO2 → CaCO3
Cho các phản ứng hóa học:
(a) FeS + 2HCl → FeCl2 + H2S.
(b) NaHS + HCl → NaCl + H2S.
(c) BaS + H2SO4 → BaSO4 + H2S.
(d) K2S + 2HCl → 2KCl + H2S.
Số phản ứng có cùng phương trình ion thu gọn với phản ứng: Na2S + H2SO4 → Na2SO4 + H2S là
A. 1
B. 4
C. 3
D. 2
Cho các chất: AgNO3, Cu(NO3)2, MgCO3, Ba(HCO3)2, NH4HCO3, NH4NO3 và Fe(NO3)2. Nếu nung các chất trên đến khối lượng không đổi trong các bình kín không có không khí, rồi cho nước vào các bình, số bình có thể tạo lại chất ban đầu sau các thí nghiệm là
A. 5
B. 3
C. 6
D. 4
Hoà tan hoàn toàn một lượng Ba vào dung dịch chứa a mol HCl thu được dung dịch X và a mol H2. Trong các chất sau: Na2SO4, Na2CO3, Al, Al2O3, AlCl3, Mg, NaOH, NaHCO3. Số chất tác dụng được với dung dịch X là
A. 6
B. 5
C. 7
D. 4
Tiến hành các thí nghiệm sau:
(a). Điện phân nóng chảy Al2O3 (có criolit)(b). Thực hiện phản ứng nhiệt nhôm với hỗn hợp Al và Cr2O3
(c). Thực hiện phản ứng điện phân dung dịch NaCl (có màng ngăn xốp, điện cực trơ)
(d). Cho mẩu Ba dư vào dung dịch CuSO4
(e). Cho AgNO3 vào lượng dư dung dịch Fe(NO3)2
(g). Cho đinh Fe vào lượng dư dung dịch hỗn hợp Cu(NO3)2 và NaHSO4
Số thí nghiệm thu được kim loại là
A. 5
B. 2
C. 3
D. 4
Dung dịch X có chứa m gam chất tan gồm Na2CO3 và NaHCO3. Nhỏ từ từ đến hết 100ml dung dịch gồm HCl 0,4M và H2SO4 0,3M vào dung dịch X, sau khi phản ứng hoàn toàn thu được 0,04 mol CO2 và dung dịch Y. Nhỏ tiếp Ba(OH)2 dư vào dung dịch Y thu được 18,81 gam kết tủa. Giá trị m là
A. 9,72
B. 13,08
C. 11,40
D. 9,28
Điện phân (với điện cực trơ, màng ngăn xốp, dòng điện có cường độ không đổi) với dung dịch X chứa a mol MSO4 (M là kim loại) và 0,3 mol KCl trong thời gian t giây, thu được 2,24 lít khí ở anot (đktc) và dung dịch Y có khối lượng giảm m gam so với khối lượng dung dịch X. Nếu thời gian điện phân là 2t giây thì thu được dung dịch Z có khối lượng giảm 19,6 gam so với khối lượng dung dịch X. Biết hiệu suất điện phân là 100%, các khí sinh ra không tan trong dung dịch. Có các phát biểu sau:
(a) Giá trị của a là 0,15.
(b) Giá trị của m là 9,8.
(c) Tại thời điểm 2t giây, chưa có bọt khí ở catot.
(d) Tại thời điểm 1,4t giây, nước chưa bị điện phân ở anot.
Số phát biểu đúng là
A. 3
B. 4
C. 2
D. 1
Dung dịch X chứa x mol NaOH và y mol Na2ZnO2; dung dịch Y chứa z mol Ba(OH)2 và t mol Ba(AlO2)2 (trong đó x < 2z). Tiến hành 2 thí nghiệm sau:
– Thí nghiệm 1: Nhỏ từ từ đến dư dung dịch HCl vào dung dịch X;– Thí nghiệm 2:Nhỏ từ từ đến dư dung dịch HCl vào dung dịch Y.
Kết quả 2 thí nghiệm trên được biểu diễn trên đồ thị sau:
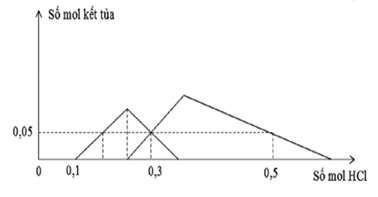
Giá trị của y và t lần lượt là
A. 0,075 và 0,10.
B. 0,15 và 0,05.
C. 0,075 và 0,05.
D. 0,15 và 0,10.
Hòa tan hoàn toàn 8,66 gam hỗn hợp X gồm Mg, Fe3O4 và Fe(NO3)2 bằng dung dịch chứa hỗn hợp gồm 0,52 mol HCl và 0,04 mol HNO3 (vừa đủ), thu được dung dịch Y và 1,12 lít (đktc) hỗn hợp khí Z gồm NO và H2 có tỉ khối hơi đối với H2 là 10,8. Cho dung dịch Y tác dụng với một lượng vừa đủ dung dịch AgNO3 thu được m gam kết tủa và dung dịch T. Cho dung dịch T tác dụng với một lượng dư dung dịch NaOH, lọc kết tủa nung đến đến khối lượng không đổi thu được 10,4 gam chất rắn. Các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây ?
A. 75
B. 79
C. 73
D. 77.
Thí nghiệm nào sau đây không tạo ra khí gây ô nhiễm ?
A. Cho Fe vào dung dịch H2SO4 đặc nóng.
B. Thêm từ từ dung dịch HCl và dung dịch NaHCO3.
C. Cho Cu vào dung dịch chứa Fe(NO3)3 và HCl.
D. Cho Zn vào dung dịch H2SO4 loãng.
Trong các phản ứng sau, có bao nhiêu phản ứng sinh ra đơn chất:
(1) H2S + SO2;
(2) KClO3 (to, MnO2 xúc tác);
(3) CH3CHO + dd AgNO3/NH3, to
(4) NH4NO3 (to);
(5) Mg + dd giấm ăn;
(6) C6H5NH2 + Br2 (dd);
(7) C2H5OH + O2 (men giấm);
(8) Na + cồn 96o;
(9) C3H5(OH)3 + Cu(OH)2;
A. 6
B. 7
C. 5
D. 4
Tiến hành các thí nghiệm sau
(a) Cho Zn vào dung dịch AgNO3
(b) Cho Fe vào dung dịch Fe2(SO4)3
(c) Cho Na vào dung dịch CuSO4
(d) Dẫn khí CO (dư) qua bột CuO nóng
(e) Nung nóng hỗn hợp rắn gồm Au và Mg(NO3)2
(g) Cho Ag vào dung dịch HCl đặc, nóng
Các thí nghiệm xảy ra sự oxi hóa kim loại là
A. 5
B. 3
C. 4
D. 2
Cho vào ống nghiệm một vài tinh thể K2Cr2O7 , sau đó thêm tiếp khoảng 1ml nước và lắc đều để K2Cr2O7 tan hết, thu được dung dịch X. Thêm vài giọt dung dịch KOH vào dung dịch X, thu được dung dịch Y. Màu sắc của dung dịch X và Y lần lượt là:
A. màu vàng chanh và màu da cam
B. màu vàng chanh và màu nâu đỏ
C. màu nâu đỏ và màu vàng chanh
D. màu da cam và màu vàng chanh
Cho các hỗn hợp rắn dạng bột có tỉ lệ số mol trong ngoặc theo thứ tự chất như sau :
(1) Na và Al2O3 (2:1)
(2) Cu và FeCl3 (1:3)
(3) Na, Ba và Al2O3 (1:1:2)
(4) Fe và FeCl3 (2:1)
(5) Al và K (1:2)
(6) K và Sr (1:1)
Có bao nhiêu hỗn hợp có thể tan hết trong nước dư?
A. 6
B. 5
C. 4
D. 3
Cho hỗn hợp X gồm 0,05 mol CaCl2; 0,03 mol KHCO3; 0,05 mol NaHCO3; 0,04 mol Na2O; 0,03 mol Ba(NO3)2 vào 437,85 gam nước. Sau khi các phản ứng xảy ra hoàn toàn thu được kết tủa Y và m gam dung dịch Z. Giá trị của m là
A. 440
B. 450
C. 420
D. 400
Cho sơ đồ phản ứng sau: NaOH → X1 → X2 → X3 → NaOH. Vậy X1, X2, X3 lần lượt là:
A. NaCl, Na2CO3 và Na2SO4.
B. Na2SO4, NaCl và NaNO3.
C. Na2CO3, NaHCO3 và NaCl.
D. Na2SO4, Na2CO3 và NaCl.
Bảng dưới đây ghi lại hiện tượng khi làm thí nghiệm với các chất sau ở dạng dung dịch nước: X, Y, Z và T:
|
Chất Cách làm |
X |
Y |
Z |
T |
|
Thí nghiệm 1: Thêm dung dịch NaOH (dư) |
Có kết tủa sau đó tan dần |
Có kết tủa sau đó tan dần |
Có kết tủa không tan |
Không có kết tủa |
|
Thí nghiệm 2: Thêm tiếp nước brom vào các dung dịch thu được ở thí nghiệm 1 |
Không có hiện tượng |
Dung dịch chuyển sang màu vàng |
Không có hiện tượng |
Không có hiện tượng |
Các chất X, Y, Z và T lần lượt là:
A. MgCl2, CrCl3, AlCl3, KCl
B. CrCl3, AlCl3, MgCl2, KCl
C. CrCl3, MgCl2, KCl, AlCl3
D. AlCl3, CrCl3, MgCl2, KCl
Khí sinh ra trong trường hợp nào sau đây không gây ô nhiễm không khí?
A. Sản xuất nhôm từ quặng boxit.
B. Sản xuất rượu vang từ quả nho chín.
C. Sản xuất giấm ăn từ ancol etylic.
D. Sản xuất xút từ muối ăn
Để phân biệt các dung dịch riêng biệt: Al(NO3)3, FeCl3, KCl, MgCl2, có thể dùng dung dịch:
A. Na2SO4
B. HNO3
C. HCl
D. NaOH
Thực hiện thí nghiệm như hình vẽ bên dưới:
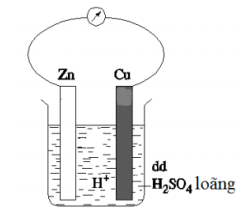
Hãy cho biết phát biểu nào sau đây không đúng ?
A. Thí nghiệm trên mô tả cho quá trình ăn mòn điện hóa học.
B. Thanh Zn bị tan dần và khí hiđro thoát ra ở cả thanh Zn và thanh Cu.
C. Thanh Zn bị tan dần và khí hiđro chỉ thoát ra ở phía thanh Zn.
D. Thanh Zn là cực âm và thanh Cu là cực dương của pin điện.
Cho dãy các chất: NaOH, Sn(OH)2, Pb(OH)2, Al(OH)3, Cr(OH)3. Số chất trong dãy có tính chất lưỡng tính là
A. 1
B. 3
C. 4
D. 2
Tiến hành các thí nghiệm sau:
(a) Cho Al vào lượng dư dung dịch FeCl3;(b) Dẫn khí H2 (dư) qua bột ZnO nung nóng;(c) Cho dung dịch AgNO3 tác dụng với dung dịch Fe(NO3)2 dư;(d) Cho Ba vào dung dịch MgSO4;(e) Nhiệt phân AgNO3;(g) Điện phân dung dịch NaCl với các điện cực trơ, màng ngăn xốp.Số thí nghiệm không tạo thành kim loại là
A. 4
B. 3
C. 2
D. 5
Cho V ml dung dịch K2Cr2O7 0,1M vào dung dịch HC1 đặc, dư thu được 1,344 lít khí Cl2 (đktc). Giá trị của V là
A. 100
B. 300
C. 400
D. 200
Cho các phát biểu sau:
(a) Trong bảng tuần hoàn các nguyên tố hóa học, crom thuộc nhóm VIIIB.
(b) Crom không tan trong dung dịch axit HNO3 và H2SO4 đặc nguội.
(c) Khi thêm dung dịch kiềm vào muối cromat sẽ tạo thành đicromat.
(d) Trong môi trường kiềm, muối crom(III) bị khử thành muối crom(II).
(e) CrO là oxit bazơ, Cr2O3 là oxit lưỡng tính, CrO3 là oxit axit.
(g) CuO nung nóng khi tác dụng với NH3 hoặc CO đều thu được Cu.
(h) Lưu huỳnh, photpho, ancol etylic đều bốc cháy khi tiếp xúc với CrO3.
Số phát biểu đúng là
A. 6
B. 4
C. 5
D. 7
Hòa tan hết 8,1 gam kim loại M vào dung dịch HCl lấy dư thấy thu được 10,08 lít khí H2 (đktc). Nhận xét về kim loại M là đúng?
A. M tác dụng với dung dịch HCl và NaOH.
B. M là kim loại nặng.
C. M có độ dẫn điện lớn hơn so với Cu.
D. M được điều chế bằng nhiệt luyện
Cho các phát biểu sau:(a) Thép là hợp kim của sắt chứa từ 2–5% khối lượng cacbon.
(b) Bột nhôm trộn với bột sắt(III) oxit dùng để hàn đường ray bằng phản ứng nhiệt nhôm.
(c) Dùng Na2CO3 để làm mất tính cứng tạm thời và tính cứng vĩnh cửu của nước.
(d) Dùng bột lưu huỳnh để xử lí thủy ngân rơi vãi khi nhiệt kế bị vỡ.
(e) Khi làm thí nghiệm kim loại đồng tác dụng với dung dịch HNO3, người ta nút ống nghiệm bằng bông tẩm dung dịch kiềm.Số phát biểu đúng là
A. 3
B. 2
C. 4
D. 5
Nung m gam hỗn hợp X gồm KHCO3 và CaCO3 ở nhiệt độ cao đến khối lượng không đổi, thu được chất rắn Y. Cho Y vào nước dư, thu được 0,25m gam chất rắn Z và dung dịch E. Nhỏ từ từ dung dịch HCl 1M vào E, khi khí bắt đầu thoát ra cần dùng V1 lít dung dịch HCl và khi khí thoát ra hết, thì thể tích dung dịch HCl đã dùng là V2 lít. Tỉ lệ V1 : V2 là:
A. 2 : 3
B. 3 : 5
C. 5 : 6
D. 3 : 4
Một loại phân kali chứa 59,6% KCl, 34,5% K2CO3 về khối lượng, còn lại là SiO2. Độ dinh dưỡng của loại phân bón trên là
A. 61,10
B. 60,20
C. 50,70
D. 49,35
Cho các phát biểu sau:
(1) Khí gây ra mưa axit chủ yếu là SO2 và NO2.
(2) Khí gây ra hiện tượng hiệu ứng nhà kính chủ yếu là CO2 và CH4.
(3) Seduxen, mocphin... là các chất gây nghiện.
(4) Đốt than đá dễ sinh ra khí CO là chất khí rất độc.
(5) Metanol có thể dùng để uống như etanol.
Số phát biểu sai là:
A. 4
B. 2
C. 1
D. 3
Cho các cặp chất với tỉ lệ số mol tương ứng như sau :
(a) Fe3O4 và Cu (1:1) (b) Na và Zn (1:1) (c) Zn và Cu (1:1)
(d) Fe2(SO4)3 và Cu (1:1) (e) FeCl2 và Cu (2:1) (g) FeCl3 và Cu (1:1)
Số cặp chất tan hoàn toàn trong một lượng dư dung dịch HCl loãng nóng là
A. 2
B. 5
C. 3
D. 4
Cho các phát biểu sau:
(1) Độ dinh dưỡng của phân kali được đánh giá bằng hàm lượng phần trăm của kali trong phân.
(2) Phân lân có hàm lượng photpho nhiều nhất là supephotphat kép (Ca(H2PO4)2)
(3) Nguyên liệu để sản xuất phân lân là quặng photphorit và quặng cacnalit.
(4) Photpho đỏ không tan trong nước, dễ tan trong dung môi hữu cơ.
(5) Đốt metan trong khí clo sinh ra CCl4.
(6) Phân hỗn hợp chứa nitơ, photpho, kali được gọi chung là phân NPK.
Số phát biểu đúng là:
A. 3
B. 4
C. 5
D. 2
Thực hiện các thí nghiệm sau:
(1) Cho NaHCO3 vào dung dịch CH3COOH.
(2) Cho phân ure vào dung dịch Ba(OH)2 đun nóng.
(3) Cho Fe2O3 vào dung dịch HNO3 đặc, nóng.
(4) Cho P vào dung dịch H2SO4 đặc, nóng.
(5) Cho Al4C3 vào nước.
(6) Cho phèn chua vào nước cứng toàn phần.
(7) Cho dung dịch HCl vào dung dịch Na2CO3.
Số thí nghiệm chắc chắn có khí thoát ra là:
A. 3
B. 2
C. 5
D. 4
Hấp thụ hoàn toàn V lít CO2 vào 250ml dung dịch hỗn hợp NaOH 0,4M và KOH aM thì thu được dung dịch X. Cho từ từ 250 ml dung dịch H2SO4 0,5M vào X thu được dung dịch Y và 1,68 lít khí. Cho Y tác dụng với Ba(OH)2 dư thấy xuất hiện 34,05 gam kết tủa trắng. Biết các khí đo ở đktc, giá trị của a là
A. 0,5M.
B. 0,7M.
C. 0,6M.
D. 0,9M.