280 Bài tập Kim loại kiềm, kiềm thổ, nhôm cực hay có lời giải chi tiết (P2)
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
Hòa tan hoàn toàn 25,3 gam hỗn hợp X gồm Mg, Al và Zn bằng dung dịch HNO3. Sau khi phản ứng kết thúc thu được dung dịch Y và 4,48 lít (đkc) khí Z (gồm hai hợp chất khí không màu) có khối lượng 7,4 gam. Cô cạn dung dịch Y thu được 122,3 gam hỗn hợp muối. Số mol HNO3 đã tham gia phản ứng gần nhất với giá trị nào sau đây?
A. 14,865 gam
B. 14,775 gam
C. 14,665 gam
D. 14,885 gam
Hoà tan 2,3 gam kim loại R vào nước, sau phản ứng thu được 1,12 lít H2 (đktc). Kim loại R là:
A. Li.
B. Na.
C. K.
D. Ba.
Cho hỗn hợp các kim loại kiềm Na, K hoà tan hết vào nước được dung dịch A và 0,672 lít khí H2 (đktc). Thể tích dung dịch HCl 0,1M cần để trung hoà hết một phần ba dung dịch A là:
A. 100ml.
B. 200ml.
C. 300ml.
D. 600ml.
Hòa tan hoàn toàn 8,975 gam hỗn hợp gồm Al, Fe và Zn vào một lượng vừa đủ dung dịch H2SO4 loãng . Sau phản ứng thu được V lít khí H2 (đktc) và dung dịch X. Cô cạn dung dịch X thu được 32,975 gam muối khan. Vậy giá trị của V là
A. 6,72 .
B. 5,6.
C. 11,2.
D. 4,48.
Các dung dịch nào sau đây đều có tác dụng với Al2O3?
A. Na2SO4, HNO3.
B. HNO3, KNO3.
C. HCl, NaOH.
D. NaCl, NaOH.
Kim loại nào sau đây tan hết trong nước dư ở nhiệt độ thường.
A. Na
B. Fe
C. Mg
D. Al
Cho 40,5 gam kim loại R (có hóa trị không đổi) tác dụng với dung dịch axit clohiđric dư thì thu được 50,4 lít khí (đktc). Kim loại R là
A. Mg.
B. Al.
C. Zn.
D. Fe.
Hòa tan hoàn toàn 8,9 gam hỗn hợp gồm Mg và Zn bằng lượng vừa đủ 500 ml dung dịch HNO3 1M. Sau khi các phản ứng kết thúc, thu được 1,008 lít khí N2O (đktc) duy nhất và dung dịch X chứa m gam muối. Giá trị của m là
A. 31,22.
B. 34,10.
C. 33,70.
D. 34.32.
Dung dịch X chứa a mol Ba(OH)2 và b mol NaOH. Sục khí CO2 dư vào dung dịch X, ta thấy lượng kết tủa biến đổi theo đồ thị: (các đơn vị được tính theo mol)

Giá trị a + b là
A. 0,8.
B. 1,0.
C. 1,6.
D. 1,8.
Cho m gam hỗn hợp Al và Na vào nước dư, sau khi các phản ứng xảy ra hoàn toàn, thu được 2,24 lít khí H2 (đktc) và 2,35 gam chất rắn không tan. Giá trị của m là
A. 4,35
B. 4,85
C. 6,95
D. 3,70
Thí nghiệm nào sau đây khi kết thúc không có kết tủa
A. Cho dung dịch AlCl3 dư vào dung dịch NaOH.
B. Cho Ba dư vào dung dịch NH4HCO3
C. Cho dung dịch NaHCO3 dư vào dung dịch Ca(OH)2
D. Cho dung dịch HCl dư vào dung dịch NaAlO2.
Khi nhỏ từ từ đến dư dung dịch NaOH vào dung dịch hỗn hợp gồm a mol HCl và b mol ZnCl2, kết quả thí nghiệm được biểu diễn trên đồ thị sau: (các đơn vị được tính theo mol)

Giá trị a và b lần lượt là:
A. 0,1 và 0,15.
B. 0,3 và 0,25.
C. 0,8 và 0,25.
D. 0,3 và 0,15.
Hòa tan hết m gam hỗn hợp X gồm Mg, MgO, Mg(HCO3)2, MgSO3 bằng một lượng vừa đủ dung dịch H2SO4 30%, thu được 11,2 lít (đktc) hỗn hợp khí Y và dung dịch Z có nồng độ 36%. Tỉ khối của Y so với He bằng 8. Cô cạn Z được 72 gam muối khan. Giá trị của m là
A. 20.
B. 36.
C. 12.
D. 25.
Cho hỗn hợp gồm bột nhôm và oxit sắt. Thực hiện hoàn toàn phản ứng nhiệt nhôm (giả sử chỉ có phản ứng oxit sắt thành Fe) thu được hỗn hợp chất rắn B có khối lượng 19,82 g. Chia hỗn hợp thành 2 phần bằng nhau:
- Phần 1: cho tác dụng với một lượng dư dung dịch NaOH thu được 1,68 lít khí H2 (đktc).
- Phần 2: cho tác dụng với một lượng dư dung dịch HCl thì có 3,472 lít khí H2 (đktc) thoát ra.
Công thức của oxit sắt là
A. Fe2O3.
B. Fe3O4.
C. FeO.
D. Không xác định được.
Chia m gam hỗn hợp Na2O và Al2O3 thành 2 phần bằng nhau:
- Phần 1: Hoà tan trong nước dư thu được 1,02 gam chất rắn không tan.
- Phần 2: Hoà tan vừa hết trong 140 ml dung dịch HCl 1M. Giá trị của m là
A. 2,26.
B. 2,66.
C. 5,32.
D. 7,00.
Điện phân 400 ml dung dịch CuSO4 0,2M với cường độ I = 10A trong thời gian t, ta thấy có 224 ml khí (đktc) thoát ra ở anot. Giả thiết rằng điện cực trơ và hiệu suất điện phân bằng 100%. Khối lượng catot tăng lên là
A. 1,28 gam.
B. 5,12 gam.
C. 2,11 gam.
D. 3,10gam.
Cho dung dịch X chứa 3,82 g hỗn hợp 2 muối sunphat của một kim loại kiềm và một kim loại hoá trị II. Thêm vào dung dịch X một lượng vừa đủ dung dịch BaCl2 thì thu được 6,99 g kết tủa. Nếu bỏ lọc kết tủa rồi cô cạn dung dịch thì được lượng muối khan thu được là
A. 3,170 g.
B. 2,005 g.
C. 4,020 g.
D. 3,070 g.
Nhiệt phân 3,0 gam MgCO3 một thời gian thu được khí X và hỗn hợp rắn Y. Hấp thụ hoàn toàn X vào 100 ml dung dịch NaOH x M thu được dung dịch Z. Dung dịch Z phản ứng với BaCl2 dư tạo ra 3,94 gam kết tủa. Để trung hoà hoàn toàn dung dịch Z cần 50 ml dung dịch KOH 0,2M. Giá trị của X và hiệu suất phản ứng nhiệt phân MgCO3 lần lượt là
A. 0,75 và 50%.
B. 0,5 và 66,67%.
C. 0,5 và 84%.
D. 0,75 và 90%.
Hòa tan hoàn toàn 7,5 gam hỗn hợp gồm Mg và Al bằng lượng vừa đủ V lít dung địch HNO3 1M. Sau khi các phản ứng kết thúc thu được 0,672 lít N2 (đktc) duy nhất và dung dịch chứa 54,9 gam muối. Giá trị của V là
A. 0,36.
B. 0,65.
C. 0,86.
D. 0,70.
Có 3,94 gam hỗn hợp X gồm bột Al và Fe3O4 (trong đó Al chiếm 41,12% về khối lượng), thực hiện phản ứng nhiệt nhôm hoàn toàn hỗn hợp X trong chân không thu được hỗn hợp Y. Hòa tan hoàn toàn Y trong dung dịch chứa 0,314 mol HNO3 thu được dung dịch Z chỉ có các muối và 0,021 mol một khí duy nhất là NO. Cô cạn dung dịch Z, rồi thu lấy chất rắn khan nung trong chân không đến khối lượng không đổi thu được hỗn hợp khí và hơi T. Khối lượng của T gần giá trị nào nhất sau đây?
A. 14,58 gam.
B. 15,35 gam.
C. 15,78 gam.
D. 14,15 gam.
Cho từ từ dung dịch chứa a mol HCl vào dung dịch chứa b mol Na2CO3 đồng thời khuấy đều, thu được V lít khí (ở đktc) và dung dịch X. Khi cho dư nước vôi trong vào dung dịch X thấy có xuất hiện kết tủa. Biểu thức liên hệ giữaV với a, b là:
A. V = 22,4.(a-b)
B. V = 22,4.(a+b)
C. V = 11,2.(a-b)
D. V = 11,2.(a+b)
Cho 10 mL dung dịch hỗn hợp HNO3 1M và H2SO4 0,5M. Thể tích dung dịch NaOH 1M cần để trung hòa dung dịch axit trên là
A. 0,02 lít.
B. 0,01 lít.
C. 0,05 lít.
D. 0,04 lít.
Cho 500 ml dung dịch NaOH 1M vào 150 ml dung dịch AlCl3 aM, sau khi kết thúc phản ứng thu được 7,8 gam kết tủa. Giá trị của a là:
A. 1,0.
B. 0,6.
C. 2,0.
D. 0,5.
Cho 7,84 lít hỗn hợp khí X (đktc) gồm Cl2 và O2 phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là
A. 75,68%.
B. 24,32%.
C. 51,35%.
D. 48,65%.
Hòa tan 6,5 gam Zn vào 200 ml dung dịch H2SO4 2M thu được dung dịch X. Thêm từ từ 550 ml dung dịch Ba(OH)2 1M vào dung dịch X thu được m gam kết tủa. Giá trị của m là
A. 126,40.
B. 121,45.
C. 116,50.
D. 99,32.
Thực hiện phản ứng nhiệt nhôm hỗn hợp gồm Al và m gam hai oxit sắt trong khí trơ, thu được hỗn hợp rắn X. Cho X tác dụng với dung dịch NaOH dư, thư được dung dịch Y, chất không tan Z và 0,672 lít khí H2 (đktc). Sục CO2 dư vào Y, thu được 7,8 gam kết tủa. Cho Z tan hết vào dung dịch H2SO4 đặc, nóng thu được dung dịch chứa 15,6 gam muối sunfat và 2,464 lít SO2 (đktc, sản phẩm khử duy nhất của ), các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 6,48.
B. 6,96.
C. 6,29.
D. 5,04.
Dẫn từ từ 15.68 lít khí NH3 (đktc) vào 200 ml dung dịch AlCl3 1M thu được m gam kết tủa. Giá trị của m là
A. 18,2.
B. 15,6.
C. 54,6.
D. 7,8.
Cho 8,1 gam Al tác dụng với O2, sau một thời gian thu được 12,9 gam chất rắn X. Cho X tác dụng với dung dịch HCl dư thu được V lít khí H2 (đktc). Giá trị của V là
A. 0
B. 5,04.
C. 3,36.
D. 2,24.
Cho 23,45 gam hỗn hợp Ba và K vào 125 ml dung dịch AlCl3 1M thu được V lít H2 (đktc), dung dịch A và 3,9 gam kết tủa. Giá trị của V là
A. 10,08.
B. 3,92.
C. 5,04.
D. 6,72.
Hỗn hợp X gồm Al, Mg, Zn. Cho 19,1 gam hỗn hợp X tác dụng với oxi, sau một thời gian thu được 25,5 gam chất rắn Y. Hòa tan hoàn tan Y trong dung dịch HCl dư, thu được 6,72 lít khí H2 (đktc) và dung dịch Z. Cô cạn Z, thu được m gam hỗn hợp muối khan, Giá trị của m là
A. 47,5
B. 40,4.
C. 53,9.
D. 68,8.
Sục CO2 vào dung dịch chứa hỗn hợp gồm a mol Ca(OH)2 và b mol KOH. Ta quan sát hiện tượng theo đồ thị. Giá trị của x là (các đơn vị được tính theo mol)
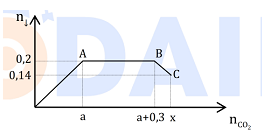
A. 0,52.
B. 0,56.
C. 0,50.
D. 0,58.
Sản phẩm cuối cùng thu được khi nhiệt phân hoàn toàn hỗn hợp rắn X gồm Ba(HCO3)2 và Na2CO3 là
A. BaCO3, Na2CO3.
B. BaO, Na2O.
C. BaO, Na2CO3.
D. BaCO3, Na2O
Tính chất không phải của kim loại kiềm là
A. có nhiệt độ nóng chảy thấp.
B. có số oxi hóa là +1 trong các hợp chất.
C. có độ cứng cao.
D. có tính khử mạnh.
Hỗn hợp X gồm Na và Al (số mol bằng nhau). Hòa tan 10 gam X trong nước dư thu được dung dịch Y. Chất tan có trong Y là
A. NaOH.
B. NaAlO2
C. AlCl3.
D. Na2AlO2.
Thêm từ từ V ml dung dịch Ba(OH)2 0,1M vào 120 ml dung dịch HNO3 1M, cô cạn dung dịch sau phản ứng, làm khô thu được 17,37 gam chất rắn khan. Giá trị của V là
A. 500.
B. 700.
C. 600.
D. 300.
Cho m gam hỗn hợp X gồm Mg và Al vào dung dịch HCl dư thu được 8,96 lít khí . Mặt khác, cho m gam hỗn hợp tác dụng với dung dịch NaOH dư, thu được 6,72 lít khí. Thể tích khí đo ở điều kiện tiêu chuẩn. Giá trị của m là
A. 10,20.
B. 6,45.
C. 7,80.
D. 14,55.
Trong công nghiệp nhôm được sản xuất bằng phương pháp
A. điện phân nóng chảy AlCl3.
B. dùng CO khử Al2O3 ở nhiệt độ cao.
C. dùng Mg khử Al3+ trong dung dịch.
D. điện phân nóng chảy Al2O3.
Cho các phát biểu sau:
(1) Để một miếng gang (hợp kim sắt – cacbon) ngoài không khí ẩm, sẽ xảy ra sự ăn mòn điện hóa.
(2) Kim loại cứng nhất là W (vonframe).
(3) Hòa tan Fe3O4 bằng dung dịch HCl vừa đủ, thu được dung dịch chứa hai muối.
(4) Khí điện phân NaCl nóng chảy (điện cực trơ), tại catot xảy ra sự oxi hóa ion Na+.
(5) Không thể dùng khí CO2 để dập tắt đám cháy magie hoặc nhôm.
Số phát biểu đúng là
A. 2.
B. 4.
C. 1.
D. 3.
Cho từ từ dung dịch HCl cào dung dịch chứa a mol Ba(AlO2)2 và b mol Ba(OH)2. Số mol Al(OH)3 tạo thành phụ thuộc vào số mol HCl được biểu diễn bằng đồ thị hình bên. Tỉ lệ a : b tương ứng là

A. 4 : 9.
B. 9 : 4.
C. 7 : 4.
D. 4 : 7.
Cho 3 kim loại thuộc chu kỳ 3: 11Na, 12Mg, 13Al. Tính khử của chúng giảm theo thứ tự là:
A. Na > Mg > Al.
B. Al > Mg > Na.
C. Mg > Al > Na.
D. Mg > Na > Al.