310 câu Lý thuyết Crom - Sắt - Đồng có lời giải chi tiết (P2)
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
Nhiệt phân trong không khí đến khi khối lượng chất rắn không thay đổi, thu được
A.
B. FeO
C.
D.
Khi cho tác dụng với thu được hỗn hợp gồm
A.
B.
C.
D.
Dãy các muối nào sau đây khi nhiệt phân thu được sản phẩm là oxit kim loại, khí và khí
A.
B.
C.
D.
Để phân tích định tính các nguyên tố trong hợp chất hữu cơ, người ta thực hiện một thí nghiệm được mô tả như hình vẽ:
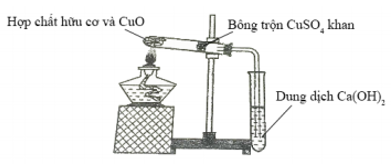
Phát biểu nào sau đây đúng?
A. Thí nghiệm trên dùng để xác định nitơ có trong hợp chất hữu cơ
B. Bông trộn khan có tác dụng chính là ngăn hơi hợp chất hữu cơ thoát ra khỏi ống nghiệm
C. Trong thí nghiệm trên có thể thay dung dịch bằng dung dịch
D. Thí nghiệm trên dùng để xác định clo có trong hợp chất hữu cơ
Chất nào sau đây vừa phản ứng được với dung dịch HCl vừa tác dụng được với dung dịch NaOH loãng?
A.
B.
C.
D.
Thí nghiệm nào sau đây không xảy ra phản ứng hóa học?
A. Cho kim loại Fe vào dung dịch
B. Cho kim loại Mg vào dung dịch
C. Cho kim loại Zn vào dung dịch
D. Cho kim loại Ag vào dung dịch
Cho dãy chuyển hóa sau:
Các chất lần lượt là:
A.
B.
C.
D.
Bột Ag có lẫn tạp chất là bột Fe và Cu. Để thu được Ag tinh khiết mà không bị thay đổi khối lượng trong hỗn hợp ban đầu có thể ngâm hỗn hợp vào một lượng dư dung dịch X, sau đó lọc lấy Ag. Dung dịch X là
A.
B. HCl
C. NaOH
D.
Cho các phát biểu sau:
(a) Dung dịch hỗn hợp làm mất màu dung dịch
(b) có trong tự nhiên dưới dạg quặng hematit.
(c) tan được trong dung dịch axit mạnh và kiềm.
(d) là oxit axit, tác dụng với chỉ tạo ra một axit.
Số phát biểu đúng là
A. 3
B. 2
C. 1
D. 4
Số oxi hóa của crom trong hợp chất Cr2O3 là
A. +4.
B. +2.
C. +3.
D. +6.
Thí nghiệm nào sau đây không có sự hòa tan chất rắn?
A. Cho Al(OH)3 vào dung dịch HNO3
B. Cho Fe vào dung dịch H2SO4 loãng, nóng.
C. Cho NaCl vào H2O.
D. Cho Al vào dung dịch H2SO4 đặc, nguội.
Phương trình hoá học nào sau đây sai?
A. Mg + H2SO4 → MgSO4 + H2
B. Al(OH)3 + 3HCl → AlCl3 + 3H2O
C. Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O
D. Fe3O4 + 4HNO3 → Fe(NO3)2 + 2Fe(NO3)3 + 4H2O
Hòa tan Fe3O4 vào dung dịch HCl dư, thu được dung dịch X. Cho dãy các chất: MnO2, Cl2, KOH, Na2CO3, CuSO4, HNO3, Fe, NaNO3. Số chất trong dãy tác dụng được với dung dịch X là:
A. 6.
B. 5.
C. 4.
D. 7.
Hòa tan hoàn toàn 5,6 gam Fe và 2,4 gam bột kim loại M vào dung dịch HCl, thu được 3,584 lít khí H2 (đktc). Kim loại M là
A. Al.
B. Mg.
C. Zn.
D. Ca.
Cho các phát biểu sau:
(1) Các oxit của kim loại kiềm phản ứng với CO tạo thành kim loại.
(2) Các kim loại Ag, Fe, Cu và Mg đều được điều chế được bằng phương pháp điện phân dung dịch.
(3) Các kim loại Mg, K và Fe đều khử được ion Ag+ trong dung dịch thành Ag.
(4) Cho Cu vào dung dịch FeCl3 dư, thu được dung dịch chứa 3 muối.
Số phát biểu đúng là
A. 4.
B. 1
C. 3.
D. 2.
Kim loại Fe phản ứng với dung dịch X (loãng, dư), tạo muối Fe(III). Dung dịch X là
A. NaNO3, HCl
B. H2SO4, Na2SO4.
C. HCl, H2SO4.
D. CuSO4, Fe2(SO4)3.
Phát biểu nào sau đây sai?
A. Hàm lượng cacbon trong thép ít hơn trong gang.
B. Nhôm là kim loại màu trắng, dẫn nhiệt tốt.
C. Quặng hematit có thành phần chính là Fe2O3.
D. Sắt (III) hiđroxit là chất rắn, màu đỏ, không tan trong nước.
Kim loại nào sau đây phản ứng được với dung dịch FeSO4 và dung dịch H2SO4 đặc, nguội?
A. Na.
B. Al.
C. Fe.
D. Cu.
Cấu hình electron nguyên tử của sắt là
A. [Ar]3d64s2
B. [Ar]3d64s1
C. [Ar]4s23d6
D. [Ar]3d54s1
Nguyên tắc sản xuất gang là
A. khử quặng sắt oxit bằng dòng điện.
B. dùng khí hiđro để khử sắt oxit ở nhiệt độ cao.
C. khử quặng sắt oxit bằng than cốc trong lò cao.
D. dùng nhôm khử sắt oxit ở nhiệt độ cao.
Có thể dùng lượng dư dung dịch của chất nào sau đây để tách Ag ra khỏi hỗn hợp Ag, Fe, Cu mà vẫn giữ nguyên khối lượng Ag ban đầu?
A. Fe(NO3)3.
B. Fe(NO3)3.
C. AgNO3.
D. Cu(NO3)2.
Nhỏ từ từ dung dịch H2SO4 loãng, dư vào dung dịch K2CrO4 thì màu của dung dịch chuyển từ:
A. không màu sang màu da cam.
B. không màu sang màu vàng.
C. màu vàng sang màu da cam.
D. màu da cam sang màu vàng.
Tiến hành các thí nghiệm sau:
(a) Cho lá Fe nguyên chất vào dung dịch CuCl2.
(b) Cho lá Ni nguyên chất vào dung dịch HCl.
(c) Cho lá Zn nguyên chất vào dung dịch FeCl3.
(d) Cho lá Ni nguyên chất vào dung dịch FeCl2.
Số thí nghiệm có thể xảy ra ăn mòn điện hóa là
A. 3.
B. 4.
C. 1.
D. 2.
Cho dung dịch AgNO3 tác dụng với dung dịch chứa chất X thấy tạo kết tủa T màu vàng. Cho kết tủa T tác dụng với dung dịch HNO3 dư thấy kết tủa tan. Chất X là
A. KI.
B. KBr.
C. KCl.
D. K3PO4.
Thực hiện các thí nghiệm sau:
1. Hòa tan hỗn hợp gồm Cu và Fe2O3 (cùng số mol) vào dung dịch HCl loãng dư.
2. Cho KHS vào dung dịch KHSO4 vừa đủ.
3. Cho CrO3 tác dụng với dung dịch NaOH dư.
4. Hòa tan Fe3O4 vào dung dịch H2SO4 loãng dư.
5. Cho hỗn hợp bột gồm Ba và NaHSO4 (tỉ lệ mol tương ứng 1: 2) vào lượng nước dư.
6. Cho 1 mol NaOH vào dung dịch chứa 1 mol Ba(HCO3)2.
7. Cho 1 mol NaHCO3 vào dung dịch chứa 1 mol Ba(OH)2.
Số thí nghiệm luôn thu được hai muối là:
A. 4
B. 5
C. 3
D. 6
Nhiệt phân Fe(NO3)2 trong môi trường khí trơ. Sau khi các phản ứng xảy ra hoàn toàn, thu được sản phẩm gồm:
A. FeO, NO2, O2.
B. Fe2O3, NO2, O2.
C. Fe3O4, NO2, O2.
D. Fe, NO2, O2.
Tiến hành các thí nghiệm sau:
(a) Nhúng thanh Fe vào dung dịch CuSO4.
(b) Dẫn khí co qua Fe2O3 nung nóng.
(c) Điện phân dung dịch NaCl bão hòa, có màng ngăn.
(d) Đốt bột Fe trong khí oxi.
(e) Cho kim loại Ag vào dung dịch HNO3 loãng.
(f) Nung nóng Cu(NO3)2.
(g) Cho Fe3O4 vào dung dịch H2SO4 đặc, nóng.
(h) Nung quặng xiđerit với bột sắt trong bình kín. Số thí nghiệm có xảy ra sự oxi hóa kim loại là:
A. 2
B. 3
C. 5
D. 4
Thực hiện các thí nghiệm sau:
(a) Nhiệt phân AgNO3. (b) Nung FeS2 trong không khí
(c) Cho Mg (dư) vào dung dịch Fe2(SO4)3. (d) Nhiệt phân Mg(NO3)2.
(c) Cho Fe vào dung dịch CuSO4 (dư) (g) Cho Zn vào dung dịch FeCl3 (dư)
(h) Nung Ag2S trong không khí. (i) Cho Ba vào dung dịch CuCl2 (dư)
Sỏ thí nghiệm thu được kim loại sau khi các phản ứng kết thúc là:
A. 4
B. 3
C. 5
D. 2
Tiến hành các thí nghiệm sau:
(a) Nung nóng Fe(NO3)2 đến phản ứng hoàn toàn.
(b) Dẫn khí H2 (dư) qua bột MgO nung nóng.
(c) Cho dung dịch AgNO3 tác dụng với dung dịch Fe(NO3)2 dư.
(d) Cho Na vào dung dịch MgSO4.
(e) Nhiệt phân Hg(NO3)2.
(g) Điện phân dung dịch Cu(NO3)2 với điện cực trơ.
(h) Cho Mg vào dung dịch Fe2(SO4)3 dư. Số thí nghiệm không tạo thành kim loại là:
A. 2
B. 5
C. 3
D. 4
Cho các phản ứng:
Dãy các chất và ion xếp theo chiếu giảm dần tính oxi hoá:
A. Cu2+ > Fe2+ > Cl2 > Fe3+
B. Cl2 > Cu2+ > Fe2+ > Fe3+
C. Fe3+ > Cl2 > Cu2+ > Fe2+
D. Cl2 > Fe3+ > Cu2+ > Fe2+
Cho các chất sau: NaOH, NH3, H2S, Cu, Fe, KI, AgNO3, KMnO4/H2SO4 . Số chất phản ứng được với dung dịch FeCl3 (điều kiện thích hợp) là:
A. 5
B. 6
C. 7
D. 8
Cho 5 phản ứng:
(1) Fe + 2HCl → FeCl2 + H2
(2) 2NaOH + (NH4)2SO4 → Na2SO4 + 2NH3 + 2H2O
(3) BaCl2 + Na2CO3 → BaCO3 + 2NaCl
(4) 2NH3 + 2H2O + FeSO4 → Fe(OH)2 + (NH4)2SO4
(5) NaOH + NaHCO3 → Na2CO3 + H2O
Số phản ứng thuộc loại phản ứng axit - bazơ là
A. 3.
B. 1.
C. 2.
D. 4.
Oxit nào sau đây là oxit axit?
A. CaO.
B. Cr2O3.
C. Na2O.
D. CrO3.
Cho các thí nghiệm sau:
(a). Đốt thanh Cu ngoài không khí.
(b). Nhúng thanh Mg vào dung dịch FeCl2.
(c). Nhúng thanh Fe vào dung dịch hỗn hợp CuCl2 và HCl.
(d). Nhúng thanh Al vào dung dịch H2SO4 loãng có pha thêm vài giọt CuSO4.
Tổng số thí nghiệm có xảy ra quá trình ăn mòn hóa học là?
A. 1
B. 2
C. 3
D. 4