310 câu Lý thuyết Crom - Sắt - Đồng có lời giải chi tiết (P8)
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
Các số oxi hoá đặc trưng của crom là ?
A. +2, +4, +6.
B. +2, +3, +6.
C. +1, +2, +4, +6.
D. +3, +4, +6.
Dẫn luồng khí H2 đến dư qua ống sứ chứa hỗn hợp gồm Al2O3, CuO, MgO, Fe3O4 nung nóng, kết thúc phản ứng lấy phần rắn X trong ống sứ cho vào dung dịch HCl loãng dư, thu được dung dịch Y. Các muối có trong dung dịch Y là.
A. AlCl3, MgCl2, FeCl3, CuCl2
B. MgCl2, AlCl3, FeCl2
C. MgCl2, AlCl3, FeCl2, CuCl2
D. AlCl3, FeCl3, FeCl2, CuCl2
Thực hiện các thí nghiệm sau:
(1) Nhúng thanh Fe vào dung dịch HCl loãng.
(2) Nhúng thanh Fe vào dung dịch FeCl3.
(3) Nhúng thanh Fe vào dung dịch CuCl2.
(4) Nhúng thanh Fe vào dung dịch HCl có lẫn một ít CuCl2.
(5) Nhúng thanh Fe vào dung dịch ZnCl2.
(6) Nhúng thanh Fe vào dung dịch HCl có lẫn một ít MgCl2.
Số thí nghiệm xảy ra ăn mòn điện hóa là.
A. 3
B. 4
C. 2
D. 5
Cho phương trình hóa học:
FeS + HNO3 Fe(NO3)3 + H2SO4 + NO + NO2 + H2O.
Biết tỉ lệ số mol NO và NO2 là 3 : 4. Sau khi cân bằng phương trình hóa học trên với hệ số các chất là những số nguyên tối giản thì hệ số của HNO3 là
A. 76.
B. 63.
C. 102.
D. 39.
Cho các phương trình ion rút gọn sau :
a) Cu2+ + Fe Fe2+ + Cu
b) Cu + 2Fe3+ 2Fe2+ + Cu2+
c) Fe2+ + Mg Mg2+ + Fe
Nhận xét đúng là :
A. Tính khử của : Mg > Fe > Fe2+ > Cu
B. Tính khử của : Mg > Fe2+ > Cu > Fe
C. Tính oxi hóa của : Cu2+ > Fe3+ > Fe2+ > Mg2+
D. Tính oxi hóa của:Fe3+>Cu2+ >Fe2+ >Mg2+
Hợp chất nào sau đây không có tính chất lưỡng tính ?
A. ZnO.
B. Zn(OH)2.
C. ZnSO4.
D. Zn(HCO3)2.
Để loại tạp chất CuSO4 khỏi dung dịch FeSO4 để thu được dung dịch FeSO4 tinh khiết. ta làm như sau :
A. Ngâm lá đồng vào dung dịch.
B. Cho AgNO3 vào dung dịch.
C. Ngâm lá kẽm vào dung dịch.
D. Ngâm lá sắt vào dung dịch.
Chọn phát biểu sai:
A. Cr2O3 là chất rắn màu lục thẫm.
B. Cr(OH)3 là chất rắn màu lục xám.
C. CrO3 là chất rắn màu đỏ thẫm.
D. Na2CrO4 là muối có màu da cam.
Cho các thí nghiệm sau:
(1) Khi cho Cu vào dung dịch FeCl3;
(2) H2S vào dung dịch CuSO4;
(3) HI vào dung dịch FeCl3;
(4) Dung dịch AgNO3 vào dung dịch FeCl3;
(5) Dung dịch NaHSO4 vào dung dịch Fe(NO3)2;
(6) CuS vào dung dịch HCl.
Số cặp chất phản ứng được với nhau là:
A. 2
B. 4
C. 5
D. 3
Thực hiện các thí nghiệm sau:
(1) Nhúng thanh Fe nguyên chất vào dung dịch CuCl2.
(2) Nhúng thanh Fe nguyên chất vào dung dịch FeCl3.
(3) Nhúng thanh Fe nguyên chất vào dung dịch HCl loãng, có nhỏ vài giọt CuCl2.
(4) Cho dung dịch FeCl3 vào dung dịch AgNO3.
(5) Để thanh thép lâu ngày ngoài không khí ẩm.
Số trường hợp xảy ra ăn mòn điện hóa là.
A. 4.
B. 2.
C. 3.
D. 1.
Cho các phát biểu sau:
(a). K2CrO4 có màu da cam, là chất oxi hóa mạnh.
(b). Kim loại Al và Cr đều tan trong dung dịch kiềm đặc.
(c). Kim loại Cr có độ cứng cao nhất trong tất cả các kim loại
(d). Cr2O3 được dùng để tạo màu lục cho đồ sứ, đồ thủy tinh.
(e). Ở trạng thái cơ bản kim loại crom có 6 electron độc thân.
(f). CrO3 là một oxit axit, là chất oxi mạnh, bốc cháy khi tiếp xúc với lưu huỳnh, photpho,…
Số phát biểu đúng là
A. 3
B. 5
C. 4
D. 2
Cho Fe tác dụng với dung dịch HNO3 đặc, nóng thu được khí X có màu nâu đỏ. Khí X là?
A. N2.
B. N2O.
C. NO.
D. NO2.
Trộn bột kim loại X với bột sắt oxit (gọi là hỗn hợp tecmit) để thực hiện phản ứng nhiệt nhôm dùng để hàn đường ray tào hỏa. Kim loại X là?
A. Fe.
B. Cu.
C. Ag.
D. Al.
Trong phòng thí nghiệm khí X được điều chế và thu vào bình tam giác theo hình vẽ bên. Khí X được tạo ra từ phản ứng hóa học nào sau đây?
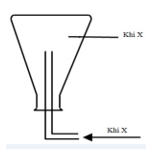
A. 2Fe + 6H2SO4(đặc) Fe2(SO4)3 + 3SO2 + 6H2O.
B. NH4Cl + NaOH NaCl + NH3+ H2O
C. CaCO3 + 2HCl CaCl2 + CO2+ H2O
D. 3Cu + 8HNO3(loãng) 3Cu(NO3)2 + 2NO+ 4H2O
Cho các phát biểu sau:
(1). Dung dịch hỗn hợp FeSO4 và H2SO4 làm mất màu dung dịch KMnO4.
(2). Fe2O3 có trong tự nhiên dưới dạng quặng hematit.
(3). Cr(OH)3 tan được trong dung dịch axit mạnh và kiềm.
(4). CrO3 là oxit axit, tác dụng với H2O chỉ tạo ra một axit.
Số phát biểu đúng là
A. 3.
B. 2.
C. 1.
D. 4.
Cho hỗn hợp Zn, Mg và Ag vào dung dịch CuCl2, sau khi các phản ứng xảy ra hoàn toàn thu được hỗn hợp ba kim loại. Ba kim loại đó là
A. Mg, Cu và Ag
B. Zn, Mg và Ag
C. Zn, Mg và Cu
D. Zn, Ag và Cu
Crom(VI) oxit (CrO3) có màu gì ?
A. Màu vàng.
B. Màu đỏ thẫm.
C. Màu xanh lục.
D. Màu da cam.
Kim loại Fe bị thụ động bởi dung dịch
A. H2SO4 loãng.
B. HCl đặc, nguội.
C. HNO3 đặc, nguội.
D. HCl loãng.
Dung dịch nào sau đây tác dụng được với kim loại Cu?
A. HCl.
B. HNO3 loãng
C. H2SO4 loãng
D. KOH.
Thực hiện các thí nghiệm sau:
(1). Cho Fe3O4 vào dung dịch HCl.
(2). Cho Fe3O4 vào dung dịch HNO3 dư, tạo sản phẩm khử duy nhất là NO.
(3). Sục khí SO2 đến dư vào dung dịch NaOH.
(4). Cho Fe vào dung dịch FeCl3 dư.
(5). Cho hỗn hợp Cu và FeCl3 (tỉ lệ mol 1 : 1) vào H2O dư.
(6). Cho Al vào dung dịch HNO3 loãng (không có khí thoát ra).
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được dung dịch chứa hai muối là
A. 4.
B. 5.
C. 3.
D. 2.
Oxit nào sau đây là oxit axit?
A. CrO3.
B. FeO.
C. Cr2O3.
D. Fe2O3.
Cho dung dịch FeCl3 vào dung dịch chất X, thu được kết tủa Fe(OH)3. Chất X là
A. H2S.
B. AgNO3.
C. NaOH.
D. NaCl.
Tiến hành các thí nghiệm sau:
(a) Cho kim loại Fe vào dung dịch CuCl2.
(b) Cho Fe(NO3)2 tác dụng với dung dịch HCl.
(c) Cho FeCO3 tác dụng với dung dịch H2SO4 loãng.
(d) Cho Fe3O4 tác dụng với dung dịch H2SO4 đặc, nóng, dư.
Số thí nghiệm tạo ra chất khí là
A. 2.
B. 3.
C. 4.
D. 1.
Thí nghiệm nào sau đây xảy ra sự oxi hóa kim loại?
A. Điện phân CaCl2 nóng chảy.
B. Cho kim loại Zn vào dung dịch NaOH.
C. Cho AgNO3 vào dung dịch Fe(NO3)2.
D. Cho Fe3O4 vào dung dịch HI.
Thực hiện các thí nghiệm sau:
(1) Đốt dây kim loại Fe dư trong khí Cl2.
(2) Cho Fe3O4 vào dung dịch HNO3 (loãng, dư).
(3) Đốt nóng hỗn hợp Fe và S (trong chân không).
(4) Cho kim loại Fe vào lượng dư dung dịch HCl.
(5) Cho 1,5a mol Fe tan hết trong dung dịch chứa 5a mol HNO3 (NO là sản phẩm khử duy nhất).
(6) Cho 0,1 mol Fe3O4 vào dung dịch chứa 0,03 mol HNO3 và HCl (dư), (NO là sản phẩm khử duy nhất).
Sau khi các phản ứng xảy ra hoàn toàn, có bao nhiêu thí nghiệm thu được muối sắt(II)?
A. 5.
B. 2.
C. 3.
D. 4.
Hai dung dịch nào sau đây đề tác dụng với kim loại Fe?
A. HCl, CaCl2.
B. CuSO4, ZnCl2.
C. CuSO4, HCl.
D. MgCl2, FeCl3.
Nhiệt phân Fe(OH)2 trong không khí đến khối lượng không đổi, thu được chất rắn là
A. Fe2O3.
B. FeO.
C. Fe(OH)3.
D. Fe3O4.
Dung dịch K2Cr2O7 có màu gì?
A. Màu lục thẫm.
B. Màu vàng.
C. Màu da cam.
D. Màu đỏ thẩm.
Phương trình hóa học nào sau đây Sai?
A. Cr2O3 + 2Al Al2O3 + 2Cr.
B. AlCl3 + 3AgNO3 Al(NO3)3 + 3Ag.
C. Fe2O3 + 8HNO3 2Fe(NO3)3 + 2NO2 + 4H2O.
D. CaCO3 + 2HCl CaCl2 + CO2 + H2O.
Tiến hành các thí nghiệm sau
(1). Cho kim loại Cu vào dung dịch FeCl3 dư.
(2). Điện phân dung dịch AgNO3 (điện cực trơ).
(3). Nung nóng hỗn hợp bột Al và FeO (không có không khí).
(4). Cho kim loại Ba vào dung dịch CuSO4 dư.
(5). Điện phân Al2O3 nóng chảy.
Số thí nghiệm tạo thành kim loại là
A. 5.
B. 4.
C. 2.
D. 3.