Đề kiểm tra giữa học kì 2 Hóa 12 có đáp án (Mới nhất) (Đề 12)
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
D. 18,0.
D. Na2CO3.
D. CaCl2.
D. Fe(OH)3.
D. FeO.
B. Li2SO4.Al2(SO4)3.24H2O.
D. Na2SO4.Al2(SO4)3.24H2O.
Hòa tan hoàn toàn m gam hỗn hợp gồm Ba và BaO vào nước dư, thu được dung dịch X và 1,12 lít khí H2. Dẫn từ từ đến dư khí CO2 vào dung dịch X, sự phụ thuộc của khối lượng kết tủa (y gam) vào thể tích khí CO2 tham gia phản ứng (x lít) được biểu diễn như đồ thị:
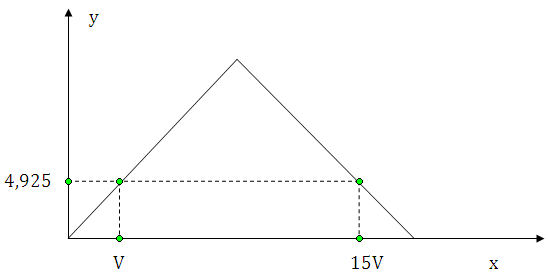
D. 37,45.
D. Nguyên tắc chung để điều chế kim loại là khử ion kim loại thành nguyên tử kim loại.
D. Al.
D. Fe.
D. Al2O3.
D. CaCO3.
Hòa tan 4,7 gam K2O vào 195,3 ml nước. Nồng độ phần trăm của dung dịch thu được là
D. 6,2%.
Kim loại nào sau đây được điều chế bằng phương pháp điện phân nóng chảy?
D. Al.
D. Al.
D. Mg(NO3)2.
D. IIA.
D. Al(OH)3.H2O.
D. 2Al + Fe2O3 2Fe + Al2O3.
A. Nhúng thanh Fe vào dung dịch CuSO4 và H2SO4 loãng.
B. Nhúng thanh Cu vào dung dịch AgNO3.
D. 2.
D. Na.
D. 13,35.
B. Chỉ có sủi bọt khí không màu.
D. 41,67%