Đề thi cuối kì 2 Hóa 12 có đáp án (Đề 1)
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
Phương pháp nhiệt luyện là phương pháp dùng chất khử như CO, C, H2, Al để khử ion kim loại trong
A.oxit kim loại.
B.bazơ.
C. dung dịch muối.
D. hợp kim.
A. dễ nhường 1 electron.
B. dễ nhận thêm 1 electron.
C. dễ nhường 2 electron.
D. dễ nhận thêm 2 electron.
Dung dịch chứa các ion: Mg2+, Ca2+, SO42-thuộc loại nước gì?
A. Nước cứng vĩnh cửu.
B. Nước cứng tạm thời.
C. Nước cứng toàn phần.
D. Nước mềm.
A. Al2O3.
B. Fe2O3.
C. Al.
D. FeO.
A. 1s22s22p63s23p63d64s2.
B. 1s22s22p63s23p63d8.
C. 1s22s22p63s23p63d74s1.
D. 1s22s22p63s23p64s23d6.
A. Fe2O3.
B. FeCO3.
C. FeS2.
D. Fe3O4.
A. Fe.
B. C.
C. Mn.
D. Si.
A. chu kì 4, nhóm VIB.
B. chu 4, nhóm VIIIB.
C. chu kì 3, nhóm VIA.
D. chu kì 3, nhóm VIB.
Hiện tượng Trái Đất nóng lên do hiệu ứng nhà kính chủ yếu do chất nào sau đây?
A. Khí CO2.
B. Khí Cl2.
C. Khí HCl.
D. Khí CO.
Mưa axit chủ yếu là do những chất sinh ra trong quá trình xản xuất công nghiệp nhưng không được xử lý triệt để. Đó là những chất nào sau đây ?
A. SO2và NO2.
B. H2S và Cl2.
C. NH3và HCl.
D. CO2và SO2.
A. CO.
B. CO2.
C. Cl2.
D. NH3.
Người hút thuốc lá nhiều thường mắc các bệnh nguy hiểm về đường hô hấp. Chất gây hại chủ yếu có trong thuốc lá là
A. Nicotin.
B. Morphin.
C. Cocain.
D. Heroin.
A. Ni, Pb, Fe, Ag.
B. Cu, Ni, Fe, Ca.
C. Cu, Ag, Fe, K.
D. Cu, Pb, Hg, Mg.
A. Ca2+ + 2e 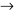 Ca.
Ca.
B. 2Cl- 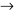 Cl2+ 2e.
Cl2+ 2e.
C. 2Cl- + 2e 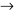 Cl2.
Cl2.
D. Ca2+ 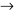 Ca + 2e.
Ca + 2e.
 X + H2O. X là hợp chất
X + H2O. X là hợp chấtA. K2CO3.
B. KOH.
C. Na2CO3.
D. NaCl.
A. CaO.
B. MgCO3.
C. CaCO3.
D. Ca(OH)2.
A. Al(OH)3.
B. Fe(OH)3.
C. Cr(OH)2.
D. Al2O3.
A. S.
B. Cl2.
C. Dung dịch AgNO3 dư.
D. HNO3loãng, dư.
A. Fe2(SO4)3, H2O .
B. FeSO4, Fe2(SO4)3, H2O.
C. FeSO4, H2O .
D. Fe2(SO4)3, SO2và H2O.
Để bảo quản dung dịch Fe2+ người ta thường cho vào dung dịch Fe2+ một lượng
A. Fe dư.
B. Zn dư.
C. Al dư.
D. Ag dư.
A. lưỡng tính.
B. axit.
C. bazo.
D. trung tính.
A. +2, +3, +6.
B. +1, +3, +4, +6.
C. +1, +2, +4,+6.
D. +2, +4, +6.
Để phân biệt CO2 và SO2chỉ cần dùng thuốc thử là
A. nước brom.
B. dung dịch Ba(OH)2.
C. CaO.
D. dung dịch NaOH.
A. Nước vôi trong dư.
B. Etanol dư.
C. Giấm ăn dư.
D. Dung dịch HNO3loãng dư.
A. 3,6 gam.
B. 2,4 gam.
C. 4,8 gam.
D. 7,2 gam.
A. 26,5 gam.
B. 21,2 gam.
C. 31,8 gam.
D. 15,9 gam.
A. 24,030 gam và 6,048 lít.
B. 12,015 gam và 6,048 lít.
C. 24,030 gam và 4,032 lít.
D. 12,015 gam và 4,032 lít.
Cho phương trình hoá học:
a FeO + b H2SO4đặc c Fe2(SO4)3+ d SO2+ e H2O.
c Fe2(SO4)3+ d SO2+ e H2O.
(a, b, c, d, e là các số nguyên, tối giản). Tỉ lệ tối giản của a và b là
A. 1:2.
B. 2:3.
C. 2:4.
D. 1:3.
A. 42,8 gam.
B. 21,4 gam.
C. 32,1 gam.
D. 53,5 gam.
A. 4,56.
B. 9,12.
C. 13,68.
D. 18,24.
A. Cr2O3tan được trong dung dịch HCl và dung dịch NaOH đặc nóng.
B. Nguyên tắc điều chế kim loại là oxi hóa ion kim loại thành nguyên tử.
C. Để điều chế Na, người ta điện phân dung dịch NaCl có màng ngăn.
D. Có thể làm mất tính cứng cứng toàn phần của nước bằng cách đun sôi.
A. Cu + FeCl3(1 : 2).
B. FeO + H2SO4đặc.
C. CO2+ NaOH (1 : 2)
D. Al2O3+ HCl.
A. 24,0 g.
B. 28,8 g.
C. 19,2 g.
D. 25,6 g.
A. 5,40.
B. 2,70.
C. 4,05.
D. 20,4.
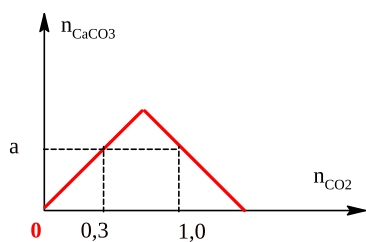
A. 45 gam.
B. 40 gam.
C. 55 gam.
D. 35 gam.
Dùng 5,376 lít khí CO (đktc) có thể khử hoàn toàn 13,92 gam một oxit sắt. Công thức oxit sắt là
A. Fe3O4.
B. Fe2O3.
C. FeO.
Hòa tan hết 12 gam hỗn hợp X gồm Fe và Fe3O4bằng dung dịch chứa 0,1 mol H2SO4và 0,5 mol HNO3, thu được dung dịch Y và hỗn hợp gồm 0,1 mol NO và a mol NO2(không còn sản phẩm khử nào khác). Chia dung dịch Y thành hai phần bằng nhau.
- Phần một tác dụng với 500 ml dung dịch NaOH 0,38M, thu được 6,42 gam một chất kết tủa.
- Phần hai tác dụng với dung dịch Ba(OH)2dư, thu được m gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Giá trị của m gần nhất với
A. 21,28.
B. 20,62.
C. 20,21.
D. 40,42.
Kali đicromat tác dụng với HCl đặc theo phương trình hóa học sau:
K2Cr2O7+ 14HCl → 2KCl + 2CrCl3+ 3Cl2+ 7H2O.
Thể tích khí clo thu được là bao nhiêu lít (đktc) nếu tiến hành khử hết 19,11 gam K2Cr2O7?
A. 4,368 lít.
B. 8,736 lít.
C. 2,912 lít.
D. 5,824 lít.
Trộn 10,17 gam hỗn hợp X gồm Fe(NO3)2và Al với 4,64 gam FeCO3được hỗn hợp Y. Cho Y vào lượng vừa đủ dung dịch chứa 0,56 mol KHSO4được dung dịch Z chứa 83,41 gam muối sunfat trung hòa và m gam hỗn hợp khí T trong đó có chứa 0,01 mol H2. Thêm NaOH vào Z đến khi toàn bộ muối sắt chuyển hết thành hiđroxit và ngừng khí thoát ra thì cần 0,57 mol NaOH, lọc kết tủa nung trong không khí đến khối lượng không đổi thu được 11,5 gam chất rắn. Giá trị m là
A. 3,76.
B. 3,22.
C. 3,46.
D. 3,42.
Cho các phát biểu sau:
(a) Điện phân dung dịch NaCl (điện cực trơ) có màng ngăn, thu được khí H2ở anot.
(b) Cho CO dư qua hỗn hợp Al2O3và CuO đun nóng, thu được Al và Cu.
(c) Hỗn hợp Fe2O3và Cu (tỉ lệ mol tương ứng 1 : 2) tan hoàn toàn trong dung dịch HCl dư.
(d) Kim loại có nhiệt độ nóng chảy thấp nhất là Hg, kim loại dẫn điện tốt nhất là Ag.
(e) Cho dung dịch AgNO3dư vào dung dịch FeCl2, thu được chất rắn chỉ có AgCl.
(f) Trong tự nhiên, các kim loại Na, Ba, K đều tồn tại ở dạng đơn chất.
(g) Khi cho CrO3là một oxit axit, tác dụng với nước chỉ tạo thành 1 loại axit.
Số phát biểu sai là
A. 6.
B. 7.
C. 4.
D. 5.