Đề thi cuối kì 2 Hóa 12 có đáp án (Đề 2)
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
A.N2.
B.H2S.
C.NH3.
D.SO2.
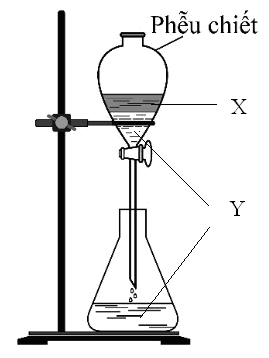
Hai chất X, Y tương ứng là
A.nước và dầu ăn.
B.benzen và nước.
C.axit axetic và nước.
D.benzen và phenol.
A.16,15 gam.
B.15,85 gam.
C.31,70 gam.
D.32,30 gam.
A.metyl axetat.
B.metyl propionat.
C.propyl propionat.
D.propyl fomat.
A.Al.
B.Ag.
C.Au.
D.Fe.
A.(C6H10O5)n.
B.C12H24O12.
C.C12H22O11.
D.C6H12O6.
A.CO2.
B.O2.
C.CO.
D.N2.
Dung dịch Na2CO3tác dụng được với dung dịch
A.NaCl.
B.KCl.
C.NaNO3.
D.CaCl2.
A.HCl.
B.KCl.
C.H2SO4loãng.
D.NaOH.
A.Alanin.
B.Etyl axetat.
C.Anilin.
D.Metylamin.
A.2KNO3 2KNO2+ O2.
2KNO2+ O2.
B.NH4NO2 N2+ 2H2O.
N2+ 2H2O.
C.NH4Cl  NH3+ HCl.
NH3+ HCl.
D.NaHCO3 NaOH + CO2.
NaOH + CO2.
A.H2SO4đặc, nóng.
B.HNO3đặc, nguội.
C.H2SO4loãng.
D.HNO3loãng.
A.Thanh Fe có màu trắng và dung dịch nhạt dần màu xanh.
B.Thanh Fe có trắng xám và dung dịch nhạt dần màu xanh.
C.Thanh Fe có màu đỏ và dung dịch nhạt dần màu xanh.
D.Thanh Fe có màu đỏ và dung dịch dần có màu xanh.
A.4,6.
B.14,4.
C.9,2.
D.27,6.
A.4.
B.2.
C.1.
D.3.
A.Tơ axetat.
B.Tơ nitron.
C.Tơ tằm.
D.Sợi bông.
A.4P + 5O2 2P2O5.
2P2O5.
B.2P + 5Cl2 2PCl5.
2PCl5.
C.P + 5HNO3→ H3PO4+ 5NO2+ H2O.
D.3Ca + 2P  Ca3P2.
Ca3P2.
A.29,70.
B.25,46.
C.33,00.
D.26,73.
A.glucozơ, bạc.
B.glucozơ, amoni gluconat.
C.fructozơ, amoni gluconat.
D.glucozơ, axit gluconic.
A.Hoa nhài.
B.Chuối chín.
C.Hoa hồng.
D.Dứa chín.
A.C2H5COOC2H5.
B.CH3COOC2H5.
C.CH3COOCH3.
D.C2H5COOCH3.
A.1454.
B.1544.
C.1640.
D.1460.
A.K3PO4.
B.HNO3.
C.KBr.
D.HCl.
Trong các ion sau đây, ion nào có tính oxi hóa mạnh nhất?
A.Ca2+.
B.Ni2+.
C.Cu2+.
D.Fe2+.
(a) Điện phân dung dịch NaCl (điện cực trơ, màng ngăn xốp).
(b) Cho FeO vào dung dịch HNO3loãng, dư, đun nóng.
(c) Cho Si vào dung dịch NaOH dư.
(d) Cho dung dịch NaHSO4vào dung dịch NaHCO3.
(e) Cho dung dịch Fe(NO3)2vào dung dịch H2SO4loãng.
(g) Cho đinh sắt vào dung dịch H2SO4đặc, nóng (dư).
Sau khi các phản ứng xảy ra, số thí nghiệm sinh ra chất khí là
A.2.
B.4.
C.6.
D.5.
Cho các sơ đồ phản ứng sau:
Phát biểu nào sau đây đúng?
A.Nhiệt độ nóng chảy của X1cao hơn X3.
B.Dung dịch X4có thể làm quỳ tím chuyển màu hồng.
C.Nhiệt độ sôi của X2cao hơn axit axetic.
D.Các chất X2, X3và X4đều có mạch cacbon phân nhánh.
A.6,0.
B.6,4.
C.5,4.
D.6,2.
A.5,28.
B.5,96.
C.5,08.
D.4,96.
A.11,60 gam.
B.27,84 gam.
C.18,56 gam.
D.23,20 gam.
(1) Cho Mg vào dung dịch Fe2(SO4)3dư.
(2) Cho bột Zn vào lượng dư dung dịch HCl.
(3) Dẫn khí H2dư qua ống sứ chứa bột CuO nung nóng.
(4) Cho Ba vào lượng dư dung dịch CuSO4.
(5) Cho dung dịch Fe(NO3)2vào dung dịch AgNO3.
Sau khi kết thúc các phản ứng, số thí nghiệm thu được kim loại là
A.4.
B.2.
C.3.
D.1.
(a) Thủy phân saccarozơ trong môi trường kiềm thu được glucozơ và fructozơ.
(b) Muối phenylamoni clorua không tan trong nước.
(c) Trong phân tử peptit mạch hở Gly-Ala-Gly có 4 nguyên tử oxi.
(d) Lực bazơ của metylamin lớn hơn của amoniac.
(e) Bản chất của quá trình lưu hóa cao su là tạo ra cầu nối  giữa các mạch cao su không phân nhánh tạo thành mạch phân nhánh.
giữa các mạch cao su không phân nhánh tạo thành mạch phân nhánh.
Số phát biểu đúng là
A.5.
B.4.
C.2.
D.3.
A.a
B.a >2b.
C.b
D.a = b.
A.60.
B.24.
C.48.
D.30.
A.110,8.
B.98,5.
C.107,6.
D.115,2.
A.CH3COOC2H5.
B.C2H3COOCH3.
C.C2H5COOCH3.
D.CH3COOCH3.
A.56,18.
B.37,45.
C.17,72.
D.47,95.
- Hai dung dịch X và Y tác dụng được với FeSO4.
- Dung dịch Z có pH thấp nhất trong 4 dung dịch.
- Hai dung dịch Y và T phản ứng được với nhau.
Các dung dịch X, Y, Z, T lần lượt là:
A.HNO3, NaOH, HCl, H2SO4.
B.NaOH, HNO3, H2SO4, HCl.
C.HNO3, NaOH, H2SO4, HCl.
D.HCl, NaOH, H2SO4, HNO3.
A.4.
B.5.
C.3.
D.6.
A.19,82.
B.17,50.
C.22,94.
D.12,98.
A.26,28%.
B.17,65%.
C.28,36%.
D.29,41%.