Đề thi cuối kì 2 Hóa 12 có đáp án (Đề 9)
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
A. HCl.
B. NaOH.
C. CO2.
D. KOH.
A. 7,6.
B. 10,2.
C. 15
D. 11,4.
A. 6,42
B. 1,07
C. 3,21
D. 2,14
Chất không có tính chất lưỡng tính là
A. Al2O3
B. AlCl3
C. Al(OH)3
A. 40,5 g
B. 27 g
C. 12,5 g
D. 45 g
A. NaCl và Ca(OH)2
B. Na2CO3và Na3PO4
C. Na2CO3và Ca(OH)2.
D. Na2CO3và HCl.
A. Tính chất hóa học đặc trưng của kim loại là tính khử.
B. Ăn mòn hóa học phát sinh dòng điện.
C. Bản chất của ăn mòn kim loại là quá trình oxi hóa - khử.
D. Nguyên tắc chung để điều chế kim loại là khử ion kim loại thành nguyên tử kim loại.
A. 27g
B. 28g
C. 29g.
D. 30g
A. 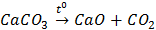 CaCO3
CaCO3  CaO + CO2
CaO + CO2
B. 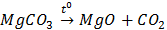 MgCO3
MgCO3 MgO + CO2
MgO + CO2
C.2NaHCO3 Na2CO3+ CO2+ H2O
Na2CO3+ CO2+ H2O
D.Na2CO3 Na2O + CO2
Na2O + CO2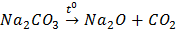
A. 0,112.
B. 0,224.
C. 0,448.
D. 0,896.
A. Fe
B. Cu
C. Mg
D. Al
A. 3
B. 1
C. 2
D. 4
A. Có kết tủa trắng sau đó tan.
B. Có kết tủa trắng
C. Không có kết tủa.
D. Không hiện tượng
A. 100 ml
B. 250 ml
C. 150 ml
D. 200 ml
A. da cam
B. đỏ
C. vàng
D. xanh
Dung dịch chứa muối X không làm đổi màu quỳ tím, dung dịch chứa muối Y làm quỳ tím hóa xanh. Trộn hai dung dịch trên với nhau thấy tạo kết tủa. Vậy X và Y có thể là cặp chất nào trong các cặp chất dưới đây
A. KNO3và Na2CO3
B. Na2SO4và BaCl2
C. Ba(NO3)2và Na2CO3
A. 0,032
B. 0.048
C. 0,06
D. 0,04
A. SO2và NO2.
B. NH3và HCl.
C. H2S và N2.
D. CO2và O2.
A. 2,24 hoặc 11,2 lít
B. 11,2 lít
C. 2,24 lít
D. 2,24 hoặc 3,36 lít
A. kim loại Ba.
B. kim loại Mg.
C. kim loại Ag.
D. kim loại Cu.
A. H2SO4loãng.
B. HNO3loãng.
C. NaCl loãng.
D. NaOH loãng
A. 10,0 g
B. 15,0 g
C. 20,0 g
D. 30,0 g
A. 27,84g.
B. 13,32g.
C. 13,92g.
D. 8,88g.
A. Cùng tác dụng với HCl tạo ra muối có mức oxi hóa là +3.
B. Cùng tác dụng với dung dịch NaOH dư.
C. Cùng tác dụng với khí clo tạo ra muối có dạng MCl3.
D. Cùng bị thụ động trong HNO3đặc nguội.
A. Mg.
B. Na.
C. Ca.
D. K.
A. 0,015 lít
B. 0,01 lít
C. 0,03 lít
D. 0,02 lít
A. Sr
B. Be
C. Ca
D. Mg
D. ZnSO4
A. Al2O3
B. Al(OH)3
C. NaHCO3
A. NaCl.
B. Ca(OH)2.
C. HCl.
D. KOH.
Cho phản ứng hoá học : Fe + CuSO4FeSO4+ Cu. Trong phản ứng trên xảy ra
A. sự oxi hoá Fe và sự khử Cu2+
B. sự oxi hoá Fe và sự oxi hoá Cu
C. sự khử Fe2+và sự oxi hoá Cu
A. Cs
B. Na
C. K.
D. Li
A. 50 ml.
B. 90 ml.
C. 75 ml.
D. 57 ml.