ĐGNL ĐH Bách khoa - Vấn đề thuộc lĩnh vực hóa học - Chromium và hợp chất của chromium
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
Dãy bao gồm các ion sắp xếp theo chiều giảm dần tính oxi hóa là
A. Ag+, Cu2+, Fe3+, Fe2+.
B. Fe3+, Cu2+, Ag+, Fe2+.
C. Ag+, Fe3+, Cu2+, Fe2+.
D. Fe3+, Ag+, Cu2+, Fe2+.
Có thể đựng axit nào sau đây trong bình sắt ?
A. HCl loãng.
B. H2SO4 loãng.
C. HNO3 đặc nguội.
D. HNO3 đặc nóng.
Đốt một lượng dư sắt trong khí clo thu được hỗn hợp gồm 2 chất rắn. Thành phần chất rắn đó gồm
A. FeCl2 và FeCl3.
B. FeCl3 và Fe.
C. FeCl2 và Fe.
D. đáp án khác.
Kim loại Fe không phản ứng với chất nào sau đây trong dung dịch
A. FeCl3.
B. CuSO4.
C. AgNO3.
D. MgCl2.
Kim loại sắt tác dụng với dung dịch nào sau đây tạo muối sắt (II)
A. HNO3 đặc, nóng, dư.
B. CuSO4.
C. H2SO4 đặc, nóng, dư
D. MgSO4.
Để bảo quản dung dịch FeSO4 trong phòng thí nghiệm, người ta cần thêm vào bình chất nào dưới đây
A. Một đinh Fe sạch.
B. Dung dịch H2SO4 loãng.
C. Một dây Cu sạch.
D. Dung dịch H2SO4 đặc.
Cho từ từ đến dư kim loại Na vào dung dịch có chứa muối FeCl3. Số phản ứng xảy ra là:
A. 4
B. 2
C. 3
D. 5
Ngâm thanh Cu (dư) vào dung dịch AgNO3 thu được dung dịch X. Sau đó ngâm thanh Fe (dư) vào dung dịch X thu được dung dịch Y. Biết các phản ứng xảy ra hoàn toàn. Dung dịch Y có chứa chất tan là:
A. Fe(NO3)3.
B. Fe(NO3)2.
C. Fe(NO3)2, Cu(NO3)2
D. Fe(NO3)3, Fe(NO3)2.
Cho hỗn hợp X gồm Fe, Cu vào dung dịch HNO3 loãng, nóng thu được khí NO là sản phẩm khử duy nhất, dung dịch Y và còn lại chất rắn chưa tan Z. Cho Z tác dụng với dung dịch H2SO4 loãng thấy có khí thoát ra. Thành phần chất tan trong dung dịch Y là:
A. Fe(NO3)3 và Cu(NO3)2.
B. Fe(NO3)2 và Cu(NO3)2.
C. Fe(NO3)2.
D. Fe(NO3)3 và Fe(NO3)2.
Có 4 dung dịch đựng riêng biệt: (a) HCl; (b) CuCl2; (c) FeCl2; (d) HCl có lẫn CuCl2. Nhúng vào mỗi dung dịch một thanh sắt nguyên chất. Số trường hợp xảy ra ăn mòn điện hóa là
A. 0
B. 1
C. 3
D. 2
Để điều chế Fe trong công nghiệp, người ta có thể dùng phương pháp nào sau đây:
A. Mg + FeCl2 →
B. Fe2O3 + Al
C. Điện phân dung dịch FeCl2
D. Fe2O3 + CO →
Phản ứng của Fe với O2 như hình vẽ
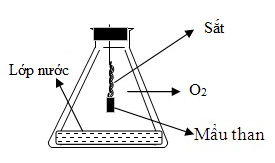
Cho các phát biểu sau đây:
(a) Vai trò của mẩu than để làm mồi cung cấp nhiệt cho phản ứng.
(b) Phản ứng tỏa nhiều nhiệt làm đầu dây sắt nóng chảy có thể thành cục tròn.
(c) Vai trò của lớp nước ở đáy bình là để tránh vỡ bình.
(d) Phản ứng cháy sáng, có các tia lửa bắn ra từ dây sắt.
Số phát biểu sai là
A. 2.
B. 0.
C. 1.
D. 3.
Những nhận định sau về kim loại sắt:
(1) Kim loại sắt có tính khử trung bình.
(2) Ion Fe2+ bền hơn Fe3+.
(3) Fe bị thụ động trong H2SO4 đặc nguội.
(4) Quặng manhetit là quặng có hàm lượng sắt cao nhất.
(5) Trái đất tự quay và sắt là nguyên nhân làm Trái Đất có từ tính.
(6) Kim loại sắt có thể khử được ion Fe3+.
Số nhận định đúng là
A. 3
B. 4
C. 5
D. 6
Kim loại sắt phản ứng với lượng dư dung dịch chất nào sau đây tạo ra muối sắt(II)?
A. H2SO4 đặc, nóng.
B. HNO3 loãng.
C. H2SO4 loãng.
D. HNO3 đặc nóng.
Dung dịch X có chứa FeSO4, dung dịch Y có chứa Fe2(SO4)3. Thuốc thử nào sau đây có thể sử dụng để phân biệt X và Y là
A. dung dịch NH3.
B.dung dịch KMnO4 trong H2SO4.
C. kim loại Cu
D. tất cả các đáp án trên.
Phát biểu nào sau đây không đúng ?
A. Kim loại Fe phản ứng với dung dịch HCl tạo ra muối sắt (II).
B. Dung dịch FeCl3 phản ứng được với kim loại Fe.
C. Kim loại Fe không tan trong dung dịch H2SO4 đặc nguội.
D. Trong các phản ứng hóa học, ion Fe2+ chỉ thể hiện tính khử.
Hòa tan chất rắn X vào dung dịch H2SO4 loãng dư thu được dung dịch Y. Dung dịch Y hòa tan được Cu và làm mất màu dung dịch KMnO4. X là
A. Fe3O4.
B. FeO.
C. Fe.
D. Fe2O3.
Hợp chất mà sắt vừa có tính oxi hóa, vừa có tính khử là
A. Fe(OH)3.
B. Fe2O3.
C. FeCl2.
D. FeCl3.
Cho các phản ứng sau:
1) dung dịch FeCl2 + dung dịch AgNO3
2) dung dịch FeSO4 dư + Zn
3) dung dịch FeSO4 + dung dịch KMnO4 + H2SO4
4) dung dịch FeSO4 + khí Cl2
Số phản ứng mà ion Fe2+ bị oxi hóa là
A. 2
B. 1
C. 4
D. 3
Cho các sơ đồ phản ứng hoá học sau đây, có bao nhiêu sơ đồ sai ?
(1) Fe3O4 + HCl → FeCl2 + FeCl3 + H2O
(2) Fe(OH)3 + H2SO4 đặc nóng → Fe2(SO4)3 + SO2 + H2O
(3) FeO + HNO3 → Fe(NO3)3 + NO + H2O
(4) FeCl2 + HNO3 → Fe(NO3)3 + HCl + NO + H2O
(5) Al + HNO3 → Al(NO3)3 + H2
(6) FeO + H2SO4 đặc nguội → Fe2(SO4)3 + SO2 + H2O
A. 1
B. 2
C. 3
D. 4
Chất nào sau đây tác dụng hoàn toàn với dung dịch HCl dư chỉ thu được muối Fe3+?
A. FeCO3.
B. Fe2O3.
C. Fe3O4.
D. Fe(OH)2.
Thực hiện các thí nghiệm sau:
(a) Cho bột Mg dư vào dung dịch FeCl3.
(b) Đốt Fe trong khí Cl2 dư.
(c) Cho bột Fe3O4 vào dung dịch H2SO4 đặc, nóng, dư.
(d) Cho bột Fe vào dung dịch AgNO3 dư.
(e) Cho bột Fe dư vào dung dịch HNO3 loãng.
(g) Cho bột FeO vào dung dịch KHSO4.
Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được muối sắt (II) là:
A. 5
B. 2
C. 4
D. 3
Trong quá trình bảo quản, một chiếc đinh sắt nguyên chất đã bị oxi hóa bởi oxi không khí tạo thành hỗn hợp X gồm Fe, Fe2O3, Fe3O4 và FeO. Hỗn hợp X không bị hòa tan hoàn toàn trong lượng dư dung dịch chất nào sau đây?
A. AgNO3.
B. HCl.
C. HNO3 đặc, nóng.
D. H2SO4 đặc, nóng.
Một mol hợp chất nào sau đây khi phản ứng với dung dịch HNO3 đặc nóng, dư tạo nhiều mol khí nhất?
A. FeO.
B. FeS.
C. FeCO3.
D. Fe3O4.
Hòa tan hoàn toàn x mol Fe vào dung dịch chứa y mol FeCl3 và z mol HCl, thu được dung dịch chỉ chứa một chất tan duy nhất. Biểu thức liên hệ giữa x, y và z là:
A. y = 2x.
B. 2x = y + z.
C. 2x = y + 2z.
D. x = y – 2z.
Cho các phản ứng chuyển hóa sau: NaOH + dung dịch X → Fe(OH)2; Fe(OH)2 + dung dịch Y → Fe2(SO4)3; Fe2(SO4)3 + dung dịch Z → BaSO4. Các dung dịch X, Y, Z lần lượt là
A. FeCl3, H2SO4 đặc nóng, Ba(NO3)2.
B. FeCl3, H2SO4 đặc nóng, BaCl2.
C. FeCl2, H2SO4 đặc nóng, BaCl2.
D. FeCl2, H2SO4 loãng, Ba(NO3)2.
Để điều chế Fe(OH)2 trong phòng thí nghiệm, người ta tiến hành như sau: Đun sôi dung dịch NaOH sau đó cho nhanh dung dịch FeCl2 vào dung dịch NaOH này. Mục đích chính của việc đun sôi dung dịch NaOH là?
A. Phân hủy hết muối cacbonat, tránh việc tạo kết tủa FeCO3.
B. Đẩy hết oxi hòa tan, tránh việc oxi hòa tan oxi hóa Fe(II) lên Fe(III).
C. Để nước khử Fe(III) thành Fe(II).
D. Đẩy nhanh tốc độ phản ứng.
Cho sơ đồ chuyển hóa sau:
Cho các chất: NaCl, KOH, AgNO3, Cu(OH)2. Có bao nhiêu chất có thể thỏa mãn Z trong sơ đồ trên?
A. 1
B. 2
C. 3
D. 4
Có bao nhiêu chất thỏa mãn sơ đồ: X + HNO3 → Fe(NO3)3 + NO + H2O ?
A. 3
B. 4
C. 5
D. 6
Bằng phương pháp hóa học. Hãy chọn một hóa chất thích hợp để nhận biết các chất rắn (dạng bột) sau: Fe, FeO, Fe3O4, CuO.
A. dung dịch HCl
B. dung dịch HNO3 đặc, nóng
C. dung dịch AgNO3
D. dung dịch NaOH
Nhận biết lọ đựng Fe và Fe2O3 bằng phương pháp hóa học trong 3 lọ hóa chất đựng hỗn hợp các chất rắn sau Fe và FeO; Fe và Fe2O3; FeO và Fe2O3 chỉ cần dùng loại thuốc thử nào dưới đây
A. dd HCl
B. dd H2SO4 loãng
C. dd HNO3 đặc nguội
D. Tất cả các phương án đều đúng