ĐGNL ĐH Bách khoa - Vấn đề thuộc lĩnh vực hóa học - Tốc độ phản ứng hóa học
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
Yếu tố nào sau đây không ảnh hưởng đến tốc độ của phản ứng sau:
CaCO3 (r) + 2HCl(dd) → CaCl2 + H2O + CO2 ↑
A. Nhiệt độ.
B. Chất xúc tác.
C. Áp suất.
D. Diện tích tiếp xúc.
Nội dung nào thể hiện trong các câu sau đây là sai ?
A. Thực phẩm bảo quản ở nhiệt độ thấp hơn sẽ giữ được lâu hơn.
B. Nấu thực phẩm trong nồi áp suất nhanh chín hơn so với khi nấu chúng ở áp suất thường.
C. Than cháy trong oxi nguyên chất nhanh hơn khi cháy trong không khí.
D. Nhiên liệu cháy ở tầng khí quyển trên cao nhanh hơn khi cháy ở mặt đất.
Cho 5 gam kẽm viên vào cốc đựng 50 ml dung dịch H2SO4 4M ở nhiệt độ thường (25oC). Trường hợp nào tốc độ phản ứng không đổi ?
A. Thay 5 gam kẽm viên bằng 5 gam kẽm bột
B. Thay dung dịch H2SO4 4M bằng dung dịch H2SO4 2M
C. Tăng nhiệt độ phản ứng từ 25oC đến 500 C
D. Dùng thể tích dung dịch H2SO4 gấp đôi ban đầu
Hai nhóm học sinh làm thí nghiệm nghiên cứu tốc độ phản ứng kẽm với dung dịch axit clohiđric:
• Nhóm thứ nhất: Cân 1 gam kẽm miếng và thả vào cốc đựng 200 ml dung dịch axit HCl 2M
• Nhóm thứ hai: Cân 1 gam kẽm bột và thả vào cốc đựng 300 ml dung dịch axit HCl 2M
Kết quả cho thấy bọt khí thoát ra ở thí nghiệm của nhóm thứ hai mạnh hơn là do:
A. Nhóm thứ hai dùng axit nhiều hơn.
B. Diện tích bề mặt kẽm bột lớn hơn kẽm miếng.
C. Nồng độ kẽm bột lớn hơn.
D. Cả ba nguyên nhân đều sai.
Có hai cốc chứa dung dịch Na2SO3, trong đó cốc A có nồng độ lớn hơn cốc B. Thêm nhanh cùng một lượng dung dịch H2SO4 cùng nồng độ vào hai cốc. Hiện tượng quan sát được trong thí nghiệm trên là
A. cốc A xuất hiện kết tủa vàng nhạt, cốc B không thấy kết tủa.
B. cốc A xuất hiện kết tủa nhanh hơn cốc B.
C. cốc A xuất hiện kết tủa chậm hơn cốc B.
D. cốc A và cốc B xuất hiện kết tủa với tốc độ như nhau.
Khi đốt củi, để tăng tốc độ cháy, người ta sử dụng biện pháp nào sau đây?
A. đốt trong lò kín.
B. xếp củi chặt khít.
C. thổi hơi nước.
D. thổi không khí khô
Người ta sử dụng các biện pháp sau để tăng tốc độ phản ứng:
(1) Dùng khí nén, nóng thổi vào lò cao để đốt cháy than cốc (trong sản xuất gang).
(2) Nung đá vôi ở nhiệt độ cao để sản xuất vôi sống.
(3) Nghiền nguyên liệu trước khi nung để sản xuất clanhke.
(4) Cho bột sắt làm xúc tác trong quá trình sản xuất NH3 từ N2 và H2.
Trong các biện pháp trên, có bao nhiêu biện pháp đúng?
A. 1
B. 2
C. 3
D. 4
Người ta đã sử dụng nhiệt độ của phản ứng đốt cháy than đá để nung vôi, biện pháp kỹ thuật nào sau đây không được sử dụng để tăng tốc độ phản ứng nung vôi?
A. Đập nhỏ đá vôi với kích thước khoảng 10cm.
B. Tăng nhiệt độ phản ứng lên khoảng 9000 C.
C. Tăng nồng độ khí cacbonic.
D. Thổi không khí nén vào lò nung vôi.
Phương pháp nào sau đây làm giảm tốc độ phản ứng?
A. Nấu thực phẩm trong nồi áp suất
B. Đưa lưu huỳnh đang cháy ngoài không khí vào oxi
C. Dùng không khí nén thổi vào lò cao để đốt than cốc (sản xuất gang)
D. Đậy nắp bếp lò than đang cháy.
Chất xúc tác trong phản ứng hóa học có tác dụng làm tăng tốc độ phản ứng, sau khi phản ứng sau chất xúc tác sẽ:
A. Phản ứng hết vừa đủ
B. Phản ứng nhưng vẫn còn dư
C. Phản ứng hết nhưng vẫn còn thiếu so với chất phản ứng
D. Không thay đổi
Cho ba mẫu đá vôi (100% CaCO3) có cùng khối lượng: mẫu 1 dạng bột mịn, mẫu 2 dạng viên nhỏ, mẫu 3 dạng khối vào ba cốc đựng cùng thể tích dung dịch HCl (dư, cùng nồng độ, ở điều kiện thường). Thời gian để đá vôi tan hết trong ba cốc tương ứng là t1, t2, t3 giây. So sánh nào sau đây đúng?
A. t1 = t2 = t3
B. t1 < t2 < t3
C. t3 < t2 < t1
D. t2 < t1 < t3
Cho phản ứng hóa học sau:
Có bao nhiêu yếu tố ảnh hưởng đến tốc độ phản ứng trên trong số các yếu tố sau: nhiệt độ, nồng độ, áp suất, diện tích tiếp xúc, chất xúc tác.
A. 5.
B. 2
C. 4
D. 3
Người ta nghiền nguyên liệu trước khi đưa vào lò nung để sản xuất clanhke (trong quá trình sản xuất xi măng) là đã tăng yếu tố nào sau đây để tăng tốc độ của phản ứng?
A. Áp suất.
B. Nhiệt độ.
C. Diện tích bề mặt chất phản ứng.
D. Nồng độ.
Yếu tố nào sau đây không ảnh hưởng đến tốc độ phản ứng sau:
A. Nhiệt độ
B. Chất xúc tác
C. Áp suất
D. Kích thước của các tinh thể KClO3
Cho phản ứng:
Na2S2O3 (l) + H2SO4 (l) → Na2SO4 (l) + SO2 (k) + S (r) + H2O (l).
Khi thay đổi một trong các yếu tố: (1) tăng nhiệt độ; (2) tăng nồng độ Na2S2O3; (3) giảm nồng độ H2SO4; (4) giảm nồng độ Na2SO4; (5) giảm áp suất của SO2; (6) dùng chất xúc tác. Có bao nhiêu yếu tố làm tăng tốc độ của phản ứng đã cho?
A. 4
B. 3
C. 2
D. 5
Có hai mẫu đá vôi:
Mẫu 1: đá vôi có dạng khối.
Mẫu 2: đá vôi có dạng hạt nhỏ.
Hòa tan cả hai mẫu đá vôi bằng cùng một thể tích dung dịch HCl dư có cùng nồng độ. Ta thấy thời gian để mẫu 1 phản ứng hết nhiều hơn mẫu 2. Thí nghiệm trên chứng minh điều gì?
A. Tốc độ phản ứng phụ thuộc vào nhiệt độ tiến hành phản ứng.
B.Tốc độ phản ứng phụ thuộc vào diện tích tiếp xúc giữa các chất phản ứng.
C. Tốc độ phản ứng phụ thuộc vào thời gian xảy ra phản ứng.
D. Tốc độ phản ứng không phụ thuộc vào nồng độ các chất tham gia phản ứng.
Đồ thị dưới đây biểu diễn sự phụ thuộc của tốc độ phản ứng vào nồng độ chất phản ứng.
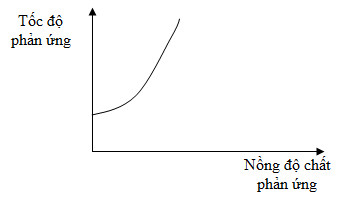
Từ đồ thị trên, ta thấy tốc độ phản ứng
A. Giảm khi nồng độ của chất phản ứng tăng.
B. Không phụ thuộc vào nồng độ của chất phản ứng.
C. Tỉ lệ thuận với nồng độ của chất phản ứng.
D. Tỉ lệ nghịch với nồng độ của chất phản ứng.
Cho phản ứng:
X → Y
Tại thời điểm t1 nồng độ của chất X bằng C1, tại thời điểm t2 (với t2>t1), nồng độ của chất X bằng C2. Tốc độ trung bình của phản ứng trong khoảng thời gian trên được tính theo biểu thức nào sau đây ?
A. 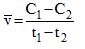
B. 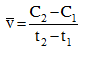
C. 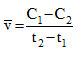
D. 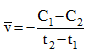
Cho phản ứng hóa học sau :
Yếu tố nào sau đây không ảnh hưởng đến tốc độ của phản ứng trên ?
A. Áp suất.
B. Nồng độ H2O2.
C. Chất xúc tác.
D. Nhiệt độ.
Cho phản ứng: 2NO + O2 → 2NO2 xảy ra trong bình kín. Biết nhiệt độ của hệ không đổi. Tốc độ của phản ứng tăng hay giảm bao nhiêu lần khi áp suất của NO tăng 3 lần ?
A. Tăng lên 9 lần.
B. Giảm đi 9 lần.
C. Tăng lên 18 lần.
D. Giảm đi 18 lần.
Cho chất xúc tác MnO2 vào 100 ml dung dịch H2O2, sau 60 giây thu được 33,6 ml khí O2 (ở đktc). Tốc độ trung bình của phản ứng (tính theo H2O2) trong 60 giây là
A. 5.10-2 mol/(L.s)
B. 5.10-3 mol/(L.s)
C. 5.10-4 mol/(L.s)
D. 5.10-5 mol/(L.s)
Cho phản ứng: 2SO2 + O2 ⇆ 2SO3. Biết thể tích bình phản ứng không đổi. Tốc độ phản ứng tăng lên 4 lần khi
A. tăng nồng độ SO2 lên 2 lần.
B. tăng nồng độ SO2 lên 4 lần.
C. tăng nồng độ O2 lên 2 lần.
D. tăng đồng thời nồng độ SO2 và O2 lên 2 lần.
A2 + 2B → 2AB
Tốc độ của phản ứng thay đổi như thế nào khi áp suất của A2 tăng lên 6 lần?
A. Tăng lên 6 lần.
B. Giảm đi 6 lần.
C. Tăng lên 36 lần.
D. Giảm đi 36 lần.
Cho phương trình hóa học của phản ứng:
X + 2Y → Z + T.
Ở thời điểm ban đầu, nồng độ của chất X là 0,01 mol/L. Sau 20 giây, nồng độ của chất X là 0,008 mol/L. Tốc độ trung bình của phản ứng tính theo chất X trong khoảng thời gian trên là
A. 10-2.
B. 10-3.
C. 10-4.
D. 10-5.
A. 2
B. 3
C. 4
D. 5
A. 1552.
B. 730.
C. 820.
D. 560.
A. 40oC
B. 50oC
C. 60oC
D. 70oC
A. 4,25.10-3mol/(l.s) và 0,0544 g.
B. 2,125.10-3mol/(l.s) và 0,1088 g.
C. 4,25.10-3mol/(l.s) và 0,1088 g.
D. 2,125.10-3mol/(l.s) và 0,0544 g.
Cho chất xúc tác MnO2 vào 100 ml dung dịch H2O2, sau 60 giây thu được 3,36 ml khí O2 (ở đktc). Tốc độ trung bình của phản ứng (tính theo H2O2) trong 60 giây trên là
A. 2,5.10-4 mol/(l.s)
B. 5,0.10-4 mol/(l.s)
C. 1,0.10-3 mol/(l.s)
D. 5,0.10-5 mol/(l.s)
Thực hiện phản ứng sau trong bình kín:
H2 (k) + Br2 (k) → 2HBr (k).
Lúc đầu nồng độ hơi Br2 là 0,072 mol/l. Sau 2 phút, nồng độ hơi Br2 còn lại là 0,048 mol/l. Tốc độ
trung bình của phản ứng tính theo Br2 trong khoảng thời gian trên là
A. 8.10-4 mol/(l.s).
B. 2.10-4 mol/(l.s).
C. 6.10-4 mol/(l.s).
D. 4.10-4mol/(l.s).