Giải Hóa Học 11 (Cánh Diều) Bài 1: Mở đầu về cân bằng hoá học
Sinx.edu.vn xin giới thiệu giải bài tập Hóa Học lớp 11 Bài 1: Mở đầu về cân bằng hoá học sách Cánh Diều hay nhất, chi tiết giúp học sinh so sánh và làm bài tập Hóa Học 11 Bài 1 dễ dàng. Mời các bạn đón xem:
Nội dung bài viết
Xem thêm »
Giải bài tập Hóa học lớp 11 Bài 1: Mở đầu về cân bằng hoá học
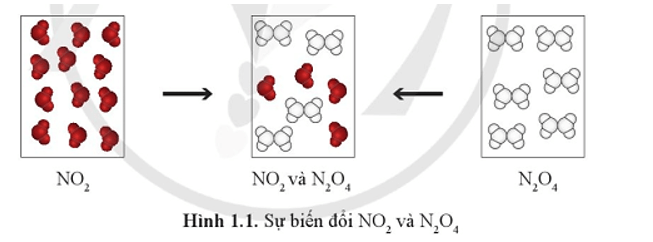
Mở đầu trang 6 Hoá học 11: Khí NO2 (màu nâu đỏ) liên tục chuyển thành khí N2O4 (không màu) và ngược lại, tại một điều kiện xác định. Cũng tại điều kiện này, bình khí NO2 hay bình khí N2O4 (Hình 1.1), sau những khoảng thời gian xác định đều chuyển thành hỗn hợp khí có thành phần như nhau và không đổi theo thời gian.
Lời giải:
Tại thời điểm hỗn hợp khí trong hai bình có thành phần như nhau, phản ứng vẫn tiếp diễn trong hai bình.
Tuy nhiên, nồng độ của một chất bất kì trong phản ứng không đổi là do lượng mất đi và lượng sinh ra chất đó là bằng nhau.
I. Khái niệm phản ứng thuận nghịch và trạng thái cân bằng
Câu hỏi 1 trang 7 Hoá học 11: Hãy nêu một số ví dụ về phản ứng thuận nghịch mà em biết.
Lời giải:
Một số ví dụ về phản ứng thuận nghịch:
+ Phản ứng của khí chlorine với nước:
Cl2(aq) + H2O(l) ⇌ HCl(aq) + HClO(aq).
+ Phản ứng hình thành hang động, thạch nhũ trong tự nhiên:
CaCO3(s) + CO2(aq) + H2O(l) ⇌ Ca(HCO3)2(aq)
+ Phản ứng của hơi iodine với khí hydrogen:
H2(g) + I2(g) ⇌ 2HI(g)
Luyện tập 1 trang 7 Hoá học 11: Phản ứng thuận nghịch có xảy ra hoàn toàn được không? Vì sao?
Lời giải:
Phản ứng thuận nghịch xảy ra không hoàn toàn. Do phản ứng thuận nghịch xảy ra đồng thời sự chuyển chất phản ứng thành chất sản phẩm và sự chuyển chất sản phẩm thành chất phản ứng (ở cùng điều kiện).
Câu hỏi 2 trang 7 Hoá học 11: Xét ví dụ 2:
Lời giải:
Quá trình trộn khí hydrogen với hơi iodine được thể hiện qua phản ứng thuận nghịch:
H2(g) + I2(g) ⇌ 2HI(g)
a) Tại thời điểm ban đầu, ngay khi vừa mới trộn khí H2 và hơi I2 với nhau, chưa có HI tạo thành, nồng độ H2 và I2 là lớn nhất. Nồng độ của I2 lớn nhất nên màu tím của hỗn hợp là đậm nhất.
Sau khi trộn khí H2 và hơi I2, phản ứng thuận diễn ra và nồng độ H2 và I2 giảm dần nên màu tím của hỗn hợp khí cũng nhạt dần.
b) Sau một khoảng thời gian, màu tím của hỗn hợp không thay đổi, chứng tỏ nồng độ của một chất bất kì trong phản ứng không đổi (do lượng mất đi và lượng sinh ra chất đó là bằng nhau).
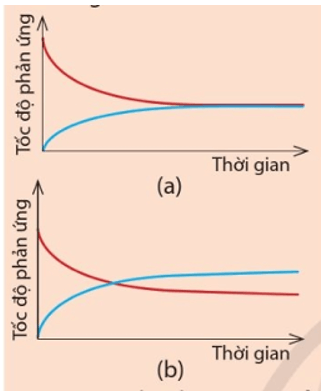
Câu hỏi 3 trang 8 Hoá học 11: Cho hai đồ thị (a) và (b) dưới đây. Mỗi đồ thị biểu diễn sự thay đổi tốc độ của phản ứng thuận và tốc độ của phản ứng nghịch theo thời gian.
Lời giải:
Đồ thị (a) thể hiện đúng Ví dụ 2. Do sau một khoảng thời gian nhất định, tốc độ của phản ứng thuận bằng tốc độ của phản ứng nghịch.
Đường màu xanh trong đồ thị biểu diễn tốc độ phản ứng nghịch. Do sau khi trộn hai khí, phản ứng thuận diễn ra, nồng độ H2 và I2 giảm dần nên vthuận giảm dần. Trong khi đó, lượng HI sinh ra theo phản ứng thuận càng nhiều và nồng độ HI tăng nên v nghịch tăng dần.
Câu hỏi 4 trang 8 Hoá học 11: Vì sao giá trị ktkn là một hằng số ở nhiệt độ xác định?
Lời giải:
kt, kn lần lượt là hằng số tốc độ phản ứng thuận, hằng số tốc độ phản ứng nghịch mà giá trị của kt, kn chỉ phụ thuộc vào nhiệt độ và bản chất của các chất tham gia phản ứng, nên tại một nhiệt độ xác định giá trị ktkn là hằng số.