Lý thuyết Phenol (Chân trời sáng tạo 2024) Hóa 11
Tóm tắt lý thuyết Hóa 11 Bài 17: Phenol ngắn gọn, chính xác sách Chân trời sáng tạo sẽ giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt Hóa 11.
Nội dung bài viết
Xem thêm »
Lý thuyết Hóa 11 Bài 17: Phenol - Chân trời sáng tạo
A. Lý thuyết Phenol
1. Khái niệm và cấu trúc
- Phenol là những hợp chất hữu cơ trong phân tử có nhóm –OH liên kết trực tiếp với nguyên tử carbon của vòng benzene.
- Phenol cũng là tên của chất đơn giản nhất (monohydroxybenzene) trong nhóm các hợp chất phenol.
- Phenol có nhóm phenyl hút electron, làm giảm mật độ electron ở nguyên tử oxygen, dẫn đến tăng sự phân cực của liên kết O-H đồng thời làm tăng mật độ electron trong vòng benzene, đặc biệt ở vị trí o,p
2. Tính chất vật lý
- Phenol là chất rắn, không màu, ít tan trong nước lạnh, tan vô hạn trong nước ở 66℃, tan tốt trong ethanol.
- Phenol độc, gây bỏng cho da.
- Các phenol có nhiệt độ nóng chảy, nhiệt độ sôi cao hơn các hydrocarbon thơm có khối lượng phân tử tương đương.
3. Tính chất hóa học
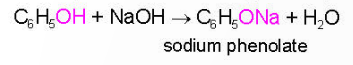
a) Phản ứng thế nguyên tử H của nhóm OH: tính acid
- Phenol thể hiện tính acid yếu, dung dịch phenol không làm đổi màu quỳ tím.
- Do nhóm phenyl hút electron, làm tăng sự phân cực của liên kết O-H, dẫn đến tính acid của phenol.
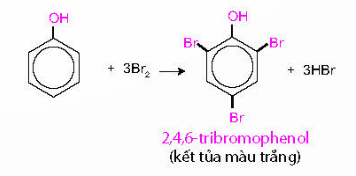
b) Phản ứng thế nguyên tử hydrogen của vòng benzene
- Nhóm OH làm tăng khả năng phản ứng thế nguyên tử H trong vòng benzene của phenol, ưu tiên thế nguyên tử H ở các vị trí 2, 4, 6.
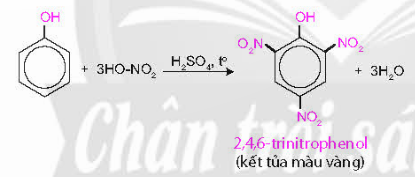
4. Ứng dụng và điều chế
a) Ứng dụng
- Dung dịch phenol ở nồng độ thấp được sử dụng như chất sát trùng, diệt nấm, vi khuẩn, virus, thuốc tăng trưởng thực vật.
- Trong công nghiệp, phenol là nguyên liệu ban đầu để sản xuất chất dẻo, chất kết dính, chất nổ, tổng hợp dược phầm hay sản xuất thuốc nhuộm azo.
b) Điều chế
- Trong công nghiệp:
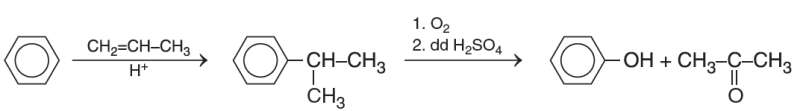
- Ngoài ra, một lượng lớn phenol được tách ra từ nhựa than đá.
Sơ đồ tư duy Phenol
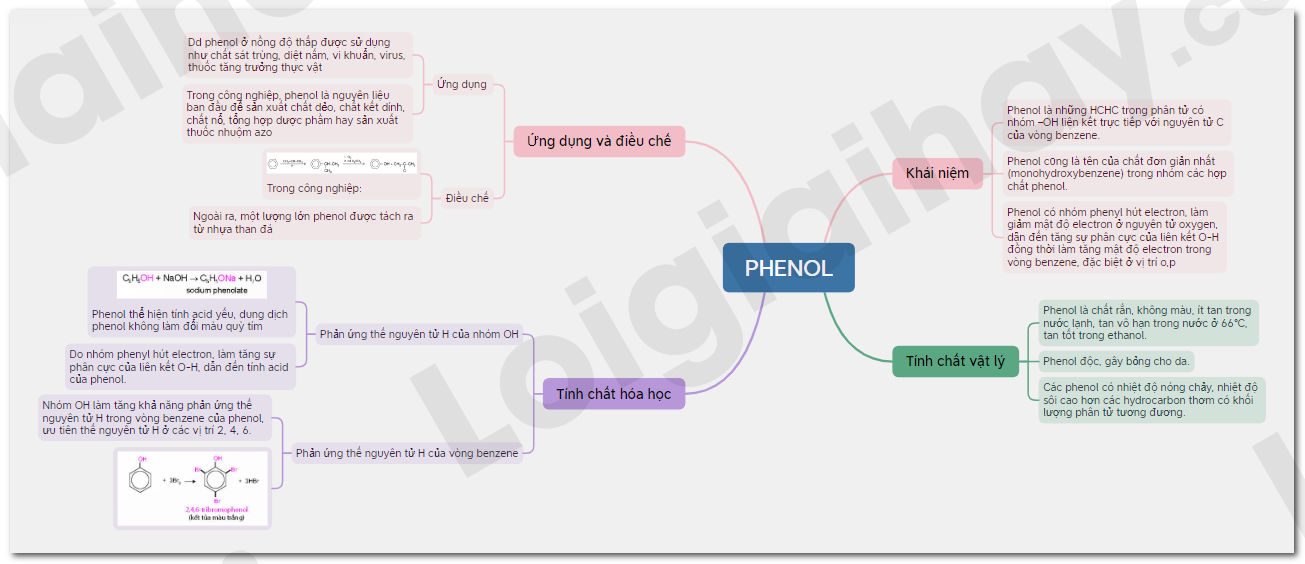
B. Trắc nghiệm Phenol
Đang cập nhật ...