Trắc nghiệm Hóa 12 (có đáp án): Tổng hợp bài tập điện phân hay và khó
- 1Làm xong biết đáp án, phương pháp giải chi tiết.
- 2Học sinh có thể hỏi và trao đổi lại nếu không hiểu.
- 3Xem lại lý thuyết, lưu bài tập và note lại các chú ý
- 4Biết điểm yếu và có hướng giải pháp cải thiện
Tiến hành điện phân dung dịch chứa 43,24 gam hỗn hợp gồm và NaCl bằng điện cực trơ màng ngăn xốp với cường độ dòng điện không đổi. Sau thời gian t giây thì nước bắt đầu điện phân ở cả 2 điện cực, thấy khối lượng catot tăng so với ban đầu, đồng thời anot thoát ra một khí duy nhất có thể tích là 4,48 lít (đktc). Nếu thời gian điện phân là 2t giây thì khối lượng dung dịch giảm 25,496 gam. Kim loại M là
A. Ni
B. Cu
D. Fe
D. Zn
Tiến hành điện phân dung dịch chứa 28,87 gam hỗn hợp gồm và NaCl bằng điện cực trơ màng ngăn xốp với cường độ dòng điện không đổi. Sau thời gian t giây thì nước bắt đầu điện phân ở cả 2 điện cực, thấy khối lượng catot tăng so với ban đầu, đồng thời anot thoát ra một khí duy nhất có thể tích là 2,464 lít (đktc). Nếu thời gian điện phân là 2t giây thì khối lượng dung dịch giảm 16,21 gam. Kim loại M là
A. Ni
B. Cu
C. Fe
D. Zn
Điện phân (điện cực trơ, màng ngăn xốp) dung dịch gồm và NaCl (tỉ lệ mol tương ứng 1 : 3) với cường độ dòng điện 1,34A. Sau thời gian t giờ, thu được dung dịch Y (chứa hai chất tan) có khối lượng giảm 10,375 gam so với dung dịch ban đầu. Cho bột Al dư vào Y, thu được 1,68 lít khí (đktc). Biết các phản ứng xảy ra hoàn toàn, hiệu suất điện phân 100%, bỏ qua sự hòa tan của khí trong nước và sự bay hơi của nước. Giá trị của t là
A. 7
B. 6
C. 5
D. 4
Điện phân (điện cực trơ, màng ngăn xốp) dung dịch gồm và NaCl (tỉ lệ mol tương ứng 1: 3) với cường độ dòng điện 2A. Sau thời gian t giờ, thu được dung dịch Y (chứa hai chất tan) có khối lượng giảm 70,4 gam so với dung dịch ban đầu. Cho bột Al dư vào Y, thu được 13,44 lít khí (đktc). Biết các phản ứng xảy ra hoàn toàn, hiệu suất điện phân 100%, bỏ qua sự hòa tan của khí trong nước và sự bay hơi của nước. Giá trị của t là
A. 15
B. 16
C. 17
D. 18
Điện phân dung dịch muối (M là kim loại) với điện cực trơ cường độ dòng điện không đổi. Sau thời gian t giây thu được a mol khí ở anot. Nếu thời gian điện phân là 2t giây thì tống số mol khí thu được ở cả hai điện cực là 2,5a mol. Giả sử hiệu suất điện phân là 100%. Khí sinh ra không tan trong nước. Phát biều nào sau đây sai
A.
B.
C.
D.
Hòa tan hoàn toàn m gam hỗn hợp và NaCl vào nước thu được dung dịch X. Tiến hành điện phân X với các điện cực trơ, màng ngăn xốp, dòng điện có cường độ không đổi. Tổng số mol khí thu được trên cả hai điện cực (n) phụ thuộc vào thời gian điện phân (t) được mô tả như đồ thị bên (đồ thị gấp khúc tại các điểm M, N). Giả sử hiệu suất điện phân là 100%, bỏ qua sự bay hơi của nước. Giá trị của m là
A. 14,48
B. 15,76
C. 13,42
D. 11,08
Điện phân dung dịch chứa với điện cực trơ trong thời gian t (s), cường độ dòng điện 2A thu được dung dịch X. Cho m gam bột Mg vào dung dịch X, sau phản ứng xảy ra hoàn toàn thu được 0,336 gam hỗn hợp kim loại; 0,112 lít hỗn hợp khí Z (đktc) gồm NO và có tỉ khối đối với là 19,2 và dung dịch Y chứa 3,04 gam muối. Cho toàn bộ hỗn hợp bột kim loại trên tác dụng với dung dịch HCl dư thu được 0,112 lit khí (đktc). Giá trị của t là
A. 2267,75
B. 2895,10
C. 2316,00
D. 2219,40
Điện phân dung dịch chứa với điện cực trơ trong thời gian t (s), cường độ dòng điện 2A thu được dung dịch X. Cho m gam bột Mg vào dung dịch X, sau phản ứng xảy ra hoàn toàn thu được 2,4 gam hỗn hợp kim loại; 3,36 lít hỗn hợp khí Z(đktc) gồm NO và có tỉ khối đối với là và dung dịch Y chứa 25,56 gam muối. Cho toàn bộ hỗn hợp bột kim loại trên tác dụng với dung dịch HCl dư thu được 0,224 lit khí (dktc). Giá trị của t là
A. 11097,5
B. 28950,1
C. 23167,6
D. 20196,4
Cho hai bình điện phân, bình (1) đựng 20 ml dung dịch NaOH 1,73M; bình (2) đựng dung dịch gồm 0,225 mol và 0,2 mol HCl. Mắc nối tiếp bình (1) và bình (2). Điện phân các dung dịch bằng dòng điện một chiều với cường độ dòng điện không đổi một thời gian. Khi dừng điện phân, tháo ngay catot ở các bình. Sau phản ứng thấy nồng độ NaOH ở bình (1) là 2M, Cho tiếp 14 gam bột Fe vào bình (2) đến khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn không tan. Biết NO là sản phẩm khử duy nhất khối lượng riêng của nước là 1 g/ml. Giá trị m là
A. 9,8
B. 10,4
C. 8,3
D. 9,4
Điện phân 1 lít dung dịch X gồm 0,6M và 0,4M cho đến khi anot thoát ra 17,92 lít khí (đktc) thì dừng lại. Nhấc catot ra khỏi bình điện phân, rồi khuấy đều dung dịch còn lại để phản ứng xảy ra hoàn toàn thấy có khí thoát ra và thu được dung dịch Y có khối lượng giảm m gam so với dung dịch X. Giả thiết kim loại sinh ra đều bám vào catot, sản phẩm khử duy nhất của là NO. Giá trị gần nhất của m là
A. 100,6
B. 91,0
C. 92,0
D. 89,0
Điện phân dung dịch với điện cực trơ, sau một thời gian thu được dung dịch X chứa 2 chất tan có cùng nồng độ (mol/lít), và thấy khối lượng dung dịch giảm đi 9,28 gam so với ban đầu. Cho tiếp 2,8 gam bột Fe vào dung dịch X, thu được dung dịch Y và chất rắn Z và khí NO ( sản phẩm khử duy nhất của ). Biết các phản ứng xảy ra hoàn toàn. Tổng khối lượng muối trong dung dịch Y là:
A. 11,48
B. 15,08
C. 10,24
D. 13,64
Điện phân dung dịch với điện cực trơ, sau một thời gian thu được dung dịch X chứa 2 chất tan có cùng nồng độ (mol/lít), và thấy khối lượng dung dịch giảm đi 11,6 gam so với ban đầu. Cho tiếp 3,36 gam bột Fe vào dung dịch X, thu được dung dịch Y và chất rắn Z và khí NO ( sản phẩm khử duy nhất của N5+). Biết các phản ứng xảy ra hoàn toàn. Tổng khối lượng muối trong dung dịch Y là
A. 14,8
B. 14,21
C. 10,24
D. 13,64
Điện phân (với điện cực trơ, màng ngăn xốp) dung dịch chứa hỗn hợp và NaCl (tỉ lệ 1 : 1) bằng dòng điện một chiều có cường độ ổn định. Sau t (h), thu được dung dịch X và sau 2t (h) thu được dung dịch Y. Dung dịch X tác dụng với bột Al dư, thu được a mol khí . Dung dịch Y tác dụng với bột Al dư thu được 4a mol khí Phát biểu nào sau đây không đúng
A. Tại thời điểm 2t (h), tổng số mol khí thoát ra ở hai điện cực là 9a mol
B. Khi thời gian là 1,75t (h), tại catot đã có khí thoát ra
C. Tại thời điểm 1,5t (h), Cu2+ chưa điện phân hế
D. Nước bắt đầu điện phân tại anot ở thời điểm 0,75t (h)
Điện phân (với điện cực trơ, màng ngăn xốp) dung dịch chứa hỗn hợp và NaCl (tỉ lệ 1 : 1) bằng dòng điện một chiều có cường độ ổn định. Sau t (h), thu được dung dịch X và sau 2t (h) thu được dung dịch Y. Dung dịch X tác dụng với bột Al dư, thu được a mol khí . Dung dịch Y tác dụng với bột Al dư thu được 3a mol khí H2. Phát biểu nào sau đây không đúng
A. Tại thời điểm 2t (h), tổng số mol khí thoát ra ở hai điện cực là 9a mol
B. Khi thời gian là 1,75t (h), tại catot đã có khí thoát ra
C. Tại thời điểm 1,5t (h), Cu2+ chưa điện phân hết
D. Nước bắt đầu điện phân tại anot ở thời điểm 0,75t (h)
Điện phân (với điện cực trơ, màng ngăn) dung dịch chứa hỗn hợp và NaCl (trong đó số mol NaCl gấp 4 lần số mol ) bằng dòng điện một chiều có cường độ ổn định. Sau t (h), thu được dung dịch X và sau 2t (h), thu được dung dịch Y. Dung dịch X tác dụng với bột Al dư, thu được 1,5a mol khí . Dung dịch Y tác dụng với bột Al dư, thu được 12a mol khí . Biết hiệu suất điện phân 100%, các phản ứng xảy ra hoàn toàn, các khí sinh ra không hòa tan vào nước. Phát biểu nào dưới đây đúng
A. Tại thời điểm 0,85t (h), tại catot đã có khí thoát ra
B. Tại thời điểm 2t (h), tổng số mol khí thoát ra ở hai cực là 13a mol
C. Tại thời điểm 1,8t (h), mol khí O2 thoát ra ở anot là 0,05a mol
D. Tại thời điểm t (h), mol khí thoát ra ở anot là 5a mol
Dung dịch X chứa m gam chất tan gồm (có m> 5 gam) và NaCl. Điện phân dung dịch X với điện cực trơ, màng ngăn xốp và cường độ dòng điện không đổi. Sau thời gian t giây thì thu được dung dịch Y chứa (m – 18,79) gam chất tan và có khí thoát ra ở catot. Nếu thời gian điện phân là 2t giây thì thu được dung dịch Z chứa z gam chất tan và hỗn hợp khí T chứa 3 khí và có tỉ khối hơi so với là 16. Cho Z vào dung dịch chứa 0,1 mol và 0,2 mol HCl thì thu được dung dịch chứa (z + 16,46) gam chất tan và có khí thoát ra. Tổng giá trị m + z là
A. 73,42
B. 72,76
C. 74,56
D. 76,24
Dung dịch X chứa m gam chất tan gồm (có m
A. 36,35
B. 35,36.
C. 37,18
D. 38,17
Hòa tan hoàn toàn m gam hỗn hợp
A. 48,775
B. 58,175
C. 31,675
D. 69,350
Tiến hành điện phân dung dịch chứa NaCl và 0,14 mol
A. 18,9 g
B. 19,38 g
C. 20,52 g
D. 20,3 g
Điện phân V lit dung dịch X (điện cực trơ, màng ngăn xốp , cường độ dòng điện không đổi) chứa đồng thời
A. 0,6
B. 0,8
C. 0,4
D. 1,6
Điện phân (điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi) V lít dung dịch X chứa đồng thời 0,45M (R là kim loại hóa trị không đổi) và NaCl 0,4M trong thời gian t giây, thu được 6,72 lít hỗn hợp khí ở anot (đktc). Nếu thời gian điện phân là 2t giây thì thu được dung dịch Y. Dung dịch Y tác dụng vừa đủ với 400 ml dung dịch chứa KOH 0,75M và NaOH 0,5M không sinh ra kết tủa. Biết hiệu suất điện phân 100%, các khí sinh ra không tan trong dung dịch. Giá trị của V là
A. 1
B. 0,5
C. 0,75
D. 2
Điện phân (với điện cực trơ, cường độ dòng điện không đổi) dung dịch muối nitrat của một kim loại M (có hóa trị không đổi). Sau thời gian t giây, khối lượng dung dịch giảm 6,96 gam và tại catot chỉ thu được (a) gam kim loại M. Sau thời gian 2t giây, khối lượng dung dịch giảm 11,78 gam và tại catot thoát ra 0,224 lít khí (đktc). Giá trị của (a) là
A. 8,64
B. 8,6
C. 6,48
D. 5,6
Điện phân dung dịch X chứa KCl và bằng dòng điện một chiều có cường độ 5A (điện cực trơ, màng ngăn xốp, hiệu suất điện phân 100%, các khí sinh ra không tan trong dung dịch). Toàn bộ khí sinh ra trong quá trình điện phân (ở cả hai điện cực) theo thời gian được biểu diễn bằng đồ thị bên
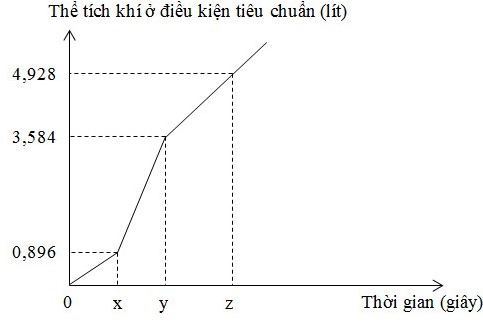
Phát biểu nào sau đây đúng
A.
B.
C.
D.
Cho hỗn hợp X gồm và . Điện phân dung dịch chứa m gam hỗn hợp X với điện cực trơ, cường độ dòng điện 2,68A, trong thời gian là 4 giờ. Sau khi kết thúc điện phân thu được dung dịch Y có khối lượng giảm 20,6 gam so với trước khi điện phân. Toàn bộ dung dịch Y tác dụng với lượng dư dung dịch thu được 136,4 gam kết tủa. Mặt khác cho 14,88 gam bột Mg vào dung dịch chứa m gam hỗn hợp X ban đầu. Kết thúc phản ứng thu được m' gam kim loại. Giá trị của m' là
A. 26,88 gam
B. 35,68 gam
C. 19,2 gam
D. 24,48 gam
Sự điện phân là quá trình oxi hóa – khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện ly nóng chảy hoặc dung dịch chất điện ly nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân: * Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều. * Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều. Cho dãy điện hóa sau:
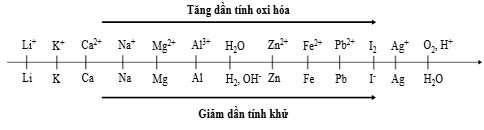
Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời thời và bằng hệ điện phân sử dụng các điện cực than chì.
Bán phản ứng nào xảy ra ở anot
A.
B.
C.
D.
Sự điện phân là quá trình oxi hóa – khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện ly nóng chảy hoặc dung dịch chất điện ly nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân: * Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều. * Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều. Cho dãy điện hóa sau:

Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời và bằng hệ điện phân sử dụng các điện cực than chì.
Dựa theo dãy điện hóa đã cho ở trên và từ Thí nghiệm, hãy cho biết
Bán phản ứng nào xảy ra ở catot
A.
B.
C.
D.
Sự điện phân là quá trình oxi hóa – khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện ly nóng chảy hoặc dung dịch chất điện ly nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân: * Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều. * Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều. Cho dãy điện hóa sau:

Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời thời và bằng hệ điện phân sử dụng các điện cực than chì.
Dựa theo dãy điện hóa đã cho ở trên và từ Thí nghiệm hãy cho biết Giá trị pH của dung dịch thay đổi như thế nào?
A. pH tăng do OH- sinh ra ở catot
B. pH giảm do H+ sinh ra ở anot
C. pH không đổi do không có H+ và OH- sinh ra
D. pH không đổi do lượng H+ sinh ra ở anot bằng với lượng OH- sinh ra ở catot
Sự điện phân là quá trình oxi hóa – khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện ly nóng chảy hoặc dung dịch chất điện ly nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân: * Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều. * Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều. Cho dãy điện hóa sau:

Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời thời và bằng hệ điện phân sử dụng các điện cực than chì.
Dựa theo dãy điện hóa đã cho ở trên và từ Thí nghiệm hãy cho biết
Nếu người sinh viên đổi 2 điện cực than chì bằng 2 điện cực kim loại Pb, phản ứng nào xảy ra ở catot và anot
A.
B.
C.
D.
Điện phân 400 ml (không đổi) dung dịch gồm NaCl, HCl và 0,02M (điện cực trơ, màng ngăn xốp) với cường độ dòng điện bằng 1,93A. Mối liên hệ giữa thời gian điện phân và pH của dung dịch điện phân được biểu diễn dưới đây
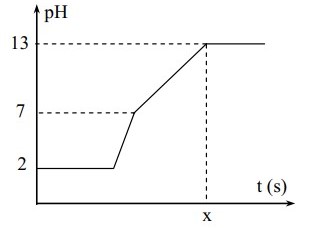
Giá trị của t trên đồ thị là
A. 3600
B. 3000
C. 1800
D. 1200
Tiến hành điện phân 100 gam dung dịch chứa 0,2 mol ; 0,1 mol và 0,16 mol HCl (với 2 điện cực trơ) đến khi có khi bắt đầu thoát ra ở cả hai điện cực thì dừng điện phân. Đem phần dung dịch cho tác dụng hết với 150 gam dung dịch chứa , kết thúc phản ứng thu được 90,08 gam kết tủa và dung dịch Y chứa một muối duy nhất có nồng độ a%. Giá trị của a gần nhất với giá trị nào sau đây
A. 34,5
B. 33,5
C. 30,5
D. 35,5
Hòa tan hoàn toàn m gam hỗn hợp và NaCl vào nước thu được dung dịch X. Tiến hành điện phân X với các điện cực trơ, màng ngăn xốp, dòng điện có cường độ không đổi. Tổng số mol khí thu được trên cả hai điện cực (n) phụ thuộc vào thời gian điện phân (t) được mô tả như đồ thị bên (đồ thị gấp khúc tại các điểm M, N). Giả sử hiệu suất điện phân là 100%, bỏ qua sự bay hơi của nước. Giá trị của m là
A. 14,48
B. 15,76
C. 13,42
D. 11,08
Hòa tan hoàn toàn m gam hỗn hợp gồm và NaCl vào nước thu được dung dịch X. Tiến hành điện phân X với các điện cực trơ, màng ngăn xốp, dòng điện có cường độ không đổi. Tổng số mol khí thu được ở cả hai điện cực (n) phụ thuộc vào thời gian điện phân (t) được mô tả như đồ thị bên (đồ thị gấp khúc tại các điểm M, N)
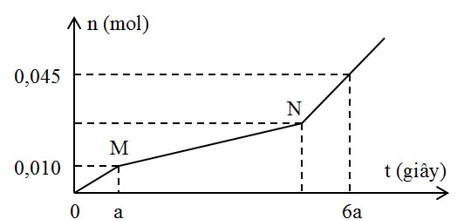
Giả thiết hiệu suất điện phân là 100%, bỏ qua sự bay hơi của nước. Giá trị của m là
A. 2,77
B. 7,57
C. 5,97
D. 9,17
Tiến hành điện phân dung dịch chứa a mol KCl và b mol với điện cực trơ, màng ngăn xốp, cường độ dòng điện không đổi I = 7,5A, trong thời gian t = 4632s, thu được dung dịch X, đồng thời anot thoát ra 0,12 mol hỗn hợp khí. Nếu thời gian điện phân là 1,5t (s) thì tổng số mol khí thoát ra ở 2 điện cực là 0,215 mol. Giả sử trong quá trình điện phân nước bay hơi không đáng kể, hiệu suất điện phân đạt 100%, các khí sinh ra không tan trong nước, bỏ qua sự thủy phân của muối. Cho các phát biểu liên quan đến bài toán: (a) Tổng khối lượng 2 muối trước điện phân là 35,48g
(b) Nếu thời gian điện phân là 1,25t (s) thì nước đã điện phân ở 2 điện cực
(c) Giá trị của a, b lần lượt là 0,12 và 0,25
(d) Dung dịch X chỉ có 2 chất tan (e) Đến thời điểm 1,5t (s), số mol H+ sinh ra ở anot là 0,32 mol Số phát biểu sai là:
A. 4
B. 1
C . 2
D. 3
Cho sơ đồ phản ứng
Trong sơ đồ trên, mỗi mũi tên là một phản ứng, các chất X, Y, Z lần lượt là những chất nào sau đây
A.
B.
C.
D.
Cho lá Al vào dung dịch HCl, có khí thoát ra. Thêm vài giọt dung dịch vào thì
A. Phản ứng ngừng lại
B. Tốc độ thoát khí không đổi
C. Tốc độ thoát khí giảm
D. Tốc độ thoát khí tăng
Cho lá Mg vào dung dịch HCl, có khí thoát ra. Thêm vài giọt X vào thì tốc độ thoát khí lớn hơn. X là
A.
B.
C.
D.
Trường hợp nào sau đây xảy ra ăn mòn điện hoá
A.
B.
C.
D.
Cho các trường hợp sau:
1, Thanh Magie nhúng trong dung dịch HCl.
2, Thanh sắt nhúng trong dung dịch .
3, Sợi dây đồng nhúng trong dung dịch dặc nóng.
4, Đốt lá sắt trong khí . Trường hợp nào sau đây không xảy ra ăn mòn điện hoá
A. 1
B. 2
C. 3
D. 4
Có 4 dung dịch riêng biệt: . Nhúng vào mỗi dung dịch một thanh Ni. Số trường hợp xuất hiện ăn mòn điện hoá là
A. 1
B. 4
C. 3
D. 2
Có 4 dung dịch riêng biệt: . Nhúng vào mỗi dung dịch một thanh Sn. Số trường hợp xuất hiện ăn mòn điện hoá là
A. 1
B. 4
C. 3
D. 2
Oxi hoá hoàn toàn m gam kim loại X cần vừa đủ 0,25m gam khí . X là kim loại nào sau đây
A. Cu
B. Ca
C. Al
D. Fe
Oxi hoá hoàn toàn m gam kim loại X cần vừa đủ 0,667m gam khí . X là kim loại nào sau đây
A. Zn
B. Ca
C. Al
B. Mg
Đốt cháy hoàn toàn 7,2 gam kim loại M (có hoá trị hai không đổi trong hợp chất) trong hỗn hợp khí . Sau phản ứng thu được 23,0 gam chất rắn và thể tích hỗn hợp khí đã phản ứng là 5,6 lít (ở đktc). Kim loại M là
A. Mg
B. Ca
C. Be
D. Cu
Đốt cháy hoàn toàn 6 gam kim loại M (có hoá trị hai không đổi trong hợp chất) trong hỗn hợp khí Cl2 và O2. Sau phản ứng thu được 11,15 gam chất rắn và thể tích hỗn hợp khí đã phản ứng là 2,24 lít (ở đktc). Kim loại M là
A. Mg
B. Ca
C. Be
D. Cu
Cho 7,84 lít hỗn hợp khí X (đktc) gồm phản ứng vừa đủ với 11,1 gam hỗn hợp Y gồm Mg và Al, thu được 30,1 gam hỗn hợp Z. Phần trăm khối lượng của Al trong Y là
A. 75,68%
B. 24,32%
C. 51,35%
D. 48,65%
Cho 8,4 lít hỗn hợp khí X (đktc) gồm phản ứng vừa đủ với 10,2 gam hỗn hợp Y gồm Mg và Al, thu được 31,95 gam hỗn hợp Z. Phần trăm khối lượng của Mg trong Y là
A. 47,06%
B. 23,52%
C. 52,94%
D. 48,65%
Hòa tan hỗn hợp X gồm 11,2 gam Fe và 2,4 gam Mg bằng dung dịch loãng (dư), thu được dung dịch Y. Cho dung dịch NaOH dư vào Y thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được m gam chất rắn. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m là
A. 36
B. 20
C. 18
D. 24
Hòa tan hỗn hợp X gồm 8,4 gam Fe và 3,6 gam Mg bằng dung dịch HCl loãng (dư), thu được dung dịch Y. Cho dung dịch NaOH dư vào Y thu được kết tủa Z. Nung Z trong không khí đến khối lượng không đổi, thu được m gam chất rắn. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m là
A. 36
B. 20
C. 18
D. 24
Cho 12 gam hợp kim của bạc vào dung dịch loãng (dư), đun nóng đến phản ứng hoàn toàn, thu được dung dịch có 8,5 gam . Phần trăm khối lượng của bạc trong mẫu hợp kim là
A. 65%
B. 30%
C. 55%
D. 45%
Cho 20 gam hợp kim của đồng vào dung dịch loãng (dư), đun nóng đến phản ứng hoàn toàn, thu được dung dịch có 37,6 gam . Phần trăm khối lượng của đồng trong mẫu hợp kim là
A. 60%
B. 64%
C. 30%
D. 32%
Cho 2,8 gam hỗn hợp X gồm Cu và Ag phản ứng hoàn toàn với dung dịch dư, thu được 0,04 mol (sản phẩm khử duy nhất của ) và dung dịch chứa m gam muối. Giá trị của m là
A. 4,08
B. 3,62
C. 3,42
D. 5,28
Cho 23,6 gam hỗn hợp X gồm Cu và Ag phản ứng hoàn toàn với dung dịch dư, thu được 11,2 lít (sản phẩm khử duy nhất của ) và dung dịch chứa m gam muối. Giá trị của m là
A. 23,7
B. 42,2
C. 54,6
D. 60,8
Hoà tan hoàn toàn 12,42 gam Al bằng dung dịch loãng (dư), thu được dung dịch X và 1,344 lít (ở đktc) hỗn hợp khí Y gồm 2 khí là và . Tỉ khối của hỗn hợp khí Y so với khí H2 là 18. Cô cạn dung dịch X, thu được m gam chất rắn khan. Giá trị của m là
A. 38,34
B. 34,08
C. 106,38
D. 97,98
Hoà tan hoàn toàn 35,1 gam Al bằng dung dịch loãng (dư), thu được dung dịch X và 8,4 lít (ở đktc) hỗn hợp khí Y gồm 2 khí là . Tỉ khối của hỗn hợp khí Y so với khí là 18,8. Cô cạn dung dịch X, thu được m gam chất rắn khan. Giá trị của m là
A. 282,9
B. 276,9
C. 308,38
D. 97,98
Cho 2,24 gam bột sắt vào 200 ml dung dịch chứa hỗn hợp gồm 0,1M và 0,5M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và m gam chất rắn Y. Giá trị của m là
A. 2,8
B. 2,16
C. 4,08
D. 0,64
Cho 8,4gam bột sắt vào 100 ml dung dịch chứa hỗn hợp gồm 2M và 1M. khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X và m gam chất rắn Y. Giá trị của m là
A. 24,8
B. 21,6
C. 28
D. 14
Cho một lượng bột Zn vào dung dịch X gồm . Khối lượng chất rắn sau khi các phản ứng xảy ra hoàn toàn nhỏ hơn khối lượng bột Zn ban đầu là 0,5 gam. Cô cạn phần dung dịch sau phản ứng thu được 13,6 gam muối khan. Tổng khối lượng các muối trong X là
A. 13,1 gam
B. 17,0 gam
C. 19,5 gam
D. 14,1 gam
Cho một lượng bột Zn vào dung dịch X gồm Khối lượng chất rắn sau khi các phản ứng xảy ra hoàn toàn nhỏ hơn khối lượng bột Zn ban đầu là 1 gam. Cô cạn phần dung dịch sau phản ứng thu được 37,8 gam muối khan. Tổng khối lượng các muối trong X là
A. 37,8 gam
B. 36,8 gam
C. 38,8 gam
D. 34,1 gam
Cho m gam bột Cu vào 400 ml dung dịch 0,2M, sau một thời gian phản ứng thu được 7,76 gam hỗn hợp chất rắn X và dung dịch Y. Lọc tách X, rồi thêm 5,85 gam bột Zn vào Y, sau khi phản ứng xảy ra hoàn toàn thu được 10,53 gam chất rắn Z. Giá trị của m là
A. 5,12
B. 3,84
C. 5,76
D. 6,4
Cho m gam bột Cu vào 100 ml dung dịch 2M, sau một thời gian phản ứng thu được 17,04 gam hỗn hợp chất rắn X và dung dịch Y. Lọc tách X, rồi thêm 8,45 gam bột Zn vào Y, sau khi phản ứng xảy ra hoàn toàn thu được 12,91 gam chất rắn Z. Giá trị của m là
A. 5,12
B. 3,84
C. 5,76
D. 6,4
Cho V lít hỗn hợp khí (ở đktc) gồm CO và phản ứng với một lượng dư hỗn hợp rắn gồm CuO và nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng hỗn hợp rắn giảm 0,32 gam. Giá trị của V là
A. 0,448
B. 0,112
C. 0,224
D. 0,560
Cho V lít hỗn hợp khí (ở đktc) gồm CO và phản ứng với một lượng dư hỗn hợp rắn gồm CuO và nung nóng. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng hỗn hợp rắn giảm 2,4 gam. Giá trị của V là
A. 4,48
B. 3,36
C. 6,72
D. 5,6
Khử hoàn toàn m gam oxit cần vừa đủ 17,92 lít khí CO (đktc), thu được a gam kim loại M. Hoà tan hết a gam M bằng dung dịch đặc nóng (dư), thu được 20,16 lít khí (sản phẩm khử duy nhất, ở đktc). Oxit MxOy là
A.
B.
C.
D.
Khử hoàn toàn 7,2 gam oxit cần vừa đủ 2,24 lít khí CO (đktc), thu được a gam kim loại M. Hoà tan hết a gam M bằng dung dịch đặc nóng (dư), thu được 3,36 lít khí (sản phẩm khử duy nhất, ở đktc). Oxit là
A.
B.
C.
D.
Cho hơi nước đi qua than nóng đỏ, thu được 15,68 lít hỗn hợp khí X (đktc) gồm CO, và H2. Cho toàn bộ X tác dụng hết với CuO (dư) nung nóng, thu được hỗn hợp chất rắn Y. Hoà tan toàn bộ Y bằng dung dịch (loãng, dư) được 8,96 lít NO (sản phẩm khử duy nhất, ở đktc). Phần trăm thể tích khí CO trong X là
A. 57,15%
B. 14,28%
C. 28,57%
D. 18,42%
Cho hơi nước đi qua than nóng đỏ, thu được 3,92 lít hỗn hợp khí X (đktc) gồm CO, . Cho toàn bộ X tác dụng hết với CuO (dư) nung nóng, thu được hỗn hợp chất rắn Y. Hoà tan toàn bộ Y bằng dung dịch HNO3 (loãng, dư) được 2,24 lít NO (sản phẩm khử duy nhất, ở đktc). Phần trăm thể tích khí CO trong X là
A. 57,15%
B. 14,28%
C. 28,57%
D. 18,42%
Phát biểu nào sau đây sai?
A. Cho viên kẽm vào dung dịch HCl thì kẽm bị ăn mòn hóa học
B. Quặng boxit là nguyên liệu dùng để sản xuất nhôm
C. Đốt Fe trong khí dư, thu được
D. Tính khử của Ag mạnh hơn tính khử của Cu
Cho 6 kim loại sau: Na, Ba, Fe, Ag, Mg, Al lần lượt vào dung dịch dư. Số trường hợp thu được chất sản phẩm là kết tủa sau phản ứng là
A. 5
B. 3
C. 2
D. 4
Sự ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường xung quanh. Đó là một quá trình hóa học hoặc quá trình điện hóa trong đó kim loại bị oxi hóa thành ion dương.
Có hai dạng ăn mòn kim loại là ăn mòn hóa học và ăn mòn điện hóa học: - Ăn mòn hóa học là quá trình oxi hóa - khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường.
- Ăn mòn điện hóa học là quá trình oxi hóa - khử, trong đó kim loại bị ăn mòn do tác dụng của dung dịch chất điện li và tạo nên dòng electron chuyển dời từ cực âm đến cực dương.
Thí nghiệm 1: Tiến hành thí nghiệm theo các bước sau: Bước 1: Rót dung dịch loãng vào cốc thủy tinh.
Bước 2: Nhúng thanh kẽm và thanh đồng (không tiếp xúc nhau) vào cốc đựng dung dịch loãng.
Bước 3: Nối thanh kẽm với thanh đồng bằng dây dẫn (có mắc nối tiếp với một điện kế).
Thí nghiệm 2: Để 3 thanh hợp kim: Cu-Fe (1); Fe-C (2); Fe-Zn (3) trong không khí ẩm
Từ Thí nghiệm 1, một bạn học sinh đã đưa ra các phát biểu sau
(1) Sau bước 2, chưa có bọt khí thoát ra tại bề mặt của hai thanh kim loại. (2) Sau bước 3, kim điện kế quay chứng tỏ xuất hiện dòng điện. (3) Trong dây dẫn, dòng electron di chuyển từ anot sang catot. (4) Sau bước 3, bọt khí thoát ra ở cả hai điện cực kẽm và đồng. (5) Sau bước 3, thanh đồng bị ăn mòn điện hóa đồng thời với sự tạo thành dòng điện
Số phát biểu đúng là
A. 2
B. 4
C. 3
D. 5
Sự ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường xung quanh. Đó là một quá trình hóa học hoặc quá trình điện hóa trong đó kim loại bị oxi hóa thành ion dương.
Có hai dạng ăn mòn kim loại là ăn mòn hóa học và ăn mòn điện hóa học: - Ăn mòn hóa học là quá trình oxi hóa - khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường.
- Ăn mòn điện hóa học là quá trình oxi hóa - khử, trong đó kim loại bị ăn mòn do tác dụng của dung dịch chất điện li và tạo nên dòng electron chuyển dời từ cực âm đến cực dương.
Thí nghiệm 1: Tiến hành thí nghiệm theo các bước sau: Bước 1: Rót dung dịch loãng vào cốc thủy tinh.
Bước 2: Nhúng thanh kẽm và thanh đồng (không tiếp xúc nhau) vào cốc đựng dung dịch loãng.
Bước 3: Nối thanh kẽm với thanh đồng bằng dây dẫn (có mắc nối tiếp với một điện kế).
Thí nghiệm 2: Để 3 thanh hợp kim: Cu-Fe (1); Fe-C (2); Fe-Zn (3) trong không khí ẩm
Trong Thí nghiệm 1, thanh kẽm và thanh đồng được nối với nhau bằng dây dẫn cùng nhúng trong dung dịch chất điện li tạo thành một cặp pin điện hóa. Quá trình xảy ra tại anot của pin điện này là
A.
B.
C.
D.
Sự ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác dụng của các chất trong môi trường xung quanh. Đó là một quá trình hóa học hoặc quá trình điện hóa trong đó kim loại bị oxi hóa thành ion dương.
Có hai dạng ăn mòn kim loại là ăn mòn hóa học và ăn mòn điện hóa học: - Ăn mòn hóa học là quá trình oxi hóa - khử, trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường.
- Ăn mòn điện hóa học là quá trình oxi hóa - khử, trong đó kim loại bị ăn mòn do tác dụng của dung dịch chất điện li và tạo nên dòng electron chuyển dời từ cực âm đến cực dương.
Thí nghiệm 1: Tiến hành thí nghiệm theo các bước sau: Bước 1: Rót dung dịch loãng vào cốc thủy tinh.
Bước 2: Nhúng thanh kẽm và thanh đồng (không tiếp xúc nhau) vào cốc đựng dung dịch loãng.
Bước 3: Nối thanh kẽm với thanh đồng bằng dây dẫn (có mắc nối tiếp với một điện kế).
Thí nghiệm 2: Để 3 thanh hợp kim: Cu-Fe (1); Fe-C (2); Fe-Zn (3) trong không khí ẩm
Trong Thí nghiệm 2, hợp kim có sắt bị ăn mòn là
A. (1), (2)
B. (2), (3)
C. (1), (3)
D. (1), (2), (3)