Lý thuyết Bảng tuần hoàn các nguyên tố hóa học và định luật tuần hoàn (Kết nối tri thức 2024) Hóa 10
Tóm tắt lý thuyết Hóa 10 Bài 9: Bảng tuần hoàn các nguyên tố hóa học và định luật tuần hoàn ngắn gọn, chính xác sách Kết nối tri thức sẽ giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt Hóa 10.
Nội dung bài viết
Xem thêm »
Lý thuyết Hóa học lớp 10 Bài 9: Bảng tuần hoàn các nguyên tố hóa học và định luật tuần hoàn
A. Lý thuyết Hóa học 10 Chương 2: Bảng tuần hoàn các nguyên tố hóa học và định luật tuần hoàn
1. Cấu tạo bảng tuần hoàn
a) Nguyên tắc sắp xếp các nguyên tố trong bảng tuần hoàn:
- Điện tích hạt nhân tăng dần.
- Cùng số lớp electron → cùng chu kì (hàng).
- Cùng số electron hóa trị → cùng nhóm (cột).
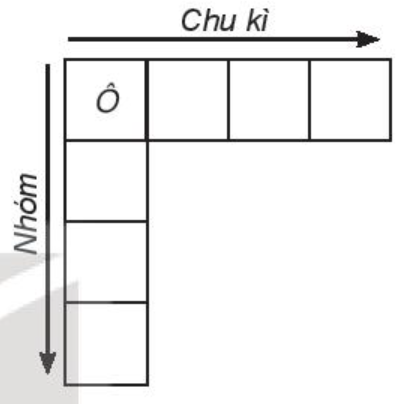
b) Trong bảng tuần hoàn (đến năm 2016) có 118 nguyên tố, 7 chu kì và 18 nhóm.
2. Xu hướng biến đổi trong bảng tuần hoàn
a) Bán kính nguyên tử
- Trong một chu kì, bán kính nguyên tử giảm theo chiều tăng dần của điện tích hạt nhân.
- Trong một nhóm A, bán kính nguyên tử tăng theo chiều tăng dần của điện tích hạt nhân.
b) Giá trị độ âm điện
Xu hướng biến đổi độ âm điện theo chiều tăng dần của điện tích hạt nhân:
- Độ âm điện tăng từ trái qua phải trong một chu kì.
- Độ âm điện giảm từ trên xuống dưới trong một nhóm A.
c) Tính kim loại, tính phi kim
- Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính kim loại giảm dần và tính phi kim tăng dần.
- Trong một nhóm A, theo chiều tăng dần của điện tích hạt nhân, tính kim loại tăng dần và tính phi kim giảm dần.
d) Tính acid – base của các oxide và hydroxide
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính base của oxide và hydroxide tương ứng giảm dần, đồng thời tính acid của chúng tăng dần.
3. Bảng tuần hoàn và cấu tạo nguyên tử
Nhận xét:
Số proton = số electron = số hiệu nguyên tử = số Z
Số thứ tự chu kì = số lớp electron
Số thứ tự nhóm A = số electron lớp ngoài cùng
4. Định luật tuần hoàn
Tính chất của các nguyên tố và đơn chất, cũng như thành phần và tính chất của các hợp chất tạo nên từ các nguyên tố đó biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân nguyên tử.
5. Ví dụ luyện tập
Ví dụ 1. Cho các nguyên tố X (Z = 11), Y (Z = 13), T (Z = 14), Q (Z = 19).
a) So sánh tính kim loại
b) So sánh bán kính nguyên tử
Hướng dẫn giải:
X (Z = 11): 1s22s22p63s1 → X thuộc chu kì 3, nhóm IA.
Y (Z = 13): 1s22s22p63s23p1 → Y thuộc chu kì 3, nhóm IIIA.
T (Z = 14): 1s22s22p63s23p2 → T thuộc chu kì 3, nhóm IVA.
Q (Z = 19): 1s22s22p63s23p64s1 → Q thuộc chu kì 4, nhóm IA.
a) So sánh tính kim loại.
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính kim loại giảm dần và tính phi kim tăng dần.
→ Tính kim loại: X > Y > T.
Trong một nhóm A, theo chiều tăng dần của điện tích hạt nhân, tính kim loại tăng dần và tính phi kim giảm dần.
→ Tính kim loại: X < Q.
Vậy, tính kim loại: Q > X > Y > T.
b) So sánh bán kính nguyên tử
Trong một chu kì, bán kính nguyên tử giảm theo chiều tăng dần của điện tích hạt nhân.
→ Bán kính nguyên tử: X > Y > T.
Trong một nhóm A, bán kính nguyên tử tăng theo chiều tăng dần của điện tích hạt nhân.
→ Bán kính nguyên tử: X < Q.
Vậy, bán kính nguyên tử: Q > X > Y > T.
Ví dụ 2. Sulfur (S) là nguyên tố thuộc nhóm VIA, chu kì 3 của bảng tuần hoàn.
a) Viết cấu hình electron của nguyên tử S.
b) Xác định số proton, electron của nguyên tử S.
c) Viết công thức oxide cao nhất và hydroxide cao nhất của S.
Hướng dẫn giải:
a)
Số thứ tự chu kì = số lớp electron = 3.
Số thứ tự nhóm A = số electron lớp ngoài cùng = 6.
→ Cấu hình electron của nguyên tử S: 1s22s22p63s23p4.
b) Số proton = số electron = Z = 16.
c) S thuộc nhóm VIA →Hóa trị cao nhất của S là VI.
Công thức oxide cao nhất của S là SO3 (acidic oxide).
Công thức hydroxide cao nhất là H2SO4 (có tính acid).
B. Trắc nghiệm Hóa học 10 Chương 2: Bảng tuần hoàn các nguyên tố hóa học và định luật tuần hoàn
Câu 1. Cho các nguyên tố X (Z = 11), Y (Z = 13), T (Z = 14), Q (Z = 19). Nguyên tố nào có tính kim loại mạnh nhất?
A. Nguyên tố X.
B. Nguyên tố Y.
C. Nguyên tố T.
D. Nguyên tố Q.
Đáp án: D
Giải thích:
X (Z = 11): 1s22s22p63s1X thuộc chu kì 3, nhóm IA.
Y (Z = 13): 1s22s22p63s23p1Y thuộc chu kì 3, nhóm IIIA.
T (Z = 14): 1s22s22p63s23p2 T thuộc chu kì 3, nhóm IVA.
Q (Z = 19): 1s22s22p63s23p64s1 Q thuộc chu kì 4, nhóm IA.
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính kim loại giảm dần và tính phi kim tăng dần.
Tính kim loại: X > Y > T.
Trong một nhóm A, theo chiều tăng dần của điện tích hạt nhân, tính kim loại tăng dần và tính phi kim giảm dần.
Tính kim loại: X < Q.
Vậy, tính kim loại: Q > X > Y > T.
Nguyên tố Q có tính kim loại mạnh nhất.
Câu 2. Hai nguyên tố A, B đứng kế tiếp nhau trong cùng một chu kì của bảng tuần hoàn và có tổng số đơn vị điện tích hạt nhân là 25, trong đó ZA < ZB. Hai nguyên tố A, B lần lượt là:
A. Mg, Al.
B. Al, Mg.
C. Na, Mg.
D. Mg, Na.
Đáp án: A
Giải thích:
Hai nguyên tố A, B đứng kế tiếp nhau trong cùng một chu kì của bảng tuần hoàn và có tổng số đơn vị điện tích hạt nhân là 25.
Ta có hệ phương trình: 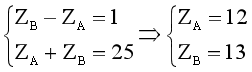 .
.
Hai nguyên tố A, B lần lượt là: Mg (Z = 12); Al (Z = 13).
Câu 3. Nguyên tố X thuộc chu kì 3, nhóm IA. Nguyên tử nguyên tố X có
A. 3 lớp electron và 3 electron ở lớp ngoài cùng.
B. 3 lớp electron và 1 electron ở lớp ngoài cùng.
C. 1 lớp electron và 3 electron ở lớp ngoài cùng.
D. 2 lớp electron và 1 electron ở lớp ngoài cùng.
Đáp án: B
Giải thích:
Số lớp electron = Số thứ tự chu kì = 3
Số electron lớp ngoài cùng = Số thứ tự nhóm A = 1.
Nguyên tử nguyên tố X có 3 lớp electron và 1 electron ở lớp ngoài cùng.
Câu 4. Nguyên tố X thuộc chu kì 3, nhóm VIA. Nguyên tố X là
A. nguyên tố kim loại.
B. nguyên tố phi kim.
C. nguyên tố khí hiếm.
D. nguyên tố phóng xạ.
Đáp án: B
Giải thích:
Số electron lớp ngoài cùng = Số thứ tự nhóm A = 6.
X là nguyên tố phi kim.
Câu 5. Nguyên tố X thuộc chu kì 4, nhóm IIA. X là
A. nguyên tố s.
B. nguyên tố p.
C. nguyên tố d.
D. nguyên tố f.
Đáp án: A
Giải thích:
Số lớp electron = Số thứ tự chu kì = 4.
Số electron lớp ngoài cùng = Số thứ tự nhóm A = 2.
Cấu hình electron của nguyên tử nguyên tố X: 1s22s22p63s23p64s2.
Electron cuối cùng điền vào phân lớp s ® X là nguyên tố s.
Câu 6. Nguyên tử nguyên tố Y có Z = 13. Trong bảng tuần hoàn các nguyên tố hóa học, nguyên tố Y thuộc
A. ô 13, chu kì 3, nhóm IIA.
B. ô 13, chu kì 4, nhóm IIIA.
C. ô 13, chu kì 3, nhóm IIIA.
D. ô 13, chu kì 4, nhóm IIA.
Đáp án: C
Giải thích:
Cấu hình electron của nguyên tử nguyên tố Y: 1s22s22p63s23p1.
Số thứ tự ô = số electron = 13.
Số thứ tự chu kì = Số lớp electron = 3.
Electron cuối cùng điền vào phân lớp p Nguyên tố Y thuộc nhóm A.
Số thứ tự nhóm A = Số electron lớp ngoài cùng = 3.
Nguyên tố Y ở ô 13, chu kì 3, nhóm IIIA.
Câu 7. X là nguyên tố thuộc nhóm A trong bảng tuần hoàn. Oxide cao nhất của X là XO. Phát biểu nào sau đây là đúng?
A. X thuộc nhóm IIIA.
B. X là nguyên tố kim loại.
C. Nguyên tử nguyên tố X có 3 electron ở lớp ngoài cùng.
D. X là nguyên tố phi kim.
Đáp án: B
Giải thích:
Oxide cao nhất của X là XO.
Hóa trị cao nhất của X là II X thuộc nhóm IIA.
Số electron ở lớp ngoài cùng = Số thứ tự nhóm A = 2.
X là nguyên tố kim loại.
Câu 8. Nguyên tử của các nguyên tố thuộc cùng một chu kì có
A. cùng số electron hóa trị.
B. cùng số lớp electron.
C. cùng số electron lớp ngoài cùng.
D. cùng số neutron.
Đáp án: B
Giải thích:
Nguyên tử của các nguyên tố có thuộc cùng một chu kì có cùng số lớp electron.
Số thứ tự chu kì = Số lớp electron.
Câu 9. Nguyên tử các nguyên tố trong cùng một nhóm A có
A. số electron hóa trị bằng nhau.
B. cùng số lớp electron.
C. cùng số neutron.
D. cùng số khối.
Đáp án: A
Giải thích:
Nguyên tử các nguyên tố trong cùng một nhóm A có số electron hóa trị bằng nhau và bằng số thứ tự của nhóm (trừ He).
Câu 10. Trong cùng một chu kì, theo chiều tăng dần của điện tích hạt nhân thì
A. bán kính nguyên tử tăng dần.
B. bán kính nguyên tử giảm dần.
C. bán kính nguyên tử tăng sau đó giảm dần.
D. bán kính nguyên tử giảm sau đó tăng dần.
Đáp án: A
Giải thích:
Trong một chu kì, bán kính nguyên tử giảm theo chiều tăng dần của điện tích hạt nhân.
Trong một nhóm A, bán kính nguyên tử tăng theo chiều tăng dần của điện tích hạt nhân.
Câu 11. Trong một nhóm A, theo chiều tăng dần của điện tích hạt nhân,
A. tính kim loại và tính phi kim tăng dần.
B. tính kim loại và tính phi kim giảm dần.
C. tính kim loại tăng dần và tính phi kim giảm dần.
D. tính kim loại giảm dần và tính phi kim tăng dần.
Đáp án: C
Giải thích:
Trong một nhóm A, theo chiều tăng dần của điện tích hạt nhân, tính kim loại tăng dần và tính phi kim giảm dần.
Chú ý:
Trong một chu kì, theo chiều tăng dần của điện tích hạt nhân, tính kim loại giảm dần và tính phi kim tăng dần.
Câu 12. Sulfur (S) là nguyên tố thuộc nhóm VIA, chu kì 3 của bảng tuần hoàn. Cấu hình electron của nguyên tử S là
A. [Ne] 3s2.
B. [Ne] 3s23p1.
C. [Ne] 3s23p2.
D. [Ne] 3s23p4.
Đáp án: D
Giải thích:
Số thứ tự chu kì = số lớp electron = 3.
Số thứ tự nhóm A = số electron lớp ngoài cùng = 6.
Cấu hình electron của nguyên tử S: 1s22s22p63s23p4 hay [Ne] 3s23p4.
Câu 13. Cho các nguyên tố X (Z = 11), Y (Z = 13), T (Z = 14), Q (Z = 19). So sánh bán kính nguyên tử của các nguyên tố trên theo chiều giảm dần.
A. T > Y > X > Q.
B. Y > X > T > Q.
C. Q > X > Y > T.
D. Q > R > X > Y.
Đáp án: C
Giải thích:
X (Z = 11): 1s22s22p63s1 X thuộc chu kì 3, nhóm IA.
Y (Z = 13): 1s22s22p63s23p1 Y thuộc chu kì 3, nhóm IIIA.
T (Z = 14): 1s22s22p63s23p2 ® T thuộc chu kì 3, nhóm IVA.
Q (Z = 19): 1s22s22p63s23p64s1 ® Q thuộc chu kì 4, nhóm IA.
Trong một chu kì, bán kính nguyên tử giảm theo chiều tăng dần của điện tích hạt nhân.
® Bán kính nguyên tử: X > Y > T.
Trong một nhóm A, bán kính nguyên tử tăng theo chiều tăng dần của điện tích hạt nhân.
® Bán kính nguyên tử: X < Q.
Vậy, bán kính nguyên tử: Q > X > Y > T.
Câu 14. Sulfur (S) là nguyên tố thuộc nhóm VIA, chu kì 3 của bảng tuần hoàn. Oxide cao nhất và hydroxide tương ứng của S là
A. SO2; H2SO3.
B. SO3; H2SO4.
C. SO4; H2SO6.
D. S2O6; H2S2O6.
Đáp án: B
Giải thích:
S thuộc nhóm VIA Hóa trị cao nhất của S là VI.
Công thức oxide cao nhất của S là SO3 (acidic oxide).
Công thức hydroxide cao nhất là H2SO4 (có tính acid).
Câu 15. Hai nguyên tố A, B thuộc cùng một nhóm A và ở hai chu kì kế tiếp nhau trong bảng tuần hoàn. Tổng số đơn vị điện tích hạt nhân của A và B là 30, trong đó ZA < ZB. Phát biểu nào sau đây không đúng?
A. Hai nguyên tố A, B thuộc cùng nhóm IA.
B. A, B đều là nguyên tố kim loại.
C. Nguyên tố A thuộc chu kì 3, nguyên tố B thuộc chu kì 4.
D. Tính kim loại của A lớn hơn B.
Đáp án: D
Giải thích:
Ta có hệ phương trình: 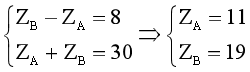 .
.
Nguyên tố A là Na (Z = 11); nguyên tố B là K (Z = 19).
Cấu hình electron của nguyên tử Na (Z = 11): [Ne]3s1.
Nguyên tố Na ở ô 11, chu kì 3, nhóm IA.
Cấu hình electron của nguyên tử K (Z = 19): [Ar]4s1.
Nguyên tố K ở ô 19, chu kì 4, nhóm IA.
Nhận xét:
Nguyên tố A, B đều là nguyên tố kim loại.
Tính kim loại: K > Na.
Phát biểu không đúng: Tính kim loại của A lớn hơn B.
Bài giảng Hóa học 10 Bài 9: Ôn tập chương 2 - Kết nối tri thức