30 câu Trắc nghiệm KHTN 8 (Cánh diều 2024) Bài 7: Tốc độ phản ứng và chất xúc tác có đáp án
Bộ 30 câu hỏi trắc nghiệm Bài 7: Tốc độ phản ứng và chất xúc tác môn KHTN 8 đầy đủ các mức độ sách Khoa học tự nhiên 8 (có đáp án) Cánh diều giúp học sinh ôn luyện trắc nghiệm KHTN 8 Bài 7.
Nội dung bài viết
Xem thêm »
Trắc nghiệm KHTN 8 Bài 7: Tốc độ phản ứng và chất xúc tác
Phần 1: 15 câu Trắc nghiệm KHTN 8 Bài 7: Tốc độ phản ứng và chất xúc tác
Câu 1. Khi cho cùng một lượng nhôm (aluminium) vào cốc đựng dung dịch acid HCl 0,1M, tốc độ phản ứng sẽ lớn nhất khi dùng nhôm ở dạng nào sau đây?
A.Dạng viên nhỏ.
B. Dạng bột mịn, khuấy đều.
C.Dạng tấm mỏng.
D.Dạng nhôm dây.
Đáp án đúng là: B
Tốc độ phản ứng sẽ lớn nhất khi dùng nhôm ở dạng bột mịn, khuấy đều vì lúc này sẽ tăng diện tích bề mặt tiếp xúc của nhôm và phân tử HCl.
Câu 2. Yếu tố nào dưới đây được sử dụng để làm tăng tốc độ phản ứng khi rắc men vào tinh bột đã được nấu chín để lên men rượu?
A. Chất xúc tác.
B.Chất ức chế.
C. Nồng độ.
D. Nhiệt độ.
Đáp án đúng là: A
Men là chất xúc tác được thêm vào để tăng tốc độ phản ứng chuyển hóa tinh bột thành rượu.
Câu 3.Cho các quá trìn biến đổi:
(a) Thực phẩm bảo quản trong tủ lạnh sẽ giữ được lâu hơn.
(b) Bệnh nhân sẽ dễ hô hấp hơn khi dùng oxygen từ bình chứa khí oxygen so với từ không khí.
Những yếu tố nào ảnh hưởng đến tốc độ của các quá trình biến đổi trên.
A. Nhiệt độ, nồng độ.
B. Nhiệt độ, xúc tác.
C.Nhiệt độ, diện tích bề mặt tiếp xúc.
D.Nồng độ, xúc tác.
Đáp án đúng là: A
(a) Thực phẩm bảo quản trong tủ lạnh sẽ giữ được lâu hơn ⇒ Ảnh hưởng của nhiệt độ đến tốc độ phản ứng.
(b) Bệnh nhân sẽ dễ hô hấp hơn khi dùng oxygen từ bình chứa khí oxygen so với từ không khí ⇒ Ảnh hưởng của nồng độ đến tốc độ phản ứng.
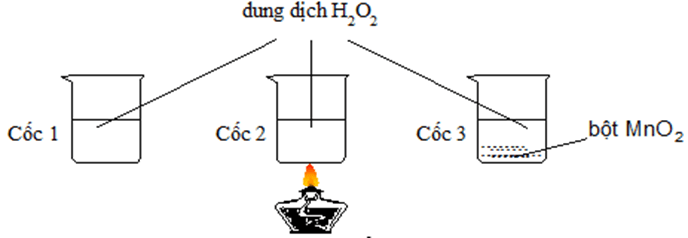
Câu 4. Có 3 cốc chứa 20ml dung dịch H2O2 cùng nồng độ. Tiến hành 3 thí nghiệm như hình vẽ sau.
Ở thí nghiệm nào có bọt khí thoát ra chậm nhất?
A.Thí nghiệm 2.
B. Thí nghiệm 3.
C.Thí nghiệm 1.
D.3 thí nghiệm như nhau.
Đáp án đúng là: C
TN2: sử dụng yếu tố nhiệt độ, TN3: sử dụng xúc tác MnO2.
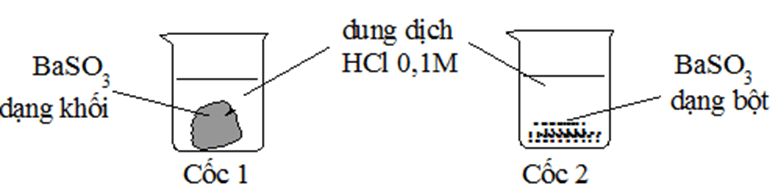
Câu 5. Cho 2 mẫu BaSO3 có khối lượng bằng nhau và 2 cốc chứa 50ml dung dịch HCl 0,1M như hình sau. Hỏi ở cốc nào mẫu BaSO3 tan nhanh hơn?
A.Cốc 1 tan nhanh hơn.
B. Cốc 2 tan nhanh hơn.
C.Tốc độ tan ở 2 cốc như nhau.
D.BaSO3 tan nhanh nên không quan sát được.
Đáp án đúng là: B
Sử dụng yếu tố diện tích tiếp xúc, Cốc 2: BaSO3 dạng bột sẽ làm tăng diện tích bề mặt tiếp xúc, tốc độ phản ứng xảy ra nhanh hơn.
Câu 6. Khi tăng nhiệt độ, hầu hết phản ứng diễn ra với tốc độ?
A. giảm xuống.
B. tăng lên.
C. lúc tăng lúc giảm.
D. không đổi.
Đáp án đúng là: B
Khi tăng nhiệt độ, hầu hết phản ứng diễn ra với tốc độ tăng lên.
Câu 7.“Diện tích bề mặt tiếp xúc của …..càng lớn, tốc độ phản ứng càng nhanh”. Cụm từ còn thiếu trong phát biểu trên là
A. chất lỏng.
B.chất rắn.
C. chất khí.
D. chất tan.
Đáp án đúng là: B
Diện tích bề mặt tiếp xúc của chất rắncàng lớn, tốc độ phản ứng càng nhanh.
Câu 8. Chất xúc tác là chất:
A. làm tăng tốc độ phản ứng không bị thay đổi cả về (chất và lượng) sau phản ứng.
B. làm giảm tốc độ phản ứng không bị thay đổi cả về (chất và lượng) sau phản ứng.
C. làm tăng tốc độ phản ứng bị thay đổi cả về (chất và lượng) sau phản ứng.
D. làm giảm tốc độ phản ứng bị thay đổi cả về (chất và lượng) sau phản ứng.
Đáp án đúng là: A
Chất xúc tác là chất làm tăng tốc độ phản ứng không bị thay đổi cả về (chất và lượng) sau phản ứng.
Câu 9. Các phản ứng khác nhau thì:
A. tốc độ phản ứng khác nhau.
B.tốc độ phản ứng vẫn giống nhau.
C.tốc độ phản ứng khác nhau không đáng kể.
D. tốc độ phản ứng chỉ khác nhau khi có chất khí tham gia.
Đáp án đúng là: A
Các phản ứng khác nhau thìtốc độ phản ứng khác nhau.
Câu 10. Để xác định được mức độ phản ứng nhanh hay chậm người ta sử dụng khái niệm nào sau đây?
A. Tốc độ phản ứng.
B. Độ tan.
C. Nồng độ phần trăm các chất trong dung dịch.
D. Tỉ khối của chất khí.
Đáp án đúng là: A
Để xác định được mức độ phản ứng nhanh hay chậm người ta sử dụng khái niệm tốc độ phản ứng.
Câu 11. “Các chất bảo quản là loại ….được sử dụng trong thực phẩm để ngăn ngừa sự thối rữa hay hư hỏng”. Cụm từ phù hợp nhất điền vào chỗ trống là
A.chất ức chế.
B. chất xúc tác.
C. chất tan trong dung dịch.
D. chất không tan trong dung dịch.
Đáp án đúng là: A
Các chất bảo quản là loại chất ức chế được sử dụng trong thực phẩm để ngăn ngừa sự thối rữa hay hư hỏng.
Câu 12. Khi giảm nồng độ của một chất tham gia phản ứng, phản ứng diễn ra với tốc độ?
A. tăng lên.
B.giảm xuống.
C. lúc tăng lúc giảm.
D. không đổi.
Đáp án đúng là: B
Khi giảm nồng độ của một chất tham gia phản ứng, phản ứng diễn ra với tốc độ giảm xuống.
Câu 13. Nung đá vôi ở nhiệt độ cao hơn để sản xuất vôi sống. Người ta đã lợi dụng yếu tố nào để tăng tốc độ phản ứng trên?
A. Chất ức chế.
B. Chất xúc tác.
C. Nồng độ.
D.Nhiệt độ.
Đáp án đúng là: D
Người ta lợi dụng việc tăng nhiệt độ để tăng tốc độ của phản ứng nung đá vôi.
Câu 14. Tốc độ phản ứng không phụ thuộc yếu tố nào sau đây?
A. Nồng độ các chất tham gia phản ứng.
B. Bề mặt tiếp xúc giữa các chất phản ứng.
C.Thời gian xảy ra phản ứng.
D.Chất xúc tác.
Đáp án đúng là: C
Tốc độ phản ứng không phụ thuộc vào thời gian xảy ra phản ứng.
Câu 15. Trong hàn xì, để phản ứng đốt cháy acetylene xảy ra nhanh và cho nhiệt độ cao hơn, người ta dùng
A.oxygen trong không khí.
B. hỗn hợp khí oxygen và carbon dioxide.
C.hỗn hợp khí oxygen và khí nitrogen.
D.oxygen nguyên chất.
Đáp án đúng là: D
Để phản ứng đốt cháy acetylene xảy ra nhanh và cho nhiệt độ cao hơn, người ta dùng oxygen nguyên chất.
Phần 2: Lý thuyết KHTN 8 Bài 7: Tốc độ phản ứng và chất xúc tác
I. Tốc độ phản ứng hoá học là gì?
Phản ứng hoá học xảy ra với những tốc độ rất khác nhau, có phản ứng xảy ra rất nhanh nhưng cũng có phản ứng xảy ra rất chậm.
Ví dụ: Phản ứng đốt cháy cồn xảy ra nhanh hơn rất nhiều so với sự gỉ sắt.
|
|
|
|
Sự cháy của cồn |
Sự gỉ sắt |
Tốc độ phản ứng là đại lượng chỉ mức độ nhanh hay chậm của một phản ứng hoá học.
II. Các yếu tố ảnh hưởng đến tốc độ của một phản ứng hoá học
Tốc độ của phản ứng hoá học phụ thuộc vào nhiều yếu tố khác nhau. Các yếu tố ảnh hưởng đến tốc độ của một phản ứng hoá học có thể là: diện tích bề mặt tiếp xúc, nhiệt độ, nồng độ, sự có mặt của chất xúc tác, chất ức chế.
1. Ảnh hưởng của diện tích bề mặt tiếp xúc
Nếu chia một vật thành nhiều phần nhỏ hơn thì tổng diện tích bề mặt sẽ tăng lên. Diện tích bề mặt tiếp xúc càng lớn, tốc độ phản ứng càng nhanh.
Ví dụ:
- Nấu cháo từ bột gạo sẽ nhanh hơn nấu cháo từ hạt gạo.
- Thanh củi được chẻ nhỏ sẽ cháy nhanh hơn thanh củi to.
Kết luận: Diện tích bề mặt tiếp xúc có ảnh hưởng đến tốc độ của phản ứng hoá học. Diện tích bề mặt tiếp xúc càng lớn, tốc độ phản ứng càng nhanh.
2. Ảnh hưởng của nhiệt độ
Nhiệt độ có ảnh hưởng đến tốc độ của phản ứng hoá học. Khi tăng nhiệt độ, phản ứng diễn ra với tốc độ nhanh hơn.
Ví dụ:
Ở điều kiện nhiệt độ phòng, vi khuẩn trong sữa có thể thực hiện nhiều phản ứng hoá học khác nhau làm cho sữa nhanh chóng bị hỏng. Để giảm thiểu điều này, chúng ta thường bảo quản sữa cũng như các thực phẩm khác trong tủ lạnh để giữ chúng được lâu hơn.
3. Ảnh hưởng của nồng độ
Nồng độ có ảnh hưởng đến tốc độ của phản ứng hoá học. Nồng độ các chất phản ứng càng cao, tốc độ phản ứng càng nhanh.
4. Chất xúc tác và chất ức chế
Chất xúc tác là chất làm tăng tốc độ phản ứng nhưng không bị thay đổi cả về lượng và chất sau phản ứng.
Đôi khi việc kiểm soát để phản ứng xảy ra chậm lại cũng rất cần thiết. Chất được sử dụng để làm giảm tốc độ phản ứng được gọi là chất ức chế. Các chất bảo quản là một loại chất ức chế được sử dụng trong thực phẩm để ngăn ngừa hoặc làm chậm lại sự thối rữa, hư hỏng gây ra bởi sự phát triển của các vi sinh vật hay do các thay đổi không mong muốn về mặt hoá học.