Lý thuyết KHTN 8 ( Cánh diều 2024) Bài 5: Tính theo phương trình hóa học
Tóm tắt lý thuyết Bài 5: Tính theo phương trình hóa học sách Khoa học tự nhiên 8 Cánh diều ngắn gọn, chính xác sẽ giúp học sinh nắm vững kiến thức trọng tâm, ôn luyện để học tốt KHTN 8.
Nội dung bài viết
--
Video bài giảng KHTN 8 Bài 5: Tính theo phương trình hóa học - Cánh diều
Khoa học tự nhiên 8 Bài 5: Tính theo phương trình hóa học
A. Lý thuyết KHTN 8 Bài 5: Tính theo phương trình hóa học
I. Xác định khối lượng, số mol của chất phản ứng và sản phẩm phản ứng hoá học
Để tính khối lượng và số mol của chất phản ứng và chất sản phẩm trong một phản ứng hoá học, ta thực hiện theo các bước sau:
Bước 1: Viết phương trình hoá học của phản ứng.
Bước 2: Tính số mol chất đã biết dựa vào khối lượng hoặc thể tích.
Bước 3: Dựa vào phương trình hoá học và số mol chất đã biết để tìm số mol chất tham gia phản ứng hoặc sản phẩm.
Bước 4: Tính khối lượng hoặc thể tích của chất cần tìm.
II. Hiệu suất phản ứng
1. Chất phản ứng hết, chất phản ứng dư
- Chất phản ứng hết là chất không còn sau khi phản ứng kết thúc.
- Chất phản ứng dư là chất còn lại sau khi kết thúc phản ứng.
- Lượng chất sản phẩm tạo thành được tính theo chất phản ứng hết.
2. Hiệu suất phản ứng
Hiệu suất phản ứng (kí hiệu là H) là tỉ số giữa lượng sản phẩm thu được theo thực tế và lượng sản phẩm thu được theo lý thuyết.
Thông thường, hiệu suất phản ứng biểu thị theo phần trăm và được tính theo biểu thức:
H=mtt×100mlt(%)H=mtt×100mlt(%)
Trong đó:
mtt là khối lượng chất (g) thu được theo thực tế.
mlt là khối lượng chất (g) thu được theo lí thuyết (tính theo phương trình).
H là hiệu suất phản ứng (%).
Hiệu suất phản ứng thường nhỏ hơn 100%. Nếu hiệu suất phản ứng là 100% tức là phản ứng hoá học xảy ra hoàn toàn.
B. Bài tập trắc nghiệm KHTN 8 Bài 5: Tính theo phương trình hóa học
Câu 1: Cho sơ đồ phản ứng sau:
Al + HCl-→−→ AlCl3 + H2
Sau phản ứng thu được 7,437 lít (đkc) khí hydrogen thì số mol của Al đã tham gia phản ứng là
A. 0,3 mol.
B. 0,2 mol.
C. 0,1 mol.
D. 0,15 mol.
Đáp án đúng là: B
Số mol khí hydrogen là: nH2=7,43724,79=0,3(mol)nH2=7,43724,79=0,3(mol)
PTHH:2Al + 6HCl → 2AlCl3 + 3H2
Tỉ lệ phản ứng:23
Đề bài:0,2←0,3(mol)
Số mol của Al đã tham gia phản ứng là 0,2 mol.
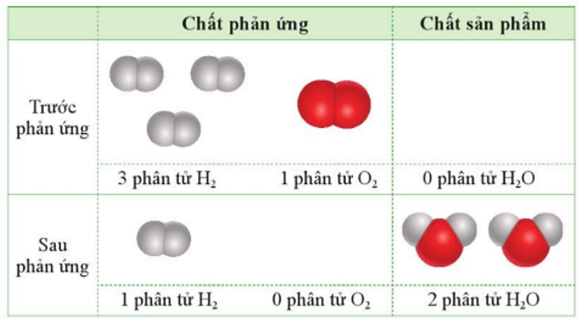
Câu 2: Cho 3 phân tử H2 tác dụng với 1 phân tử O2 (trong điều kiện thích hợp):
Chọn phát biểu đúng trong những phát biểu dưới đây?
A. Sau khi phản ứng xảy ra hoàn toàn, chỉ thu được 2 phân tử nước, không còn phân tử H2 và O2.
B. Sau khi phản ứng xảy ra hoàn toàn, thu được 2 phân tử nước và còn 1 phân tử H2 dư.
C. Sau khi phản ứng xảy ra hoàn toàn, thu được 2 phân tử nước và còn 1 phân tử O2 dư.
D. Sau khi phản ứng xảy ra hoàn toàn, thu được 1 phân tử nước và còn 1 phân tử H2 dư.
Đáp án đúng là: B
Phát biểu đúng là “Sau khi phản ứng xảy ra hoàn toàn, thu được 2 phân tử nước và còn 1 phân tử H2 dư”.
Câu 3: Một nhà máy dự tính sản xuất 80 tấn vôi sống CaO từ đá vôi. Tuy nhiên, khi đưa vào quy trình sản xuất thực tế chỉ thu được 25 tấn CaO. Hiệu suất của quá trình nói trên là
A. 25,0% gam.
B. 31,25%.
C. 32,0%.
D. 30,5 %.
Đáp án đúng là: B
Hiệu suất phản ứng là H=mCaO ttmCaO lt×100%=2580×100%=31,25%H=mCaOttmCaOlt×100%=2580×100%=31,25%
Câu 4: Đốt 32,0 gam sulfur trong khí oxygen dư, tính khối lượng SO2 thu được nếu hiệu suất phản ứng đạt 80%.
A. 64 gam.
B. 80 gam.
C. 51,2 gam.
D. 52,1 gam.
Đáp án đúng là: C
Số mol sulfur tham gia phản ứng là: 80100×32=25,6 (g)80100×32=25,6(g)
PTHH:S + O2 → SO2
Tỉ lệ phản ứng:11
Đề bài:0,8 →0,8 (mol)
Vậy khối lượng SO2 thu được là: 0,8 ×64 = 51,2 (gam).
Câu 5: Cho hỗn hợp X (chứa 2,3 gam sodium và 1,95 gam potassium) tác dụng hết với nước, thu được khí hydrogen và dung dịch chứa NaOH và KOH. Thể tích khí hydrogen thu được (đkc) là
A. 3,7185 lít.
B. 1,85925 lít.
C. 1,7353 lít.
D. 2,6848 lít.
Đáp án đúng là: C
|
2Na+ 2H2Ot0→t0→ 2NaOH+H2 |
||
|
Tỉ lệ phản ứng: |
21 |
(mol) |
|
Phản ứng: |
0,1→→0,05 |
(mol) |
|
2K+2H2O t0→t0→ 2KOH+H2 |
||
|
Tỉ lệ phản ứng: |
21 |
(mol) |
|
Phản ứng: |
0,05→→0,025 |
(mol) |
⇒nH2=0,05+0,025=0,075(mol)⇒nH2=0,05+0,025=0,075(mol)⇒VH2=nO2.24,79=0,075.24,79=1,85925(lit)⇒VH2=nO2.24,79=0,075.24,79=1,85925(lit)
Câu 6: Cho kim loại sắt tác dụng với dung dịch H2SO4 loãng, thu được FeSO4 và khí hydrogen. Nếu dùng 5,6 gam sắt thì số mol H2SO4 cần để phản ứng là bao nhiêu?
A. 0,1 mol.
B. 1 mol.
C. 0,2 mol.
D. 0,3 mol.
Đáp án đúng là: A
Số mol sắt là: nFe=5,656=0,1(mol).nFe=5,656=0,1(mol).
PTHH: Fe + H2SO4 → FeSO4 + H2
Tỉ lệ phản ứng:1 →1
Đề bài:0,1 →0,1(mol)
Vậy số mol H2SO4 cần dùng là 0,1 (mol).
Câu 7: Cho sơ đồ phản ứng sau:
Zn + HCl ZnCl2 + H2
Sau phản ứng thu được 7,437 lít (đkc) khí hydrogen thì khối lượng của Zn đã tham gia phản ứng là
A. 13,0 gam.
B. 15,9 gam.
C. 19,5 gam.
D. 26,0 gam.
Đáp án đúng là: C
Số mol H2 thu được là: nH2=7,43724,79=0,3(mol)nH2=7,43724,79=0,3(mol)
Số mol H2 thu được là:
PTHH: Zn + 2HCl →ZnCl2 + H2
Tỉ lệ phản ứng:11
Đề bài:0,3←0,3 (mol)
Vậy khối lượng của Zn là 0,3×65 = 19,5 gam.
Câu 8: Cho phương trình hóa học sau:
2KMnO4to→K2MnO4+MnO2+O2↑.2KMnO4to→K2MnO4+MnO2+O2↑⏐⏐.
Thể tích khí O2 (đkc) thu được khi nhiệt phân hoàn toàn 1 mol KMnO4 là
A. 24,79 lít.
B. 12,395 lít.
C. 49,58 lít.
D. 11,2 lít.
Đáp án đúng là: B
PTHH: 2KMnO4to→K2MnO4+MnO2+O2↑.2KMnO4to→K2MnO4+MnO2+O2↑⏐⏐.
Tỉ lệ phản ứng:21
Đề bài:1←0,5(mol).
Số mol oxygen thu được là 0,5 mol
Thể tích khí O2 (đkc) thu được là: 0,5.24,79 = 12,395 (lít).
Câu 9: Cho phương trình hóa học sau:
2Fe+ 3Cl2t0→ 2FeCl3.2Fe+3Cl2t0→2FeCl3.
Số mol Fe cần dùng để điều chế được 2 mol iron(III) chloride là
A. 2 mol.
B. 3 mol.
C. 1 mol.
D. 1,5 mol.
Đáp án đúng là: A
PTHH: 2Fe+ 3Cl2t0→ 2FeCl3
Tỉ lệ phản ứng: 22
Đề bài: 2←2(mol)
Vậy số mol Fe cần dùng là 2 mol.
Câu 10: Nếu đốt 12,0 gam carbon trong khí oxygen dư thu được 39,6 gam CO2 thì hiệu suất phản ứng là
A. 80%.
B. 85%.
C. 95%.
D. 90%..
Đáp án đúng là: D
PTHH: C + O2 → CO2
Tỉ lệ phản ứng:11
Đề bài:0,9←0,9(mol)
Hiệu suất phản ứng là H=nC ttnC lt×100%=0,91×100%=90%
Câu 11: Trộn 4 gam bột sulfur với 14 gam bột sắt rồi nung nóng trong điều kiện không có không khí. Khối lượng FeS thu được sau phản ứng là
A. 18 gam.
B. 11,0 gam.
C. 16 gam.
D. 13 gam.
Đáp án đúng là: B
|
nS=mM=432=0,125(mol) |
nFe=mM=1456=0,25(mol) |
|
|
Fe+S t0→FeS |
||
|
Tỉ lệ phản ứng: |
111 |
(mol) |
|
Đề bài: |
0,250,125 |
(mol) |
|
Tỉ lệ: |
0,251 > 0,1251 |
|
|
Fe dưS hết |
||
|
Phản ứng: |
0,125 →0,125 |
(mol) |
mFeS = n.M = 0,125.88 = 11,0 (g)
Câu 12: Một nhà máy dự tính sản xuất 100 tấn NH3 từ N2 và H2 trong điều kiện thích hợp. Tuy nhiên, khi đưa vào quy trình sản xuất thực tế chỉ thu được 25 tấn NH3. Hiệu suất của phản ứng sản xuất NH3 nói trên là
A. 4,0% gam.
B. 25,0%.
C. 40%.
D. 2,5 %.
Đáp án đúng là: B
Hiệu suất phản ứng là H=mNH3 ttmNH3 lt×100%=25100×100%=25%
Câu 13: Đốt cháy hoàn toàn 7,5 gam than đá (biết than đá có thành phần chính là carbon, chứa 4% tạp chất không cháy) thu được CO2. Thể tích khí oxi cần dùng (đkc) để đốt cháy hết lượng than đá trên là
A. 15,29 lít.
B. 67,2 lít.
C. 33,6 lít.
D. 14,874 lít.
Đáp án đúng là: D
Khối lượng carbon nguyên chất trong 7,5 gam than đá là:
mC = 7,5.100−4100=7,2(gam)
|
C + O2 → CO2 |
||
|
Tỉ lệ phản ứng: |
1 1 |
(mol) |
|
Phản ứng: |
0,6 → 0,6 |
(mol) |
⇒VO2=nO2.24,79=14,874(lit)
Câu 14: Cho phương trình hóa học nhiệt phân muối calcium carbonate:
Số mol CaCO3 cần dùng để điều chế được 0,2 mol CaO là
A. 0,2 mol.
B. 0,3 mol.
C. 0,4 mol.
D. 0,1 mol.
Đáp án đúng là: A
PTHH: CaCO3to→CaO+CO2.
Tỉ lệ phản ứng:11
Đề bài:0,2←0,2(mol)
Vậy số mol CaCO3 cần dùng để điều chế được 0,2 mol CaO là 0,2 mol.