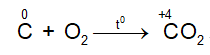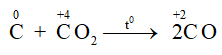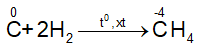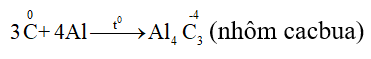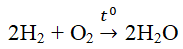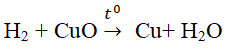C ra C2H2 l C + H2 → C2H2 | Cacbon ra Axetilen
Sinx.edu.vn xin giới thiệu phương trình C + H2 → C2H2 là phản ứng oxi hóa khử. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng C + H2 → C2H2
1. Phương trình điều chế C2H2 từ C và H2
C + H2 C2H2
2. Điều kiện phương trình phản ứng xảy ra
Điều kiện: Nhiệt độ 1500 - 2000°C
3. Hiện tượng nhận biết phản ứng.
Phương trình không có hiện tượng nhận biết đặc biệt.
Trong trường hợp này, bạn chỉ thường phải quan sát chất sản phẩm C2H2 (Axetilen), được sinh ra
Hoặc bạn phải quan sát chất tham gia C (cacbon), H2 (hidro), biến mất.
4. Bản chất của các chất tham gia phản ứng
4.1. Bản chất của C (Cacbon)
Trong phản ứng trên C là chất oxi hoá.
C thể hiện tính oxi hoá khi tác dụng với hidro, kim loại...
4.2. Bản chất của H2 (Hidro)
Trong phản ứng trên H2 là chất khử.
Hidro có thể phản ứng với phi kim ở nhiệt độ cao.
5. Cách thực hiện phản ứng
- Cho C (cacbon) tác dụng H2 (hidro) ở nhiệt độ 1500 - 2000°C và tạo ra chất C2H2 (Axetilen)
6. Tính chất hóa học của C
- Trong các dạng tồn tại của C, C vô định hình hoạt động hơn cả về mặt hóa học.
- Trong các phản ứng hóa học C thể hiện hai tính chất: Tính oxi hóa và tính khử. Tuy nhiên tính khử vẫn là chủ yếu của C.
6.1. Tính khử
- Tác dụng với oxi
Ở nhiệt độ cao C lại khử CO2 theo phản ứng:
- Tác dụng với oxit kim loại:
+ C khử được oxit của các kim loại đứng sau Al trong dãy hoạt động hóa học của kim loại:
CuO + C → Cu + CO (tº)
Fe2O3 + 3C → 2Fe + 3CO (tº)
+ Với CaO và Al2O3:
CaO + 3C → CaC2 + CO (trong lò điện)
2Al2O3 + 9C → Al4C3 + 6CO (2000ºC)
- Tác dụng với các chất oxi hóa mạnh thường gặp H2SO4 đặc, HNO3, KNO3, KClO3, K2Cr2O7, ... trong các phản ứng này, C bị oxi hóa đến mức +4 (CO2).
C + 2H2SO4 đặc → CO2 + 2SO2 + 2H2O (tº)
C + 4HNO3 đặc → CO2 + 4NO2 + 2H2O (tº)
C + 4KNO3 → 2K2O + CO2 + 4NO2 (tº)
- Khi nhiệt độ cao, C tác dụng được với hơi nước:
C + H2O → CO + H2 (1000ºC)
C + 2H2O → CO2 + 2H2
6.2. Tính oxi hóa
- Tác dụng với hidro
- Tác dụng với kim loại
7. Tính chất hóa học của Hidro (H2)
Hiđro là phi kim có tính khử. Ở những nhiệt độ thích hợp, hiđro không những kết hợp được với đơn chất oxi mà còn kết hợp được với nguyên tố oxi trong một số oxit kim loại. Các phản ứng này đều tỏa nhiều nhiệt. Cụ thể:
- Hiđro tác dụng với oxi
Hiđro cháy trong oxi theo phương trình hóa học:
Hỗn hợp H2 và O2 là hổn hợp nổ. Hỗn hợp nổ mạnh nhất khi tỉ lệ H2 : O2 là 2:1 về thể tích.
- Hiđro tác dụng với một số oxit kim loại như FeO, CuO, Fe2O3, …
Ví dụ:
Hiđro phản ứng với đồng oxit ở nhiệt độ khoảng 400°C theo phương trình hóa học:
8. Ứng dụng của C
- Các mảnh kim cương hoặc bột màu đen ở vành ô tô hoặc mực máy in, tản nhiệt ở các thiết bị điện tử... Đặc biệt kim cương được dùng làm đồ trang sức quý hiếm.
- Than chì là một dạng carbon khác đã được sử dụng cho nồi nấu kim loại ở nhiệt độ cao, điện cực đèn hồ quang, tế bào khô hoặc cho đầu bút chì, các vật liệu có khả năng chịu lửa, chất bôi trơn...
- Có một trạng thái vô định hình khác của cacbon được sử dụng ở dạng chất tẩy trắng và chất hấp thụ khí, than hoạt tính làm mặt nạ phòng hơi độc…
- Than đá, than gỗ… được sử dụng làm chất đốt trong công nghiệp hay điều chế một số kim loại…
- Cacbon-14, có tính phóng xạ, là đồng vị được sử dụng trong việc xác định niên đại bằng carbon phóng xạ và dán nhãn phóng xạ.
- Các hợp chất của cacbon có nhiều công dụng như:
+ Sử dụng carbon dioxide và bình chữa cháy.
+ Đá khô là dạng rắn của cacbon.
+ Carbon monoxide rất hữu ích cho việc khử trong một số quy trình luyện kim.
+ Sản xuất dung môi trong công nghiệp, carbon disulphide và carbon tetrachloride là một số nguyên liệu đáng chú ý.
9. Bạn có biết
- Hiện tại chúng tôi không có thêm bất kỳ thông tin nào thêm về phương trình này.
10. Bài tập vận dụng
Câu 1. Tính chất vật lý của axetilen là
A. chất khí không màu, không mùi, ít tan trong nước, nặng hơn không khí.
B. chất khí không màu, không mùi, ít tan trong nước, nhẹ hơn không khí.
C. chất khí không màu, không mùi, tan tốt trong nước, nhẹ hơn không khí .
D. chất khí không màu, mùi hắc, ít tan trong nước, nặng hơn không khí.
Lời giải:
Đáp án: B
Câu 2. Khí X có tỉ khối đối với oxi là 0,8125. Khí X là
A. C2H2.
B. C2H4.
C. C2H6.
D. CH4.
Lời giải:
Đáp án: A
Câu 3. Khí axetilen không có tính chất hóa học nào sau đây?
A. Phản ứng cộng với dung dịch brom.
B. Phản ứng cháy với oxi.
C. Phản ứng cộng với hiđro.
D. Phản ứng thế với clo ngoài ánh sáng.
Lời giải:
Đáp án: D
Câu 4. Trong phân tử axetilen, giữa hai nguyên tử cacbon có
A. một liên kết đơn.
B. một liên kết đôi
C. một liên kết ba.
D. hai liên kết đôi.
Lời giải:
Đáp án: C
Câu 5. Hãy cho biết trong các chất sau: C2H4, C3H4, C2H6, C2H2 có bao nhiêu chất làm mất màu dung dịch brom?
A. 1
B. 2
C. 3
D. 4
Lời giải:
Đáp án: C