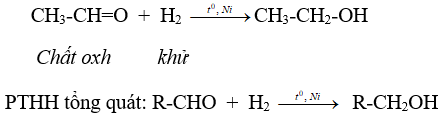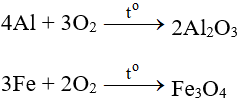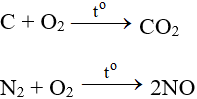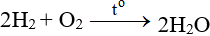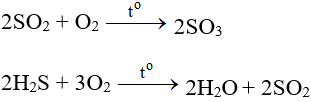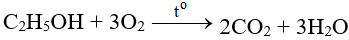CH3CHO ra CH3COOH l CH3CHO + O2 → CH3COOH | Andehit axetic ra Axit axetic
Sinx.edu.vn xin giới thiệu phương trình CH3CHO + O2 → CH3COOH là phản ứng oxi hóa khử. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng CH3CHO + O2 → CH3COOH
1. Phản ứng oxi hóa không hoàn toàn anđehit axetic
CH3CHO + O2 CH3COOH
2. Điều kiện để phản ứng CH3CHO ra CH3COOH
Nhiệt độ, xúc tác: ion Mn2+
3. Hiện tượng nhận biết phản ứng.
Chất khí hóa lỏng
4. Cách thực hiện phản ứng
Andehit bị oxi hóa bởi oxi
5. Bản chất của các chất tham gia phản ứng
5.1. Bản chất của CH3CHO (Andehit axetic)
- Trong phản ứng trên CH3CHO là chất khử.
- Với xúc tác và nhiệt độ thích hợp, CH3CHO phản ứng oxi hóa không hoàn toàn với O2 cho ra axit axetic CH3COOH.
5.2. Bản chất của O2 (Oxi)
Trong phản ứng trên O2 là chất oxi hoá.
6. Mở rộng các phương pháp điều chế Axit axetic CH3COOH
6.1. Cacbonyl hóa methanol
Methanol tác dụng với cacbon monoxit tạo thành axit axetic:
CH3OH + CO → CH3COOH
Quá trình liên quan đến chất trung gian iodometan, xúc tác là phức chất kim loại với 3 bước sau:
CH3OH + HI → CH3I + H2O
CH3I + CO → CH3COI
CH3COI + H2O → CH3COOH + HI
6.2. Oxy hóa axetaldehit
Trong công nghiệp, Axit axetic CH3COOH được sản xuất từ butan C4H10 có xúc tác và nhiệt độ
2C4H10+ 3O2→ 4CH3COOH + 2H2O
6.3. Phương pháp lên men trong điều kiện hiếu khí
Phương pháp lên men chậm
Cho axit axetic CH3COOH vào thùng gỗ sồi thể tích 250- 300l, trống 1/5 thể tích lượng axit axetic rồi đổ thêm nước ép nho vào đến khi được 1/2 thùng.
Tiến hành lên men ở nhiệt độ thường. Quá trình kéo dài vài tuần. Kiểm tra rượu còn 0.3- 0.5% thì lấy giấm ra, bổ sung thêm dinh dưỡng mới vì nếu để lâu, chất lượng giấm sẽ giảm.
7. Tính chất hóa học của Andehit
7.1. Phản ứng cộng hiđro
7.2. Phản ứng oxi hóa không hoàn toàn
HCHO + 2AgNO3 + H2O + 3NH3 −tº→ H-COONH4 + 2NH4NO3 + 2Ag
TQ: R-CH=O + 2AgNO3 + H2O + 3NH3 −tº→ R-COONH4 + 2NH4NO3 + 2Ag
Pư trên còn được gọi là pư tráng bạc.
Hay: 2CH3-CH=O + O2 −tº, xt→ 2CH3-COOH
2R-CHO + O2 −tº, xt→ 2R-COOH
Nhận xét: Anđehit vừa thể hiện tính oxi hóa vừa thể hiện tính khử.
7.3. Tác dụng với brom và kali pemanganat
Anđehit rất dễ bị oxi hoá, nó làm mất màu nước brom, dung dịch kali pemanganat và bị oxi hoá thành axit cacboxylic, thí dụ :
RCH=O + Br2 + H2O → R-COOH + 2HBr
* Chú ý : Đối với HCHO phản ứng xảy ra như sau :
HCH=O + 2Br2 + H2O → CO2 + 4HBr
8. Tính chất vật lí của Andehit
Trạng thái tồn tại: Ở điều kiện thường, các anđehit dãy đồng đẳng tồn tại dưới dạng chất khí (HCHO sôi ở -19 độ C và CH3CHO sôi ở nhiệt độ 21 độ C), tan rất tốt trong nước. Các anđehit tiếp theo là chất lỏng hoặc rắn, độ tan trong nước giảm dần theo chiều tăng của phân tử khối.
Nhiệt độ sôi: Nhiệt độ sôi của Anđehit thấp hơn Ancol cùng khối lượng do không có liên kết hidro trong phân tử và cao hơn hidrocacbon có cùng số nguyên tử C.
Dung dịch nước của anđehit fomic là fomon.
Dung dịch bão hòa của anđehit fomic nồng độ 37 - 40% là fomalin.
9. Tính chất hóa học của O2
Khi tham gia phản ứng, nguyên tử O dễ dàng nhận thêm 2e. Nguyên tử oxi có độ âm điện lớn (3,44), chỉ kém flo (3,98).
Do vậy, oxi là nguyên tố phi kim hoạt động hoá học, có tính oxi hoá mạnh. Trong các hợp chất (trừ hợp chất với flo), nguyên tố oxi có số oxi hoá là -2.
Oxi tác dụng với hầu hết các kim loại (trừ Au, Pt, ...) và các phi kim (trừ halogen). Oxi tác dụng với nhiều hợp chất vô cơ và hữu cơ.
9.1. Tác dụng với kim loại
Tác dụng với hầu hết kim loại (trừ au và Pt), cần có to tạo oxit:
9.2. Tác dụng với phi kim
Tác dụng với hầu hết phi kim (trừ halogen), cần có to tạo oxit:
ĐB: Tác dụng với H2 nổ mạnh theo tỉ lệ 2:1 về số mol:
9.3. Tác dụng với hợp chất
- Tác dụng với các chất có tính khử:
- Tác dụng với các chất hữu cơ:
10. Bài tập vận dụng
Câu 1. Nhận xét nào sau đây không đúng?
A. Đốt cháy hoàn toàn anđehit no, đơn chức, mạch hở, thu được số mol CO2 và H2O bằng nhau.
B. Anđehit axetic làm đổi màu quỳ tím sang đỏ.
C. Axit fomic có thể tham gia phản ứng tráng bạc.
D. Phản ứng giữa axit axetic với ancol etylic tạo thành etyl axetat gọi là phản ứng este hóa.
Lời giải:
Đáp án: B
Câu 2. Hiện nay nguồn nguyên liệu chính để sản xuất anđehit axetic trong công nghiệp là
A. etanol.
B. etan.
C. axetilen.
D. etilen.
Lời giải:
Đáp án: D
Câu 3. Đốt cháy hoàn toàn 0,5 mol hợp chất hữu cơ X, thu được 2 mol CO2. Chất X tác dụng được với K, tham gia phản ứng tráng bạc với phản ứng cộng Br2 theo tỉ lệ mol 1 : 1. Công thức cấu tạo của X là
A. HO-CH2-CH2-CH=CH-CHO.
B. HOOC-CH=CH-COOH.
C. HO-CH2-CH=CH-CHO.
D. HO-CH2-CH2-CH2-CHO
Lời giải:
Đáp án: C
Giải thích:
X: có 4C, có chứa nhóm OH hoặc COOH, nhóm -CHO và có 1 liên kết đôi C=C
Chú ý phản ứng RCHO + Br2 + H2O => RCOOH + 2HBr không phải là phản ứng cộng
Câu 4. Cho 6,8 gam một chất hữu cơ A (có thành phần nguyên tố C, H, O) tác dụng vừa đủ với dung dịch chứa 0,3 mol AgNO3 trong NH3, đun nóng, thu được 21,6 gam Ag. Công thức cấu tạo của A là
A. CH≡C-[CH2]2-CHO.
B. CH2=C=CH-CHO.
C. CH≡C–CH2CHO .
D. CH3-C≡C-CHO.
Lời giải:
Đáp án: C
Giải thích:
Ta có:
nAg= 21,6 /108 = 0,2 mol → nX= 0,1 mol ( cả 4 Đáp án đều anđehit đơn chức)
nAg = 0,2 mol < nAgNO3 phản ứng = 0,3 mol.
Nên X có nối 3 đầu mạch
MX = 68 = R + 29 → R= 39 (C3H3-)
Câu 5. Cho các nhận định sau:
(a) Anđehit là hợp chất chỉ có tính khử.
(b) Anđehit cộng hiđro thành ancol bậc một.
(c) Anđehit tác dụng với AgNO3/NH3 tạo thành Ag.
(d) Anđehit no, đơn chức, mạch hở có công thức tổng quát CnH2nO.
Số nhận định đúng là
A. 1
B. 2
C. 3
D. 4
Lời giải:
Đáp án: C
Giải thích:
(b) Anđehit cộng hiđro thành ancol bậc một.
(c) Anđehit tác dụng với AgNO3/NH3 tạo thành Ag.
(d) Anđehit no, đơn chức, mạch hở có công thức tổng quát CnH2nO.
Câu 6. Đốt cháy hoàn toàn 0,2 mol anđehit A no, mạch hở, đơn chức thu được tổng khối lượng CO2 và H2O là 49,6 gam. Anđehit A là
A. C2H4O
B. C3H6O2
C. C4H8O
D. C5H10O
Lời giải:
Đáp án: C
Giải thích:
Đốt cháy anđehit no, mạch hở đơn chức thu được nCO2 = nH2O = a mol
=> mCO2 + mH2O = 49,6 => 44a + 18a = 49,6 => a = 0,8 mol
=> số C trong A = nCO2 / nA = 0,8 / 0,2 = 4
=> Công thức phân từ của A là C4H8O
Câu 7. Hợp chất A chứa C, H, O có M < 90 đvC. A tham gia phản ứng tráng bạc và có thể tác dụng với H2 (xt Ni) sinh ra ancol chứa C bậc IV trong phân tử. Công thức của A là
A. (CH3)2CHCHO.
B. (CH3)2CH-CH2CHO.
C. (CH3)3C-CH2CHO.
D. (CH3)3CCHO.
Lời giải:
Đáp án: D
Giải thích:
Hợp chất A có khả năng tráng bạc do đó A chứa gốc –CHO
Ancol chứa C bậc IV => có dạng (CH3)3C-R-CHO
Vì M < 90 => 57 + R + 29 < 90 => R = 0
CTCT của A là (CH3)3CCHO.
Câu 8. Có bao nhiêu anđehit 2 chức có công thức đơn giản nhất là C2H3O?
A. 2
B. 4
C. 1
D. 3
Lời giải:
Đáp án: A
Giải thích:
Anđehit có CTPT dạng C2nH3nOn (anđehit no, mạch hở, n chức)
Do anđehit no, mạch hở, có n chức nên độ bất bão hòa: k = n
Ta có: H = 2C + 2 - 2k => 3n = 2.2n + 2 - 2n => n = 2
Vậy công thức công cấu tạo của anđehit là C4H6O2
=> Có 2 đồng phân: HOC-CH2-CH2-CHO; CH3CH(CHO)2
Câu 9. Có thể dùng một chất nào trong các chất dưới đây để nhận biết được các chất: ancol etylic, glixerol, dung dịch anđehit axetic đựng trong ba lọ mất nhãn?
A. Cu(OH)2/OH-
B. Quỳ tím
C. Kim loại Na
D. dd AgNO3/NH3.
Lời giải:
Đáp án: A
Giải thích:
Trích mẫu thử và đánh số thứ tự
Sử dụng thuốc thử Cu(OH)2/OH− để nhận biết các chất mất nhãn
|
C3H5(OH)3 |
CH3CHO |
C2H5OH |
|
|
Cu(OH)2/OH- (to thường) |
Phức màu xanh |
Không phản ứng |
Không phản ứng |
|
Cu(OH)2/OH- đun nóng |
Kết tủa đỏ gạch |
Không phản ứng |
Phương trình hóa học
Cu(OH)2 + 2C3H5(OH)3→ [C3H5(OH)2O]2Cu + 2H2O
phức màu xanh
CH3CHO + 2Cu(OH)2→ CH3COOH + Cu2O + 2H2O