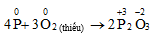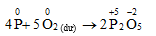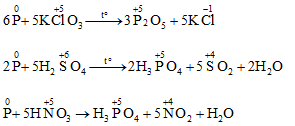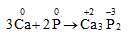P + KClO3 → KCl + P2O5 | P ra P2O5
Sinx.edu.vn xin giới thiệu phương trình P + KClO3 → KCl + P2O5 là phản ứng oxi hóa khử. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Nội dung bài viết
Phản ứng P + KClO3 → KCl + P2O5
1. Phương trình phản ứng P ra P2O5
6P + 5KClO3 → 5KCl + 3P2O5
2. Cân bằng phản ứng P + KClO3 → KCl + P2O5
Xác định số oxi hóa thay đổi
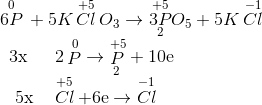
Phương trình phản ứng hóa học
6P + 5KClO3→ 5KCl + 3P2O5
P đóng vai trò là chất khử
3. Điều kiện phản ứng P tác dụng với KClO3
Nhiệt độ cao
4. Cách thực hiện phản ứng
Cho KClO3 (kali clorat) tác dụng P (photpho) ở nhiệt độ cao và tạo ra chất KCl (kali clorua), P2O5 (diphotpho penta oxit)
5. Hiện tượng nhận biết phản ứng.
Phương trình không có hiện tượng nhận biết đặc biệt.
Trong trường hợp này, bạn chỉ thường phải quan sát chất sản phẩm KCl (kali clorua) (trạng thái: lỏng) (màu sắc: không màu), P2O5 (diphotpho penta oxit) (trạng thái: rắn) (màu sắc: trắng), được sinh ra
Hoặc bạn phải quan sát chất tham gia KClO3 (kali clorat) (trạng thái: rắn) (màu sắc: trắng), P (photpho) (trạng thái: rắn) (màu sắc: đỏ), biến mất.
6. Bản chất của các chất tham gia phản ứng
6.1. Bản chất của P (Photpho)
- Trong phản ứng trên P là chất khử.
- P vừa có tính khử vừa có tính oxi hoá nên P khử được một số hợp chất có tính oxi hoá mạnh.
6.2. Bản chất của KClO3 (Kali clorat)
- Trong phản ứng trên KClO3 là chất oxi hoá.
- KClO3 là hợp chất có tính oxi hoá mạnh tác dụng được với nhiều phi kim tạo muối như S, P, Mg.
7. Tính chất hoá học của P
P vừa có tính khử vừa có tính oxi hóa
7.1. Tính khử
a. Khử phi kim mạnh hơn:O2, Cl2, S...
- Khử O2 :
Photpho trắng tác dụng với oxi ở điều kiện thường, phản ứng tỏa năng lượng ở dạng ánh sáng → gây ra hiện tượng phát quang hóa học
Photpho đỏ chỉ tác dụng với oxi ở nhiệt độ cao
- Khử : 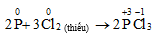
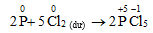
b. Khử một số hợp chất có tính oxi hóa mạnh
7.2. Tính oxi hóa
* P oxi hóa các kim loại hoạt động tạo ra photphua kim loại
8. Ứng dụng của P
+ P đỏ được dùng trong sản xuất diêm.
+ Điều chế axit photphoric, thuốc trừ sâu chứa photpho…
+ Dùng trong quân sự: sản xuất bom, đạn cháy, đạn khói…
+ Photpo còn là một nguyên tố rất cần cho con người nhất là trí thông minh, sáng tạo, phát triển xương. Cần cho cây nhất là cấy ăn quả.
9. Câu hỏi vận dụng
Câu 1. Cho phản ứng: P + KClO3 → P2O5 + KCl. Hệ số cân bằng của phương trình phản ứng này từ trái qua phải lần lượt là:
A. 2, 1, 1, 1
B. 4, 3, 2, 3
C. 8, 1, 4, 1
D. 6, 5, 3, 5
Lời giải:
Đáp án: D
Câu 2. Photpho thể hiện tính oxi hóa ở phản ứng nào sau đây?
A. 2P + 5Cl2 2PCl5
B. 2P + 5O2 2P2O5
C. P + 5HNO3⟶ H3PO4 + 5NO2+ H2O
D. 3Ca + 2P Ca3P2
Lời giải:
Đáp án: D
Câu 3. Trong phản ứng của photpho với (1) Ca, (2) O2, (3) Cl2, (4) KClO3. Những phản ứng trong đó photpho thể hiện tính khử là
A. (1), (2), (4).
B. (1), (3).
C. (2), (3), (4).
D. (1), (2), (3).
Lời giải:
Đáp án: C
Câu 4. Đốt cháy photpho trong khí clo dư, phản ứng xảy ra hoàn toàn, sau phản ứng ta thu được hợp chất nào?
A. PCl3
B. PCl5
C. PCl2
D. PCl6
Lời giải:
Đáp án: B
Các bài liên quan:
- Ca + H2O → Ca(OH)2 + H2
- Ca(HCO3)2 → CaCO3 + CO2 + H2O
- CaO + H2O → Ca(OH)2
- CaO + CO2 → CaCO3
- CaO + HCl → CaCl2 + H2O
- Ca(OH)2 + HCl → CaCl2 + H2O
- Ca(OH)2 + H2SO4 ⟶ CaSO4 + H2O
- CaCO3 → CaO + CO2
- CaCO3 + HCl → CaCl2 + CO2 + H2O
- CaCO3 + HNO3 → Ca(NO3)2 + CO2 + H2O
- CaCO3 + CO2 + H2O → Ca(HCO3)2
- CaOCl2 + HCl → CaCl2 + Cl2 + H2O
- CaOCl2 → CaCl2 + O2
- H2SO4 + KOH → K2SO4 + H2O
- KOH + HCl → KCl + H2O
- KOH + H3PO4 → K3PO4 + H2O
- K + H2O → KOH + H2
- K2O + H2O → KOH
- KCl + H2O → KOH + H2 + Cl2
- K2CO3 + HCl → KCl + CO2 + H2O
- KClO3 + HCl → Cl2 + KCl + H2O
- KClO3 → KCl + O2
- BaCl2 + H2SO4 → BaSO4 + HCl
- Ba(OH)2 + H2SO4 → BaSO4 + H2O
- BaCl2 + Na2SO4 → BaSO4 + NaCl
- BaCl2 + NaHSO4 → BaSO4 + Na2SO4 + HCl
- Ba + H2O → Ba(OH)2 + H2
- BaO + H2O → Ba(OH)2
- Ba(HCO3)2 + NaOH → BaCO3 + Na2CO3 + H2O
- C + H2SO4 → SO2 + CO2 + H2O
- C + CO2 → CO
- CO + O2 → CO2
- CO2 + H2O → H2CO3
- CO2 + NaOH → Na2CO3 + H2O
- CO2 + NaOH → NaHCO3
- CO2 + KOH → K2CO3 + H2O
- CO2 + Ca(OH)2 → CaCO3 + H2O
- CO2 + Ba(OH)2 → BaCO3 + H2O
- SiO2 + HF → SiF4 + H2O
- SiO2 + Na2CO3 → Na2SiO3 + CO2
- S + O2 → SO2
- S + HNO3 → H2SO4 + NO2 + H2O
- S + H2SO4 → SO2 + H2O
- H2 + S → H2S
- SO2 + Na2O → Na2SO3
- SO2 + KOH → K2SO3 + H2O
- SO2 + Ca(OH)2 → CaSO3 + H2O
- SO2 + H2S → S + H2O
- SO2 + NaH → H2S + Na2SO4
- SO2 + Br2 + H2O → HBr + H2SO4
- SO2 + Cl2 + H2O → HCl + H2SO4
- SO2 + O2 → SO3
- SO2 + O2 + H2O → H2SO4
- SO2 + KMnO4 + H2O → MnSO4 + K2SO4 + H2SO4
- SO3 + H2O → H2SO4
- H2SO4 + KCl → HCl + K2SO4
- H2S + FeCl3 → S + FeCl2 + HCl
- H2S + KMnO4 → KOH + MnO2 + S + H2O
- H2S + Br2 + H2O → H2SO4 + HBr
- H2S + CuSO4 → CuS + H2SO4
- H2S + H2SO4 → SO2 + H2O + S
- H2S + O2 → SO2 + H2O
- H2S + Cl2 + H2O → H2SO4 + HCl
- H2S + NaOH → Na2S + H2O
- H2S + NaOH → NaHS + H2O
- H2S + HNO3 → H2O + NO + S
- H2O2 → O2 + H2O
- ZnS + H2SO4 → ZnSO4 + H2S
- P2O5 + H2O → H3PO4
- P2O5 + KOH → K3PO4 + H2O
- P + Cl2 → PCl3
- P + H2SO4 → H3PO4 + SO2 + H2O
- P + HNO3 → H3PO4 + NO2 + H2O
- H3PO4 + NaOH → Na3PO4 + H2O
- NO2 + O2 + H2O → HNO3
- Na + H2O → NaOH + H2
- Na2O + H2O → NaOH
- Na2O + H2SO4 → Na2SO4 + H2O
- NaNO3 + H2SO4 → HNO3 + NaHSO4
- NaHCO3 → Na2CO3 + CO2 + H2O
- NaHSO3 + NaOH → Na2SO3 + H2O
- NaHCO3 + H2SO4 → Na2SO4 + CO2 + H2O
- Na2CO3 + H2SO4 → Na2SO4 + CO2 + H2O
- Na2CO3 + HCl → NaCl + CO2 + H2O
- Na2CO3 + Ba(OH)2 → NaOH + BaCO3
- Na2CO3 + CaCl2 → CaCO3 + NaCl
- Na2SO3 + HCl → NaCl + SO2 + H2O
- Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O
- NaAlO2 + CO2 + H2O → Al(OH)3 + Na2CO3
- NaClO + HCl → NaCl + Cl2 + H2O
- NaClO + CO2 + H2O → Na2CO3 + HClO
- NaOH + HCl → NaCl + H2O
- NaOH + H2SO4 → Na2SO4 + H2O
- NaCl → Na + Cl2
- NaCl + H2O → NaOH + Cl2 + H2
- NaCl + H2SO4 → NaHSO4 + HCl
- NaHCO3 + Ca(OH)2 → CaCO3 + NaOH + H2O
- NaHCO3 + Ba(OH)2 → BaCO3 + Na2CO3 + H2O
- NaHCO3 + NaOH → Na2CO3 + H2O
- NaHCO3 + HCl → NaCl + CO2 + H2O
- NaAlO2 + HCl + H2O → Al(OH)3 + NaCl
- NaF + AgNO3 → AgF + NaNO3
- Fe + FeCl3 → FeCl2
- Fe + HCl → FeCl2 + H2
- Fe + O2 → Fe3O4
- Fe + S → FeS
- Fe + Cl2 → FeCl3
- Fe + CuSO4 → FeSO4 + Cu
- Fe + AgNO3 → Fe(NO3)2 + Ag
- Fe + H2SO4 loãng → FeSO4 + H2
- Fe + H2SO4 (đặc, nóng) → Fe2(SO4)3 + SO2 + H2O
- Fe + HNO3 → Fe(NO3)3 + NO + H2O
- Fe + HNO3 (đặc, nóng) → Fe(NO3)3 + NO2 + H2O
- Fe + HNO3 đặc → Fe(NO3)3 + N2O + H2O
- FeCl2 + AgNO3 → Fe(NO3)2 + AgCl
- FeCl2 + Cl2 → FeCl3
- FeCl2 + Cl2 → FeCl3
- FeCl3 + AgNO3 → Fe(NO3)3 + AgCl
- FeCl3 + NaOH → Fe(OH)3 + NaCl
- FeCl2 + NaOH → Fe(OH)2 + NaCl
- FeS2 + O2 → Fe2O3 + SO2
- FeS2 + HNO3 → Fe(NO3)3 + H2SO4 + NO + H2O
- FeS2 + H2SO4 → Fe2(SO4)3 + SO2 + H2O
- FeS + H2SO4 đặc, nóng → Fe2(SO4)3 + SO2 + H2O
- FeS + H2SO4 loãng → FeSO4 + H2S
- FeO + HNO3 loãng → Fe(NO3)3 + NO + H2O
- FeO + HNO3 → Fe(NO3)3 + NO2 + H2O
- FeO + HNO3 loãng → Fe(NO3)3 + N2O + H2O
- FeO + H2SO4 đặc → Fe2(SO4)3 + SO2 + H2O
- Fe2O3 + CO → Fe + CO2
- Fe2O3 + HNO3 loãng → Fe(NO3)3 + H2O
- Fe2O3 + H2SO4 → Fe2(SO4)3 + H2O
- Fe3O4 + H2SO4 loãng → FeSO4 + Fe2(SO4)3 + H2O
- Fe3O4 + HCl → FeCl3 + FeCl2 + H2O
- Fe3O4 + CO → FeO + CO2
- Fe3O4 + H2 → Fe + H2O
- Fe3O4 + H2SO4 → Fe2(SO4)3 + SO2 + H2O
- Fe3O4 + HNO3 → Fe(NO3)3 + NO + H2O
- Fe3O4 + HNO3 đặc → Fe(NO3)3 + NO2 + H2O
- FeSO4 + NaOH → Fe(OH)2 + Na2SO4
- FeSO4 + HNO3 → Fe(NO3)3 + H2SO4 + NO2 + H2O
- FeSO4 + H2SO4 đặc, nóng → Fe2(SO4)3 + SO2 + H2O
- Fe(OH)2 + HNO3 → Fe(NO3)3 + NO2 + H2O
- Fe(OH)2 + H2SO4 đặc → Fe2(SO4)3 + H2S + H2O
- Fe(OH)3 → Fe2O3 + H2O
- Fe2O3 + HCl → FeCl3 + H2O
- FeCl3 + KOH → Fe(OH)3 + KCl
- FeS + HCl → FeCl2 + H2S
- FeSO4 + K2Cr2O7 + H2SO4 → Fe2(SO4)3 + Cr2(SO4)3 + K2SO4 + H2O
- FeCO3 + H2SO4 → Fe2(SO4)3 + SO2 + CO2 + H2O
- AgNO3 + NaCl → AgCl + NaNO3
- AgNO3 + H2O + NH3 + HCOOH → (NH4)2CO3 + Ag + NH4NO3
- Ag + H2SO4 → Ag2SO4 + SO2 + H2O
- Ag + HNO3 → AgNO3 + NO2 + H2O
- Ag + HNO3 → AgNO3 + NO + H2O
- Ag2S + O2 → Ag + SO2
- AgCl → Cl2 + Ag
- KMnO4 → K2MnO4 + MnO2 + O2
- Mg + HCl → MgCl2 + H2
- Mg + H2SO4 loãng → MgSO4 + H2
- Mg + HNO3 → Mg(NO3)2 + NO2 + H2O
- Mg + HNO3 → Mg(NO3)2 + N2O + H2O
- Mg + HNO3 → Mg(NO3)2 + NO + H2O
- Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O
- Mg + HNO3 → Mg(NO3)2 + N2 + H2O
- MgO + HCl → MgCl2 + H2O
- Mg(OH)2 + HCl → MgCl2 + H2O
- Zn + H2SO4 loãng → ZnSO4 + H2
- Zn + H2SO4 đặc → ZnSO4 + SO2 + H2O
- Zn + HNO3 → Zn(NO3)2 + NO2 + H2O
- Zn + HNO3 loãng → Zn(NO3)2 + NO + H2O
- Zn + HNO3 → Zn(NO3)2 + N2 + H2O
- Zn + HNO3 → Zn(NO3)2 + NH4NO3 + H2O
- Zn + HNO3 → Zn(NO3)2 + N2O + N2 + H2O
- Zn + HCl → ZnCl2 + H2
- Zn + CuSO4 → ZnSO4 + Cu
- Zn + NaOH + H2O → Na2[Zn(OH)4] + H2
- ZnO + H2SO4 → ZnSO4 + H2O
- ZnO + NaOH → Na2ZnO2 + H2O
- Zn(OH)2 + HCl → ZnCl2 + H2O
- Zn(OH)2 + NaOH → Na2ZnO2 + H2O
- CuSO4 + Na2S → CuS + Na2SO4
- Cu + HNO3 → Cu(NO3)2 + NO2 + H2O
- Cu + HNO3 → Cu(NO3)2 + N2O + H2O
- Cu + HNO3 → Cu(NO3)2 + NO+ H2O
- Cu+ H2SO4 → CuSO4 + SO2 + H2O
- Cu + AgNO3 → Cu(NO3)2 + Ag
- CuO + HCl → CuCl2 + H2O
- CuO + H2SO4 → CuSO4 + H2O
- CuO + H2 → Cu + H2O
- CuO + HNO3 → Cu(NO3)2 + H2O
- CuSO4 + NaOH → Cu(OH)2 + Na2SO4
- Cu(OH)2 + H2SO4 → CuSO4 + H2O
- Ag + O3 → Ag2O + O2
- O3 + KI + H2O → KOH + I2 + O2
- Al + FeCl3 → AlCl3 + Fe
- Al + Fe2O3 → Al2O3 + Fe
- Al + H2O + NaOH → NaAlO2 + H2
- Al + HCl → AlCl3 + H2
- Al + Cl2 → AlCl3
- Al + O2 → Al2O3
- Al + H2SO4 → Al2(SO4)3 + H2
- Al + H2SO4 → Al2(SO4)3 + SO2 + H2O
- Al + H2SO4 → Al2(SO4)3 + S + H2O
- Al + HNO3 → H2O + NO2 + Al(NO3)3
- Al + HNO3 → Al(NO3)3 + N2O + H2O
- Al + HNO3 → Al(NO3)3 + N2 + H2O
- Al + HNO3 → Al(NO3)3 + NH4NO3 + H2O
- Al + HNO3 → Al(NO3)3 + NO + H2O
- Al2O3 + NaOH → NaAlO2 + H2O
- Al2O3 + HCl → AlCl3 + H2O
- Al2O3 + H2SO4 → Al2(SO4)3 +H2O
- Al(OH)3 + NaOH → NaAlO2 + H2O
- Al(OH)3 + HCl → AlCl3 + H2O
- Al2(SO4)3 + NaOH → Al(OH)3 ↓ + Na2SO4
- AlCl3 + NaOH → NaAlO2 + NaCl + H2O