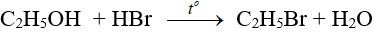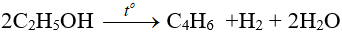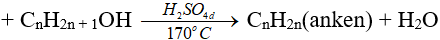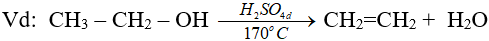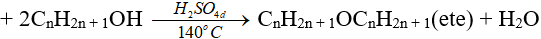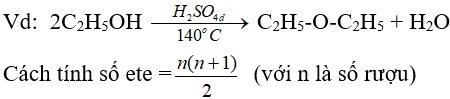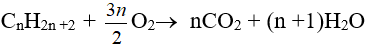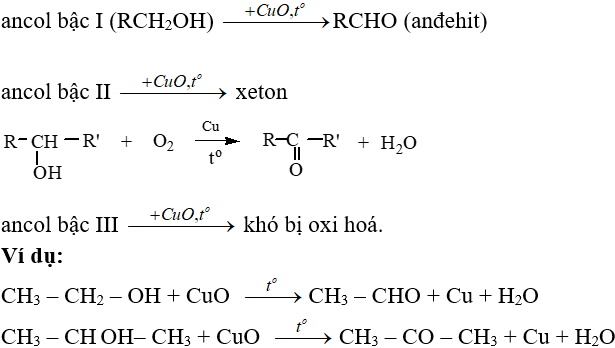CH3OH ra CH3COOH l CH3OH + CO → CH3COOH | Ancol metylic ra Axit axetic
Sinx.edu.vn xin giới thiệu phương trình CH3OH + CO → CH3COOH là phương trình phản ứng điều chế axit axetic trong công nghiệp. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng CH3OH + CO → CH3COOH
1. Phương trình phản ứng CH3OH ra CH3COOH
CH3OH + CO CH3COOH
2. Điều kiện để phương trình phản ứng hóa học xảy ra
Nhiệt độ xúc tác
Phương pháp đi từ metanol cho giá thành thấp nhất do CH4 có sẵn trong khí thiên nhiên và khí dầu mỏ.
3. Hiện tượng nhận biết phản ứng.
Phương trình không có hiện tượng nhận biết đặc biệt.
Trong trường hợp này, bạn chỉ thường phải quan sát chất sản phẩm CH3COOH (acid acetic) (trạng thái: lỏng) (màu sắc: không màu), được sinh ra
Hoặc bạn phải quan sát chất tham gia CH3OH (metanol) (trạng thái: lỏng) (màu sắc: không màu), CO (cacbon oxit) (trạng thái: khí) (màu sắc: không màu), biến mất.
4. Cách thực hiện phản ứng
Cho CH3OH (metanol) tác dụng CO (cacbon oxit) và tạo ra chất CH3COOH (acid acetic)
5. Tính chất hóa học của Ancol
5.1. Phản ứng thế nguyên tử hiđro của nhóm OH ancol (phản ứng đặc trưng của Ancol)
- Tính chất chung của ancol:
2ROH + Na → 2RONa + H2↑
- Tính chất đặc trưng của glixerol:
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + H2O
(ĐK: muốn tác dụng với Cu(OH)2 phải có 2 nhóm -OH trở lên liền kề nhau)
→ Phản ứng này dùng để phân biệt ancol đơn chức với ancol đa chức có 2 nhóm OH cạnh nhau trong phân tử.
5.2. Phản ứng thế nhóm OH
- Phản ứng với axit vô cơ:
- Phản ứng tạo dien: dùng sản xuất cao su buna.
(ĐK: phải có xúc tác là Al2O3 + MgO hoặc ZnO/500ºC)
5.3. Phản ứng tách nước (phản ứng đề hidrat hoá)
Chú ý:
(ĐK n ≥ 2, theo quy tắc Zai-xép)
(ancol bậc càng cao thì càng dễ khử nước tạo anken)
(phải là rượu no, đơn chức)
(ancol bậc càng thấp thì càng dễ khử nước tạo ete)
5.4. Phản ứng oxi hoá
- Phản ứng oxi hoá hoàn toàn:
- Phản ứng oxi hoá không hoàn toàn:
6. Tính chất vật lí của ancol
Các ancol thường có các tính chất vật lý sau: Nhiệt độ nóng chảy và nhiệt độ sôi cao hơn: Do sự tồn tại của liên kết hidro giữa các phân tử ancol, cần nhiều nhiệt độ để vỡ các liên kết này, vì vậy nhiệt độ nóng chảy và nhiệt độ sôi của ancol thường cao hơn so với các hidrocacbon tương đương.
Độ tan trong nước: Các ancol từ C1 đến C3 (methanol, ethanol và propanol) tan vô hạn trong nước do khả năng tạo liên kết hidro mạnh với nước. Từ C4 trở đi, độ tan trong nước giảm dần do kích thước của phân tử ancol tăng lên và sức mạnh của liên kết hidro không còn đủ mạnh để duy trì tính tan trong nước.
Sự tồn tại của liên kết hidro giữa các phân tử ancol và giữa các phân tử ancol với nước có thể giải thích các tính chất này. Điều này làm cho ancol trở thành một loại chất lỏng có sự tương tác mạnh mẽ với nước và có nhiều ứng dụng trong hóa học và công nghiệp.
7. Tính chất hóa học của CO
7.1. CO là oxit trung tính
– Ở điều kiện thường, CO không phản ứng với nước, kiềm và axit.
7.2. CO là chất khử
– Ở nhiệt độ cao, CO khử được điều oxit kim loại
• CO khử CuO (CO khử oxit đồng)
CO(k) + CuO(r,đen) 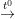 Cu(r,đỏ) + CO2(k)
Cu(r,đỏ) + CO2(k)
• CO khử Fe3O4 (CO khử oxit sắt trong lò cao)
4CO(k) + Fe3O4(r) 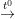 3Fe(r) + 4CO2(k)
3Fe(r) + 4CO2(k)
• CO cháy trong không khí (cháy trong oxi) với ngọn lửa màu xanh nhiều nhiệt
2CO(k) + O2(k) 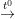 2CO2(k)
2CO2(k)
8. Các phương pháp khác điều chế Axit axetic
Các phương pháp điều chế axit axetic
Trong công nghiệp, đi từ Butan C4H10
2C4H10+ 3O2 (xúc tác, to) → 4CH3COOH + 2H2O
Để sản xuất giấm ăn, người ta thường dùng phương pháp lên men dung dịch rượu etylic loãng
CH3CH2OH + O2 → CH3COOH + 2H2O
9. Câu hỏi vận dụng
Câu 1. Hóa chất dùng để phân biệt rượu etylic, axit axetic là
A. Quỳ tím.
B. Brom.
C. Clo.
D. Nước.
Lời giải:
Đáp án: A
Giải thích:
Dựa vào tính chất hóa học đặc trưng của rượu etylic và axit axetic.Hóa chất dùng để phân biệt rượu etylic, axit axetic là quỳ tím.+ Axit axetic làm quỳ tím hóa đỏ.+ Rượu etylic không làm quỳ tím đổi màu.
Câu 2. Trong công nghiệp, phương pháp điều chế axit axetic hiện đại nhất là
A. lên men giấm
B. oxi hóa anđehit axetic
C. đi từ metanol
D. oxi hóa butan
Lời giải:
Đáp án: C
Câu 3.Trong công nghiệp một lượng lớn axit axetic được điều chế bằng cách
A. nhiệt phân metan sau đó làm lạnh nhanh.
B. lên men dung dịch rượu etylic.
C. oxi hóa etan có xúc tác và nhiệt độ thích hợp.
D. oxi hóa butan có xúc tác và nhiệt độ thích hợp.
Lời giải:
Đáp án: D
Câu 4. Khi tách nước từ 2 ancol đồng phân có cơng thức C4H10O với H2SO4đặc ở 170oC thu được 3 anken (khơng kể đồng phân hình học). Công thức cấu tạo của hai ancol là
A. CH3CH2CH2CH2OH và (CH3)2CHCH2OH.
B. (CH3)2CHCH2OH và (CH3)3COH.
C. CH3CH(OH)CH2CH3 và CH3CH2CH2CH2OH.
D. CH3CH(OH)CH2CH3 và (CH3)3COH.
Lời giải:
Đáp án: C
Giải thích:
CH3CH2CH2CH2OH: tách nước tạo 1 anken(CH3)2CHCH2OH: tách nước đk 1 anken=>A loại(CH3)3COH: cái này không tách nước tạo anken dk=>B loại tiếpCH3CH(OH)CH2CH3: cái này tách nước tạo 2 anken là CH2=CH-CH2-CH3và CH3-CH=CH-CH3