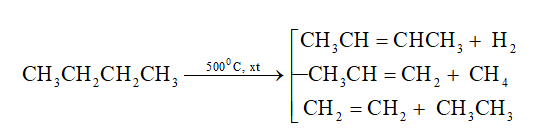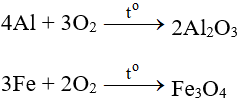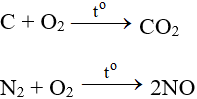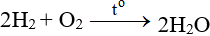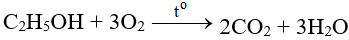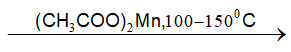C4H10 ra CH3COOH l C4H10 + O2 → CH3COOH + H2O | Butan ra Axit axetic
Sinx.edu.vn xin giới thiệu phương trình C4H10 + O2 → CH3COOH + H2O là phản ứng oxi hóa khử. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Nội dung bài viết
Xem thêm »
Phản ứng C4H10 + O2 → CH3COOH + H2O
1. Phương trình phản ứng oxi hóa không hoàn toàn
C4H10 + O2 CH3COOH + H2O
Lưu ý: Phản ứng cháy hoàn toàn sản phẩm đốt cháy C4H10 tạo ra CO2 và H2O
C4H10 + 13/2O2 4CO2 + 5H2O
2. Bản chất của các chất tham gia phản ứng
2.1. Bản chất của C4H10 (Butan)
- Trong phản ứng trên C4H10 là chất khử.
- Trong công nghiệp, với điều kiện chất xúc tác và nhiệt độ thích hợp từ butan điều chế ra axit axetic (CH3COOH).
2.2. Bản chất của O2 (Oxi)
Trong phản ứng trên O2 là chất oxi hoá.
3. Điều kiện phản ứng xảy ra oxi hóa không hoàn toàn butan
Nhiệt độ: nhiệt độ Xúc tác: Mn2+.
4. Các phương pháp điều chế Axit axetic
Trong công nghiệp, đi từ Butan C4H10:
2C4H10 + 3O2 (xúc tác, to) → 4CH3COOH + 2H2O
Trong phòng thí nghiệm:
2CH3COONa + H2SO4 2CH3COOH + Na2SO4
Để sản xuất giấm ăn, người ta thường dùng phương pháp lên men dung dịch rượu etylic loãng:
CH3CH2OH + O2 CH3COOH + 2H2O
5. Tính chất của C4H10
5.1 Tính chất hóa học của C4H10
Trong phân tử C4H10 các liên kết xích ma bền vững, vì thế C4H10 tương đối trơ về mặt hóa học: Ở nhiệt độ thường, chúng không phản ứng với axit, bazơ và chất oxi hóa mạnh (như KMnO4) Dưới tác dụng của ánh sáng, xúc tác, nhiệt, C4H10 tham gia các phản ứng thế, phản ứng tách và phản ứng oxi hóa.
a. Phản ứng thế bởi halogen
- Khi chiếu sáng hoặc đốt nóng hỗn hợp butan và clo sẽ xảy ra phản ứng thế lần lượt các nguyên tử hidro bằng clo. Tương tự như metan.
C4H10 + Cl2 → C4H9Cl + HCl
- Phản ứng thế H bằng halogen thuộc loại phản ứng halogen hóa, sản phẩm hữu cơ có chứa halogen gọi là dẫn xuất halogen.
b. Phản ứng tách (gãy liên kết C-C và C-H)
- Dưới tác dụng của nhiệt và xúc tác (Cr2O3, Fe, Pt,...), các ankan không những bị tách hidro tạo thành các hidrocacbon không no mà còn bị gãy các liên kết C-C tạo ra các phân tử nhỏ hơn.
c. Phản ứng oxi hóa
- Khi đốt, butan bị cháy tạo ra CO2, H2O và tỏa nhiều nhiệt
- Nếu không đủ oxi, ankan bị cháy không hoàn toàn, khi đó ngoài CO2 và H2O còn tạo ra các sản phẩm như CO, than muội, không những làm giảm năng suất tỏa nhiệt mà còn gây độc hại cho môi trường.
5.2 Tính chất vật lí của C4H10
Butan là chất khí, không màu, dễ cháy, dễ hóa lỏng. Butan có trong khí thiên nhiên, khí chế biến dầu.
6. Tính chất hóa học của Oxi
Khi tham gia phản ứng, nguyên tử O dễ dàng nhận thêm 2e. Nguyên tử oxi có độ âm điện lớn (3,44), chỉ kém flo (3,98).
Do vậy, oxi là nguyên tố phi kim hoạt động hoá học, có tính oxi hoá mạnh. Trong các hợp chất (trừ hợp chất với flo), nguyên tố oxi có số oxi hoá là -2.
Oxi tác dụng với hầu hết các kim loại (trừ Au, Pt, ...) và các phi kim (trừ halogen). Oxi tác dụng với nhiều hợp chất vô cơ và hữu cơ.
6.1. Tác dụng với kim loại
Tác dụng với hầu hết kim loại (trừ au và Pt), cần có to tạo oxit:
6.2. Tác dụng với phi kim
Tác dụng với hầu hết phi kim (trừ halogen), cần có to tạo oxit:
ĐB: Tác dụng với H2 nổ mạnh theo tỉ lệ 2:1 về số mol:
6.3. Tác dụng với hợp chất
- Tác dụng với các chất có tính khử:
- Tác dụng với các chất hữu cơ:
 7. Hiện tượng nhận biết phản ứng
7. Hiện tượng nhận biết phản ứng
Sản phẩm thu được sau phản ứng làm quỳ tím chuyển sang màu đỏ.
8. Bạn có biết
- Phản ứng trên còn được gọi là phản ứng oxi hóa cắt mạch cacbon.
- Phản ứng trên được dùng để điều chế axit axetic trong công nghiệp.
- Các axit béo mạch dài dùng để sản xuất xà phòng được điều chế tương tự bằng cách oxi hóa cắt mạch các ankan phân đoạn C25 – C40:
R – CH2 – CH2 – R’ + O2 RCOOH + R’COOH + H2O
Người ta dùng dung dịch kiềm để tách lấy axit khỏi ankan chưa phản ứng.
9. Câu hỏi bài tập
Câu 1. Dãy chất phản ứng với axit axetic là
A. K, ZnO, Cu, Na2CO3, KOH
B. Al, ZnO, Fe, Na2CO3, Ag
C. Cu, SO2, Na2CO3, Fe, KOH
D. Zn , ZnO, Na2CO3, Fe, KOH
Lời giải:
Đáp án: D
Giải thích:
Zn + 2CH3COOH → (CH3COO)2Zn + H2
ZnO + 2CH3COOH → (CH3COO)2Zn + H2O
2CH3COOH + Na2CO3 → 2CH3COONa + H2O + CO2
Fe + 2CH3COOH → (CH3COO)2Fe + H2
CH3COOH + KOH → CH3COOK + H2O
Câu 2. Để phân biệt C2H5OH và CH3COOH, ta dùng hóa chất nào sau đây là đúng?
A. kim loại Na.
B. dung dịch NaOH.
C. quỳ tím.
D. cả A và C đều đúng.
Lời giải:
Giải thích:
Để nhận biết 2 lọ đựng dung dịch C2H5OH và CH3COOH ta dùng quỳ tím
C2H5OH không làm đổi màu quỳ còn CH3COOH làm quỳ chuyển đỏ.
Loại A vì cả 2 dung dịch đều phản ứng tạo bọt khí.
Loại B vì cho dung dịch NaOH vào cả 2 dung dịch không có hiện tượng
Câu 3. Sản phẩm thu được khi oxi hóa cắt mạch butan ở nhiệt độ cao, có xúc tác coban axetat là
A. Axit axetic.
B. Ancol metylic.
C. Anđehit metylic.
D. Propanal.
Lời giải:
Đáp án: A
Câu 4. Có 3 chất hữu cơ có công thức phân tử là C2H4, C2H4O2, C2H6O được kí hiệu ngẫu nhiên là A, B, C biết:
Chất A và C tác dụng được với natri.
Chất B ít tan trong nước
Chất C tác dụng được với Na2CO3 Công thức phân tử của A, B, C lần lượt là
A. C2H4, C2H4O2, C2H6O.
B. C2H4, C2H6O, C2H4O2.
C. C2H6O, C2H4O2, C2H4
D. C2H6O, C2H4, C2H4O2.
Lời giải:
Đáp án: D
Giải thích:
Chất C vừa tác dụng với Na, vừa tác dụng với Na2CO3 => trong phân tử có nhóm –COOH
=> C là C2H4O2
Chất A tác dụng được với Na => trong phân tử có nhóm –OH => A là C2H5OH hay C2H6O
Chất B không tan trong nước, không phản ứng với Na và Na2CO3 => B là etilen: CH2=CH2
Câu 5. Cho sơ đồ phản ứng sau: C2H4→ X → CH3COOH → CH3COOC2H5. Chất X là
A. CH4.
B. C6H6.
C. C2H2.
D. C2H5OH.
Lời giải:
Đáp án: D
Giải thích:
C2H4 → C2H5OH → CH3COOH → CH3COOC2H5
Phương trình hóa học:
C2H4+ H2O C2H5OH
C2H5OH + O2 CH3COOH + H2O
CH3COOH + C2H5OH CH3COOC2H5 + H2O
Câu 6. Để tách các chất ra khỏi nhau từ hỗn dung dịch chứa axit axetic và ancol etylic, có thể tiến hành theo trình tự nào sau đây?
A. Dùng CaCO3, chưng cất, sau đó tác dụng với H2SO4
B. Dùng CaCCl2, chưng cất, sau đó tác dụng với H2SO4
C. Dùng Na2O, sau đó cho tác dụng với H2SO4
D. Dùng NaOH, sau đó cho tác dụng với H2SO4
Lời giải:
Đáp án: A
Câu 7. Cho các phản ứng sau ở điều kiện thích hợp:
(1) Lên men giấm ancol etylic
(2) Oxi hóa không hoàn toàn andehit axetic
(3) Oxi hóa không hoàn toàn Butan
(4) Cho metanol tác dụng với cacbon oxit
Trong những phản ứng trên, số phản ứng tạo ra axit axetic là?
A. 1
B. 2
C. 3
D. 4
Lời giải:
Đáp án: D
Giải thích:
C2H5OH + O2 CH3COOH (axit axetic)
CH3CHO + O2 CH3COOH
C4H10+ O2 CH3COOH + H2O
CH3OH + CO CH3COOH
Câu 8. Phương pháp được xem là hiện đại để điều chế axit axetic là:
A. Tổng hợp từ CH3OH và CO
B. Phương pháp oxi hóa CH3CHO
C. Phương pháp lên men giấm từ ancol etylic
D. Điều chế từ muối axetat
Lời giải:
Đáp án: A
Giải thích:
Tất cả các cách trên điều điều chế được axit axetic trực tiếp, tuy nhiên trong công nghiệp người ta đi từ metanol để điều
chế axit axetic
CH3OH + CO → CH3COOH
Đây là phương pháp hiện đại để sản xuất axit axetic.Do metanol và cacbon oxit được điều chế từ metan có sẵn trong
khí thiên nhiên và khí mỏ dầu nên chi phí sản xuất rẻ, tạo sản phẩm với giá thành hạ.