C2H2 + AgNO3 + NH3 → Ag–C≡C-Ag + NH4NO3 | Axetilen ra Bạc axetilua
Sinx.edu.vn xin giới thiệu phương trình C2H2 + AgNO3 + NH3 → Ag–C≡C-Ag + NH4NO3 là phản ứng thế bằng ion kim loại. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng: C2H2 + AgNO3 + NH3 → Ag–C≡C-Ag + NH4NO3
1. Phương trình phản ứng axetilen tác dụng với AgNO3/NH3
HC ≡ CH + 2AgNO3 + 2NH3→ + 2NH4NO3
2. Điều kiện phản ứng axetilen tác dụng với AgNO3/NH3
- Phản ứng diễn ra ngay điều kiện thường.
3. Hiện tượng của phản ứng axetilen tác dụng với AgNO3/NH3
- Có kết tủa vàng xuất hiện; kết tủa là (bạc axetilua).
4. Cách tiến hành phản ứng axetilen tác dụng với AgNO3/NH3
- Sục khí axetilen vào ống nghiệm có chứa dung dịch AgNO3/NH3.
5. Lưu ý về phản ứng axetilen tác dụng với AgNO3/NH3
- Phản ứng giữa axetilen và AgNO3/NH3 là phản ứng thế H linh động. Đây không phải là phản ứng tráng gương.
6. Mở rộng về tính chất hoá học của ankin
6.1. Phản ứng cộng
a) Cộng hiđro
- Khi có niken (hoặc platin hoặc palađi) làm xúc tác, ankin cộng hiđro tạo thành anken, sau đó tạo thành ankan.
Thí dụ:
CH ≡ CH + H2 Ni,to−−→→??,?? CH2 = CH2
CH2 = CH2 + H2 Ni,to−−→→??,?? CH3 – CH3
- Lưu ý: Khi dùng xúc tác là hỗn hợp Pd/PbCO3 hoặc Pd/BaSO4, ankin chỉ cộng một phân tử hiđro tạo thành anken.
CH ≡ CH + H2 Pd/PbCO3,to−−−−−−−→→??/????3,?? CH2 = CH2
⇒ Đặc tính này được dùng để điều chế anken từ ankin.
b) Cộng brom, clo
- Brom và clo cũng tác dụng với ankin theo hai giai đoạn liên tiếp.
Thí dụ:
CH ≡ CH + Br2 → CHBr = CHBr
CHBr = CHBr + Br2 → CHBr2 – CHBr2
c) Cộng HX (X là OH, Cl, Br, CH3COO...)
- Ankin tác dụng với HX theo hai giai đoạn liên tiếp.
Thí dụ:
CH ≡ CH + HCl to,xt−→→??,?? CH2 = CHCl
CH2 = CHCl + HCl to,xt−→→??,?? CH3 – CHCl2
- Khi có xúc tác thích hợp, ankin tác dụng với HCl sinh ra dẫn xuất monoclo của anken.
Thí dụ:
CH ≡ CH + HCl HgCl2−−−−−−→150−200Co→150−200??????2 CH2 = CHCl
- Phản ứng cộng HX của các ankin cũng tuân theo quy tắc Mac-côp-nhi-côp.
- Phản ứng cộng H2O của các ankin chỉ xảy ra theo tỉ lệ số mol 1:1.
Thí dụ:
CH ≡ CH + H2O HgSO4,H2SO4−−−−−−−−→→????4,?2??4 CH3 – CH = O (anehit axetic)
d) Phản ứng đime và trime hoá
2CH ≡ CH to,xt−→→??,?? CH ≡ C – CH = CH2 (vinylaxetilen)
3CH ≡ CH 600Co−−→bôtC→?ô??600?? C6H6 (benzen)
6.2. Phản ứng thế bằng ion kim loại
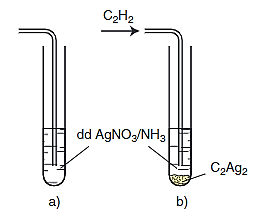
- Sục khí axetilen vào dung dịch bạc nitrat trong amoniac, thấy có kết tủa vàng nhạt.
CH ≡ CH + 2AgNO3 + 2NH3 → Ag – C ≡ C – Ag↓ + 2NH4NO3
Phản ứng thế nguyên tử hidro của C2H2 bằng ion bạc
a) Trước khi sục khí C2H2.
b) Sau khi sục khí C2H2.
Kết luận:
- Nguyên tử hiđro liên kết trực tiếp với nguyên tử cacbon liên kết ba đầu mạch có tính linh động cao hơn các nguyên tử hiđro khác nên có thể bị thay thế bằng ion kim loại.
- Các ank-1-in khác như propin, but-1-in, ... cũng có phản ứng tương tự axetilen.
⇒ Tính chất này được dùng để phân biệt ank-1-in với anken và các ankin khác.
6.3. Phản ứng oxi hoá
a) Phản ứng oxi hoá hoàn toàn (cháy)
Các ankin cháy toả nhiều nhiệt:
2CnH2n – 2 + (3n – 1)O2 to→→?? 2nCO2 + 2(n – 1)H2O
b) Phản ứng oxi hoá không hoàn toàn
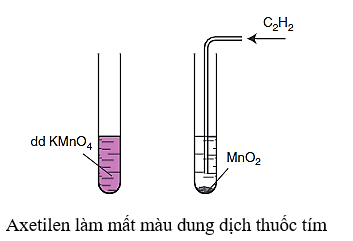
- Tương tự anken và ankađien, ankin cũng có khả năng làm mất màu dung dịch thuốc tím.
7. Tính chất vật lí của ankin
Ít tan trong nước, tan được trong một số dung môi hữu cơ. Nhiệt độ sôi và nhiệt độ nóng chảy tăng dần theo phân tử khối. Từ C2 đến C4 là chất khí; C5 đến C16 là chất lỏng.
8. Bài tập vận dụng liên quan
Câu 1: Để phân biệt but-1-in và but-2-in người ta dùng thuốc thử nào sau đây?
A. Dung dịch hỗn hợp KMnO4 + H2SO4
B. Dung dịch AgNO3/NH3
C. Dung dịch Br2
D. Dung dịch HCl
Hướng dẫn giải:
Đáp án B
Các ankin-1-in có phản ứng đặc trưng là tác dụng với AgNO3/NH3 tạo kết tủa màu vàng → chọn thuốc thử là dung dịch AgNO3/NH3
Phương trình hóa học:
CH≡C−CH2CH3+AgNO3+NH3→AgC≡C−CH2CH3+NH4NO3??≡?−??2??3+????3+??3→???≡?−??2??3+??4??3
Câu 2: X có thể tham gia cả 4 phản ứng. Phản ứng cháy trong oxi, phản ứng cộng brom, phản ứng cộng hiđro (xúc tác Ni, t0), phản ứng thế với dung dịch AgNO3/NH3. X là
A. etan
B. etilen
C. axetilen
D. but-2-in
Hướng dẫn giải:
Đáp án C
X tham gia phản ứng cộng brom, cộng hidro phải có liên kết π kém bền (loại A)
X có phản ứng thế với dung dịch AgNO3/NH3 → X là ank-1-in
→ Chất thỏa mãn đề Câu là axetilen.
Câu 3: Số đồng phân ankin có công thức phân tử C5H8 không tác dụng với dung dịch chứa AgNO3/NH3 là
A. 4
B. 2
C. 1
D. 3
Hướng dẫn giải:
Đáp án C
Có 1 đồng phân thỏa mãn: CH3−C≡C−CH2−CH3??3−?≡?−??2−??3
Câu 4: Dẫn 17,4 gam hỗn hợp khí X gồm propin và but-2-in lội thật chậm qua bình đựng dung dịch AgNO3/NH3 dư thấy có 44,1 gam kết tủa xuất hiện. Phần trăm thể tích của mỗi khí trong X là
A. C3H4 (80%) và C4H8 (20%)
B. C3H4 (25%) và C4H6 (75%)
C. C3H4 (75%) và C4H6 (25%)
D. C3H4 (20%) và C4H6 (80%)
Hướng dẫn giải:
Đáp án C
Khi cho hỗn hợp X tác dụng với dung dịch AgNO3/NH3 thì chỉ có propin phản ứng, but-2-in không phản ứng vì không có nối ba đầu mạch.
Phương trình hóa học
CH≡C−CH3+AgNO3+NH3→AgC≡C−CH3+NH4NO3??≡?−??3+????3+??3→???≡?−??3+??4??3
Ta có: n↓ = 0,3 mol
Theo phương trình: nC3H4=n↓=0,3mol??3?4=?↓=0,3???
→mC3H4=0,3.40=12gam→??3?4=0,3.40=12???
→mC4H6=17,4−12=5,4gam→??4?6=17,4−12=5,4???
→nC4H6=5,454=0,1mol→??4?6=5,454=0,1???
Thành phần phần trăm về thể tích các khí trong hỗn hợp là
%VC3H4=0,30,3+0,1.100%=75%%??3?4=0,30,3+0,1.100%=75%
→%VC4H6=100%−75%=25%→%??4?6=100%−75%=25%
Câu 5: Cho 3,36 lít khí ankin X (đktc) phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3 thu được 36 gam kết tủa. Công thức phân tử của X là
A. C4H6
B. C2H2
C. C4H4
D. C3H4.
Hướng dẫn giải:
Đáp án B
Ta có: nX = 0,15 mol
Gọi công thức của ankin là CnH2n-2 (n ≥ 2)
Ta có: n↓ = nX = 0,15 mol
→M↓=360,15=240→?↓=360,15=240
TH1: Ankin có 1H linh động
Mankin = 14n – 2 = 240 – 108 + 1 = 133
→ không có ankin thỏa mãn
TH2: Ankin có 2H linh động
Mankin = 14n – 2 = 240 – 2.108 + 2 = 26
→ X là C2H2
Câu 6: Cho 0,1 mol hỗn hợp gồm axetilen và ankin X có tỉ lệ mol 1:1 vào dung dịch chứa AgNO3 dư trong NH3 thu được 19,35 gam kết tủa. Công thức của ankin X là
A. CH3−CH2−CH2−C≡CH??3−??2−??2−?≡??
B. CH3−CH2−C≡CH??3−??2−?≡??
C. CH3−C≡C−CH3??3−?≡?−??3
D. CH3−C≡CH??3−?≡??
Hướng dẫn giải:
Đáp án D
nC2H2=nX=0,12=0,05mol??2?2=??=0,12=0,05???
TH1: ankin X không tác dụng với AgNO3/NH3
Kết tủa thu được là Ag2C2
nAg2C2=nC2H2=0,05mol→n↓=0,05.240=12<19,35g???2?2=??2?2=0,05???→?↓=0,05.240=12<19,35? (không thỏa mãn)
TH2: ankin X có tác dụng với AgNO3/NH3
Gọi công thức của ankin là R−C≡CH?−?≡??
→ Kết tủa thu được gồm Ag2C2 (0,05 mol) và R−C≡CH(0,05mol)?−?≡??(0,05???)
Ta có: 0,05.240 + 0,05(R + 132) = 19,35 → R = 15 (-CH3)
Vậy X là CH3−C≡CH??3−?≡??
Câu 7: Hỗn hợp X gồm hidro và một hidrocacbon. Nung nóng 14,56 lít hỗn hợp X (đktc), có Ni xúc tác đến khi phản ứng hoàn toàn thu được hỗn hợp Y có khối lượng 10,8 gam. Biết tỉ khối của Y so với metan là 2,7 và Y có khả năng làm mất màu dung dịch brom. Công thức phân tử của hidrocacbon là
A. C3H6
B. C4H6
C. C3H4
D. C4H8
Hướng dẫn giải:
Đáp án C
nX=0,65mol,¯¯¯¯¯¯MY=43,2??=0,65???,??¯=43,2
Áp dụng định luật bảo toàn khối lượng ta có:
mX=mY=10,8→nX.¯¯¯¯¯¯MX=nY.¯¯¯¯¯¯MY→nY=0,25mol??=??=10,8→??.??¯=??.??¯→??=0,25???
Vì hỗn hợp Y có khả năng làm mất màu dung dịch brom nên hidro phản ứng hết, hidrocacbon còn dư. Như vậy trong hỗn hợp X
nH2=0,65−0,25=0,4mol;nCxHy=0,25mol??2=0,65−0,25=0,4???;?????=0,25???
→ (12x + y).0,25 + 0,4.2 = 10,8 → 12x + y = 40 → x = 3 và y = 4
Vậy hidrocacbon là C3H4
Câu 8: Cho 3,12 gam ankin X phản ứng với 0,1 mol H2 (xúc tác Pd/PbCO3, ), thu được hỗn hợp Y chỉ có hai hiđrocacbon. Công thức phân tử của X là
A. C2H2
B. C5H8
C. C4H6
D. C3H4
Hướng dẫn giải
Đáp án A
Gọi công thức phân tử ankin X: CnH2n−2(n≥2)???2?−2?≥2
CnH2n−2+H2Pb/PbCO3,t0−−−−−−−→CnH2n0,1←0,1(mol)???2?−2+?2→??/????3,?0???2?0,1←0,1(???)
Sau phản ứng thu được 2 hidrocacbon →ankin X dư
→nX>0,1→MX<3,120,1=31,2→→??>0,1→??<3,120,1=31,2→ ankin X là C2H2
Câu 9: Đốt cháy hoàn toàn hỗn hợp X gồm C2H2, C3H4 và C4H4 (số mol mỗi chất bằng nhau) thu được 0,09 mol CO2. Nếu lấy cùng một lượng hỗn hợp X như trên tác dụng với một lượng dư dung dịch AgNO3 trong NH3, thì khối lượng kết tủa thu được lớn hơn 4 gam. Công thức cấu tạo của C3H4 và C4H4 trong X lần lượt là
A. CH≡C−CH3,CH2=CH−C≡CH??≡?−??3,??2=??−?≡??
B. CH≡C−CH3,CH2=C=C=CH2??≡?−??3,??2=?=?=??2
C. CH2=C=CH2,CH2=C=C=CH2??2=?=??2,??2=?=?=??2
D. CH2=C=CH2,CH2=CH−C≡CH??2=?=??2,??2=??−?≡??
Hướng dẫn giải:
Đáp án A
Gọi số mol các chất trong hỗn hợp X đều là x mol
→nCO2=2x+3x+4x=0,09→x=0,01→???2=2?+3?+4?=0,09→?=0,01
C2H2AgNO3/NH3−−−−−−−→Ag2C20,010,01?2?2→????3/??3??2?20,010,01
Khối lượng kết tủa tạo ra do C2H2 phản ứng với AgNO3/NH3 là 2,4 gam suy ra hai chất còn lại khi phản ứng với AgNO3/NH3 cho lượng kết tủa lớn hơn 1,6 gam
CH2=CH−C≡CHAgNO3/NH3−−−−−−−→CH2=CH−C≡CAg0,010,01??2=??−?≡??→????3/??3??2=??−?≡???0,010,01
Khối lượng kết tủa tạo ra do C4H4 phản ứng với AgNO3/NH3 là 1,59 gam
→ C3H4 phải tham gia phản ứng kết tủa
Vậy công thức cấu tạo của C3H4 và C4H4 trong X lần lượt là CH≡C−CH3,CH2=CH−C≡CH??≡?−??3,??2=??−?≡??
Câu 10: Cho 13,8 gam chất hữu cơ X có công thức phân tử C7H8 tác dụng với một lượng dư dung dịch AgNO3 trong NH3, thu được 45,9 gam kết tủa. X có bao nhiêu đồng phân cấu tạo thỏa mãn
A. 5
B. 4
C. 6
D. 2
Hướng dẫn giải:
Đáp án B
Phương trình phản ứng
C7H8+nAgNO3+nNH3→C7H8−nAgn+nNH4NO30,150,15?7?8+?????3+???3→?7?8−????+???4??30,150,15
Ta có: (12.7 + 8-n + 108n).0,15 = 45,9 → n = 2
Mặt khác độ bất bào hòa của C7H8 bằng 2.7−8+22=42.7−8+22=4
→ C7H8 có hai nối ba ở đầu mạch, các đồng phân thỏa mãn là
CH≡C−CH2−CH2−CH2−C≡CH??≡?−??2−??2−??2−?≡??
CH≡C−CH2−CH(CH3)−C≡CH??≡?−??2−??(??3)−?≡??
CH≡C−C(CH3)2−C≡CH??≡?−?(??3)2−?≡??
CH≡C−CH(C2H5)−C≡CH??≡?−??(?2?5)−?≡??
Câu 11: Đốt cháy m gam hidrocacbon A ở thể khí trong điều kiện thường được CO2 và m gam H2O. Đốt cháy hoàn toàn 0,1 mol hidrocacbon B là đồng đẳng kế tiếp của A rồi hấp thụ toàn bộ sản phẩm cháy vào bình nước vôi trong dư thấy khối lượng bình tăng x gam. Giá trị x là
A. 29,2 gam
B. 31 gam
C. 20,8 gam
D. 16,2 gam
Hướng dẫn giải:
Đáp án A
Đặt công thức phân tử của A là CxHy
Phương trình phản ứng:
CxHy+(x+y4)O2t0→xCO2+y2H2Om12x+yy2.m12x+y????+(?+?4)?2→?0???2+?2?2??12?+??2.?12?+?
→y2.m12x+y=m18→xy=23→?2.?12?+?=?18→??=23
Vì hidrocacbon A ở thể khí nên số C không vượt quá 4. Vậy A là C4H6, đồng đẳng kế tiếp của A là C5H8
C5H8+O2,t0−−−→5CO2+4H2O0,10,50,4?5?8→+?2,?05??2+4?2?0,10,50,4
→x=0,5.44+0,4.18=29,2gam→?=0,5.44+0,4.18=29,2???
Câu 12: Cho 2,24 lít (đktc) hỗn hợp X gồm C2H4 và C2H2 lội chậm qua bình đựng dung dịch Br2 dư thấy khối lượng bình tăng thêm 2,7 gam. Thành phần phần trăm thể tích của C2H2 có trong hỗn hợp X là
A. 40%
B. 50%
C. 60%
D. 75%
Hướng dẫn giải
Đáp án B
nX=2,2422,4=0,1mol??=2,2422,4=0,1???
Gọi số mol của C2H4 và C2H2 lần lượt là x và y mol
x + y = 0,1 (1)
C2H4+Br2→C2H4Br2x→xx(mol)C2H2+2Br2→C2H2Br4y→2yy(mol)?2?4+??2→?2?4??2?→??????2?2+2??2→?2?2??4?→2??(???)
Ta có khối lượng bình tăng bằng khối lượng hỗn hợp khí X →28x + 26y = 2,7 (2)
Từ (1) và (2) →x = y = 0,05
Phần trăm thể tích bằng phần trăm số mol khí.
→%VC2H4=0,050,1.100%=50%%VC2H2=100%−50%=50%