NaHCO3 + NaOH → Na2CO3 + H2O | NaHCO3 ra Na2CO3
Sinx.edu.vn xin giới thiệu phương trình NaHCO3 + NaOH → Na2CO3 + H2O là phản trao đổi. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng NaHCO3 + NaOH → Na2CO3 + H2O
1. Phương trình phản ứng NaHCO3 ra Na2CO3
NaHCO3 + NaOH → Na2CO3 + H2O
2. Viết phương trình ion rút gọn NaHCO3 + NaOH
Phương trình ion:
Na+ + HCO3−+ Na+ + OH− → 2Na+ + CO32− + H2O
Phương trình ion thu gọn:
HCO3− + OH− → CO32− + H2O
3. Điều kiện phản ứng NaHCO3 tác dụng với NaOH
Điều kiện phản ứng NaHCO3 tác dụng với NaOH: nhiệt độ thường
4. Cách thực hiện phản ứng NaHCO3 tác dụng với NaOH
Cho NaHCO3 tác dụng với NaOH sau phản ứng thu được muối và nước.
5. Hiện tượng nhận biết phản ứng
Nhỏ BaCl2 vào sản phẩm tạo thành thấy thu được kết tủa.
6. Bản chất của các chất tham gia phản ứng
6.1. Bản chất của NaHCO3 (Natri hidrocacbonat)
NaHCO3 là một muối axit nhưng thể hiện tính axit yếu. NaHCO3 khi tác dụng với NaOH sẽ tạo thành muối trung hoà và nước.
6.2. Bản chất của NaOH (Natri hidroxit)
NaOH là một bazo mạnh phản ứng với axit tạo thành muối và nước.
7. Lý thuyết và phương pháp giải nhiệt phân muối hiđrocacbonat và muối cacbonat
Nhiệt phân muối hiđrocacbonat (HCO3-)
Nhận xét: Tất cả các muối hiđrocacbonat đều kém bền nhiệt và bị phân huỷ khi đun nóng.
Phản ứng:
2M(HCO3)n → M2(CO3)n + nCO2 + nH2O
Ví dụ: 2NaHCO3 → Na2CO3 + CO2 + H2O
Nhiệt phân muối cacbonat (CO32-)
Nhận xét: Các muối cacbonat không tan (trừ muối amoni) đều bị phân huỷ bởi nhiệt.
Phản ứng:
M2(CO3)n → M2On + CO2
VD: CaCO3 → CaO + CO2
Lưu ý:
Các phản ứng nhiệt phân muối cacbonat và hiđrocacbonat đều không thuộc phản ứng oxi hoá - khử.
Phản ứng nhiệt phân muối FeCO3 trong không khí có phản ứng:
FeCO3 → FeO + CO2
4FeO + O2→ 2Fe2O3
8. Muối NaHCO3 có tính chất
8.1. Nhiệt phân tạo thành muối và giải phóng CO2
2NaHCO3 → Na2CO3 +CO2↑ + H2O
8.2. Thủy phân tạo thành môi trường Bazơ yếu
NaHCO3 + H2O → NaOH + H2CO3
8.3. Tác dụng với axit mạnh tạo thành muối và nước
Tác dụng với Axit Sunfuric:
2NaHCO3 + H2SO4 → Na2SO4+ 2H2O + 2CO2
Tác dụng với axit Clohiric:
NaHCO3 + HCl → NaCl + H2O + CO2
8.4. Tác dụng với bazơ tạo thành muối mới và bazơ mới
Tác dụng với Ca(OH)2:
NaHCO3+ Ca(OH)2 → CaCO3 + NaOH + H2O.
Một trường hợp khác có thể tạo thành 2 muối mới với phương trình phản ứng:
2NaHCO3 + Ca(OH)2 → CaCO3 + Na2CO3 + 2H2O.
Tác dụng với NaOH:
NaHCO3 + NaOH → H2O + Na2CO3
9. Ứng dụng NaHCO3
Natri Bicarbonat được biết đến rộng rãi với vai trò là chất phụ gia và có các tác dụng tốt đối với chế biến món ăn, làm bánh, làm mềm thịt... hoặc các tác dụng tẩy rửa tại chỗ. Trong y tế, thuốc đóng vai trò chống toan hóa máu, chống acid dạ dày, kiềm hóa nước tiểu. Việc sử dụng dung dịch bicarbonate để chống toan hóa máu bắt buộc phải được xét nghiệm trước và chỉ định cẩn trọng. Chỉ định trước khi có kết quả xét nghiệm chỉ được cho khi ở trong tình huống đe dọa nghiêm trọng đến tính mạng người bệnh.
10. Tính chất hoá học của NaOH
NaOH là một bazơ mạnh nó sẽ làm quỳ tím chuyển màu xanh, còn dung dịch phenolphtalein thành màu hồng. Một số phản ứng đặc trưng của Natri Hidroxit được liệt kê ngay dưới đây.
Phản ứng với axit tạo thành muối + nước:
NaOHdd + HCldd→ NaCldd + H2O
Phản ứng với oxit axit: SO2, CO2…
2 NaOH + SO2→ Na2SO3 + H2O
NaOH + SO2→ NaHSO3
Phản ứng với axit hữu cơ tạo thành muối và thủy phân este, peptit:
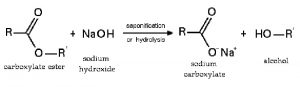
Phản ứng với muối tạo bazo mới + muối mới (điều kiện: sau phản ứng phải tạo thành chất kết tủa hoặc bay hơi):
2 NaOH + CuCl2→ 2NaCl + Cu(OH)2↓
Tác dụng với kim loại lưỡng tính:
2 NaOH + 2Al + 2H2O→ 2NaAlO2 + 3H2↑
2NaOH + Zn → Na2ZnO2 + H2↑
Tác dụng với hợp chất lưỡng tính:
NaOH + Al(OH)3 → NaAl(OH)4
2NaOH + Al2O3 → 2NaAlO2 + H2O
11. Một số bài tập vận dụng liên quan
11.1. Câu hỏi bài tập tự luận
Câu 1. Hoàn thành chuỗi phản ứng hóa học sau:Na → NaOH → Na2CO3 → NaHCO3 → NaOH → NaCl → NaOH → Na → NaH → NaOH → NaCl + NaOCl
Đáp án hướng dẫn giải chi tiết
1) 2Na + 2H2O → 2NaOH + H2
2) 2NaOH + CO2 → Na2CO3 + H2O
3) Na2CO3 + CO2 + H2O → 2NaHCO3
4) 2NaHCO3 + Ca(OH)2 → CaCO3 + 2NaOH + 2H2O
5) NaOH + HCl → NaCl + H2O
6) 2NaCl + 2H2O → 2NaOH + Cl2 + H2
7) 4NaOH → 4Na + O2 + 2H2O
8) 2Na + H2 → 2NaH
9) NaH + H2O → NaOH + H2
10) 2NaOH + Cl2 → NaCl + NaOCl + H2O
Câu 2. Hấp thụ hoàn toàn 0,16 mol CO2 vào 2 lít dung dịch Ca(OH)2 0,05 M thu được kết tủa X và dd Y. Cho biết khổi lượng dd Y tăng hay giảm bao nhiêu so với dd Ca(OH)2 ban đầu?
Đáp án hướng dẫn giải
CO2 + Ca(OH)2 → CaCO3 + H2O
0,1 0,1 0,1
2CO2 + CaCO3 + H2O → Ca(HCO3)2
0,16 – 0,1 → 0,06
=> n↓= 0,04 mol
n↓= 0,04 mol => m ↓ = 4g < 0,16 . 44 = 7,04g
=> mdd tăng = 7,04 – 4 = 3,04g
Câu 3. Hoàn thành chuỗi phản ứng hóa học sau:Na → Na2O → NaOH → Na2CO3 → NaCl → NaOH → NaHCO3
Đáp án hướng dẫn giải
1) 4Na + O2 2Na2O
2) Na2O + H2O → 2NaOH
3) 2NaOH + CO2 → Na2CO3 + H2O
4) Na2CO3 + HCl → NaCl + CO2 + H2O
5) 2NaCl + H2O → 2NaOH + H2 + Cl2
6) NaOH + CO2 → NaHCO3
Câu 4. A là hh khí gồm CO2, SO2 dA/ H2 = 27. Dẫn a mol n hợp khí A qua bình đựng 1 lít dung dịch NaOH 1,5aM. Sau phản ứng cô cạn cẩn thận dung dịch thu được m (g) muối khan. Tìm m theo a?
Đáp án hướng dẫn giải
Gọi CT chung của 2 oxit MO2 → MMO2 = 54 => M = 22 (g)
Phương pháp nối tiếp
MO2 + 2NaOH→ Na2MO3 + H2O
0,75a 1,5a → 0,75a
MO2 + Na2CO3 + H2O → 2NaHCO3
0,25a → 0,25a
Sau phản ứng
=> m = 0,5a . (46 + 22 + 48) + 0,5a . (24 + 22 + 48) = 105a
Câu 5. Hỗn hợp A gồm R2CO3, RHCO3 và MCl (trong đó R là kim loại kiềm). Nung nóng 20,29 g hỗn hợp A, sau phản ứng xảy ra hoàn toàn thấy còn lại 18,74g chất rắn. Cũng đem 20,29g hỗn hợp A tác dụng hết với 500 ml dung dịch HCl 1M thì thoát ra 3,36 lit khí (dktc) và dung dịch B. Cho B tác dụng với dung dịch AgNO3 dư thu được 74,62g kết tủa . Kim loại R là:
Đáp án hướng dẫn giải
Khi nung nóng X chỉ có RHCO3phản ứng
2RHCO3 → R2CO3+ CO2 + H2O
mol x → 0,5x → 0,5x
=> mX - mrắn = mCO2 + mH2O (CO2 và hơi nước thoát đi làm cho khối lượng rắn giảm)
=> 20,29 – 18,74 = 44.0,5x + 18.0,5x => x = 0,05 mol
- Khi X + HCl: nHCl = 0,5.1 = 0,5 mol; nCO2= 3,36 : 22,4 = 0,15 mol
+) RHCO3 + HCl → RCl + CO2 + H2O
Mol 0,05 → 0,05
+) R2CO3 + 2HCl → 2RCl + CO2 + H2O
Mol 0,1 → (0,15 – 0,05)
- Bảo toàn nguyên tố Clo : nCl-(Y) = nHCl+ nMCl
+) Ag+ + Cl- → AgCl (nAgCl = 74,62 : 143,5 = 0,52 mol)
Mol 0,52 → 0,52
=> 0,52 = nHCl+ nRCl => nRCl = 0,52 – 0,5 = 0,02 mol
=> mX = mRHCO3 + mR2CO3 + mRCl
=> 20,29 = 0,05.(R+ 61) + 0,1.(2R + 60) + 0,02.(R + 35,5)
=> R = 39g/mol (Kali)
Câu 6. Cho dung dịch Ba(HCO3)2 lần lượt vào các dung dịch: CaCl2; Ca(NO3)2; NaOH; Na2CO3; KHSO4; Na2SO4; Ca(OH)2; H2SO4; HCl. Số trường hợp có kết tủa
Đáp án hướng dẫn giải
Có 6 trường hợp tạo kết tủa sau đây:
Ba(HCO3)2 + 2NaOH → BaCO3+ Na2CO3 + 2H2O
Ba(HCO3)2 + Na2CO3 → BaCO3 + 2NaHCO3
Ba(HCO3)2 + 2KHSO4 → BaSO4 + K2SO4+ 2CO2 + 2H2O
Ba(HCO3)2 + Na2SO4 → BaSO4+ 2NaHCO3
Ba(HCO3)2 + Ca(OH)2 → BaCO3 + CaCO3 + 2H2O
Ba(HCO3)2 + H2SO4 → BaSO4 + 2CO2 + 2H2O
Câu 7. Nhận biết 4 dung dịch mất nhãn sau: Na2SO4, K2CO3, BaCl2, AgNO3
Đáp án hướng dẫn giải
Trích mẫu thử và đánh dấu thứ tự:
Cho quỳ tím vào các mẫu thử:
Mẫu thử nào làm quỳ tím hóa đỏ → nhận ra dung dịch AgNO3
Mẫu thử nào làm quỳ tím hóa xanh → nhận ra dung dịch K2CO3
Mẫu thử nào không đổi màu → nhận ra các dung dịch Na2SO4, BaCl2
Cho dung dịch BaCl2 vào 2 mẫu thử còn lại:
Mẫu thử nào nếu xuất hiện kết tủa trắng → nhận ra dung dịch Na2SO4
BaCl2+ Na2SO4 → BaSO4↓+ 2NaCl
(trắng)
Nếu không có hiện tượng gì xảy ra → nhận ra dung dịch BaCl2
Câu 8. Nhận biết các khí sau: CO, CO2, SO2, SO3, H2
Đáp án hướng dẫn giải
Dẫn từng khí qua dung dịch BaCl2→ nhận được SO3 tạo kết tủa trắng
Phương trình phản ứng:
SO3 + BaCl2 + H2O → BaSO4↓trắng + 2HCl
Dẫn các khí còn lại qua dung dịch nước brom → nhận biết được SO2 làm mất màu nước brom.
Phương trình phản ứng: SO2 + Br2+ 2H2O → 2HBr + H2SO4
Các khí còn lại dẫn qua dung dịch nước vôi trong → nhận biết được CO2 làm đục nước vôi trong.
Phương trình phản ứng: CO2+ Ca(OH)2 → CaCO3↓ + H2O
Hai khí còn lại đốt trong oxi rồi dẫn sản phẩm qua dung dịch nước vôi trong. Nếu khí làm đục nước vôi trong là CO2 → chất ban đầu là CO, khí không phản ứng là H2O → chất ban đầu là H2.
Phương trình phản ứng: 2CO + O2 → 2CO2
CO2 + Ca(OH)2 → CaCO3↓ + H2O
11.2. Câu hỏi bài tập trắc nghiệm
Câu 1. Hỗn hợp X chứa K2O, NH4Cl, KHCO3 và CaCl2 với số mol các chất bằng nhau. Cho hỗn hợp X vào nước dư và đun nóng. Các chất tan trong dung dịch thu được là:
A. KCl, NaOH, CaCl2.
B. KCl, KOH.
C. KCl, KHCO3, NH4Cl, CaCl2.
D. KCl.
Lời giải:
Đáp án: D
Phản ứng xảy ra khi hỗn hợp tác dụng với nước:
K2O + H2O → 2KOH
Các phản ứng xảy ra tiếp theo:
NH4Cl + KOH → NH3 + H2O + KCl
KHCO3 + KOH → K2CO3 + H2O
K2CO3 + CaCl2 → CaCO3 + KCl
Vậy sau phản ứng dung dịch còn lại KCl
Câu 2. Phát biểu nào sau đây là sai khi nói về 2 muối NaHCO3 và Na2CO3?
A. Cả 2 muối đều dễ bị nhiệt phân.
B. Cả 2 muối đều tác dụng với axit mạnh giải phóng khí CO2.
C. Cả 2 muối đều bị thủy phân tạo mỗi trường kiềm yếu.
D. Cả 2 muối đều có thể tác dụng với dung dịch Ca(OH)2 tạo kết tủa.
Lời giải:
Đáp án: A
Phát biểu nào sai khi nói về 2 muối NaHCO3 và Na2CO3: Cả 2 muối đều dễ bị nhiệt phân.
Câu 3. Cho các dãy chắc hóa chất sau: Na, Na2O, NaCl, NaHCO3, Na2CO3. Số chất có thể tạo ra NaOH trực tiếp từ một phản ứng là:
A. 2
B. 3
C. 4.
D. 5.
Lời giải:
Đáp án: D
Phương trình phản ứng minh họa
Na + H2O → NaOH + H2
Na2O + H2O → 2NaOH
2NaCl + 2H2O → 2NaOH + Cl2 + H2
NaHCO3 → NaOH + CO2
Na2CO3 + Ba(OH)2 → 2NaOH + BaCO3
Câu 4. Khi cho một miếng natri có hình dạng bất kì vào chậu nước có pha thêm vài giọt phenolphtanein. Hiện tượng nào không xảy ra trong thí nghiệm này?
A. Miếng natri trở nên có dạng hình cầu.
B. Dung dịch thu được làm quỳ tím hoá hồng.
C. Trong quá trình phản ứng, miếng natri chạy trên mặt nước.
D. Viên natri bị nóng chảy và nổi trên mặt nước.
Lời giải:
Đáp án: B
Khi cho mẩu natri vào nước , mẩu natri nóng chảy thành giot tròn chuyển động xung quanh bề mạt chất lỏng
Phương trình hóa học:
2Na + 2H2O → 2NaOH + H2
Vì dung dịch thu được sau phản ứng là dung dich bazo → Chuyển mau phenolphtalein thành màu đỏ
Câu 5. Trung hòa 50 gam dung dịch A chứa hỗn hợp HCl và H2SO4 cần vừa đủ 100 ml dung dịch B chứa NaOH 0,4M và Ba(OH)2 0,3M thu được 5,825 gam kết tủa. Nồng độ phần trăm của HCl trong dung dịch A là
A. 7,30%
B. 5,84%
C. 3,65%
D. 5,00%
Lời giải:
Đáp án: C
Gọi số mol HCl và H2SO4 lần lượt là a và b
Phản ứng trung hòa:
H+ + OH- → H2O
Phản ứng tạo kết tủa:
Ba2+ + SO42- → BaSO4
Ta có:
nH+ = nOH- ⇒ x + 2y = 0,2
nBaSO4 = 0,025 mol,
nBa(OH)2 = 0,03 mol
⇒ Ba2+ dư sau phản ứng, SO42- đã kết tủa hết
⇒ y = nBaSO4⇒ x = 0,05 mol
=> mHCl = 0,05.36,5 = 1,825 gam
C%HCl = 1,825501,82550 .100 = 3,56%
Câu 6. Cho 3,9 gam hỗn hợp 2 muối Na2CO3 và K2SO3 tác dụng với 200 ml dung dịch HCl, ta thu được một hỗn hợp khí A có tỉ khối hơi so với metan là 3,583 và dung dịch B. Để trung hòa lượng axit còn dư trong dung dịch B ta phải dùng hết 100 ml dung dịch Ba(OH)2 0,2M. Vậy % Na2CO3 và K2SO3 trong hỗn hợp ban đầu là:
A. 60,5% và 39,5%
B. 64% và 36%
C. 64,6% và 35,4%
D. 25,14% và 74,86%
Lời giải:
Đáp án: B
Phương trình phản ứng minh họa
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
x → x
MgCO3 + 2HCl → MgCl2 + CO2 + H2O
y → y
Số mol CO2 là nCO2= 0,67222,40,67222,4 = 0,03 mol
Gọi x, y lần lượt là số mol CaCO3 và MgCO3 trong hỗn hợp
Theo bài ra ta có hệ phương trình
%mCaCO3 = 0,02.1002,840,02.1002,84 . 100% = 70,42%
%mMgCO3 = 100% - 70,42% = 29,58%
Câu 7. Có 4 chất rắn đựng trong 4 lọ riêng biệt không nhãn: Na2CO3, CaCO3, Na2SO4 và CaSO4.H2O. Chỉ dùng cặp hóa chất nào sau đây có thể nhận được cả 4 chất trên?
A. H2O và Na2CO3.
B. H2O và HCl.
C. H2SO4 và BaCl2.
D. H2O và KCl.
Lời giải:
Đáp án: A
Hòa tan vào nước ta chia làm 2 nhóm. Sau đó dùng HCl để nhận biết chất phản ứng với HCl tạo khí là muối CO32-
Nhóm 1: Na2SO4 và Na2CO3
Nhóm 2: CaCO3 và CaSO4.H2O
Phương trình hóa học:
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Câu 8. Cho các dung dịch đựng trong các lọ mất nhãn sau: NaCl, Na2CO3, Na2SO3, Na2S, HCl. Chỉ dùng một chất nào sau đây có thể nhận biết được cả 5 chất trên?
A. Quì tím
B. H2SO4
C. Pb(NO3)2
D. BaCl2
Lời giải:
Đáp án: A
Thí nghiệm trên từng lượng nhỏ hóa chất.
Cho quỳ tím vào từng dung dịch. HCl làm quì tím hóa đỏ, Na2CO3 làm quì tím hóa xanh.
Cho HCl vào 3 mẫu thử còn lai. Lọ có khí thoát ra có mùi trứng thối là N2S, lọ có khí mùi sốc là Na2SO3, lọ còn lại không hiện tượng là NaCl.
Phương trình hóa học
2HCl + Na2S → 2NaCl + H2S
2HCl + Na2SO3 → 2NaCl + SO2 + H2O.
Câu 9. Kim loại kiềm có mạng tinh thể lập phương tâm khối,mật độ electron tự do thấp,điện tích ion nhỏ nên liên kết kim loại kém bền vững.Điều đó giúp giải thích tính chất nào sau này của kim loại kiềm?
A. Nhiệt độ nóng chảy thấp.
B. Mềm.
C. Nhiệt độ nóng chảy thấp và mềm
D. Khối lượng riêng nhỏ.
Lời giải:
Đáp án: C
Kim loại kiềm có khối lượng riêng nhỏ do nguyên tử của các kim loại kiềm có bán kính lớn và có cấu tạo mạng tinh thể kém đặc khít.
Kim loại kiềm có nhiệt độ nóng chảy thấp do lực liên kết kim loại trong mạng tinh thể kim loại kiềm kém.
Kim loại kiềm có năng lượng ion hóa I1I1 thấp là do
Nguyên tử của kim loại kiềm có 1 electron hóa trị ở lớp ngoài cùng.
Bán kính nguyên tử lớn, diện tích hạt nhân nhỏ so với các nguyên tố khác trong cùng chu kì.
Câu 10. Chọn phát biểu đúng:
A. Dung dịch Na2CO3 có tính kiềm mạnh.
B. Dung dịch Na2CO3 có môi trường trung tính có Na2CO3 là muối trung hòa.
C. Dung dịch chứa Na2CO3 có môi trường axit do Na2CO3 là muối của axit yếu.
D. Na2CO3 dễ bị phân hủy khi đung nóng.
Lời giải:
Đáp án: A
Phát biểu đúng: Dung dịch Na2CO3 có tính kiềm mạnh.