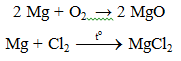Mg + HCl → MgCl2 + H2 | Mg ra MgCl2
Sinx.edu.vn xin giới thiệu phương trình Mg + HCl → MgCl2 + H2 là phản ứng thế. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng Mg + HCl → MgCl2 + H2↑
1. Phương trình phản ứng giữa Mg và HCl
Mg + 2HCl → MgCl2 + H2↑
2. Điều kiện phản ứng
Nhiệt độ thường
3. Hiện tượng phản ứng xảy ra
Sinh ra khí hidro
4. Bản chất của các chất tham gia phản ứng
4.1. Bản chất của Mg (Magie)
Mg là chất khử mạnh tác dụng được với các axit.
4.2. Bản chất của HCl (Axit clohidric)
HCl tác dụng với kim loại đứng trước H trong dãy hoạt động hóa học ( trừ Pb) tạo thành muối và khí hidro.
5. Tính chất hoá học của Mg
Magie là chất khử mạnh:
Mg → Mg2+ + 2e
5.1. Tác dụng với phi kim
Lưu ý: Do Mg có ái lực lớn với oxi: 2Mg + CO2 → MgO. Vì vậy không dùng tuyết cacbonic để dập tắt đám cháy Mg.
5.2. Tác dụng với axit
- Với dung dịch HCl và H2SO4 loãng:
Mg + H2SO4 → MgSO4 + H2
- Với dung dịch HNO3:
4Mg + 10 HNO3 → 4 Mg(NO3)2 + NH4NO3 + 3 H2O
5.3. Tác dụng với nước
Ở nhiệt độ thường, Mg hầu như không tác dụng với nước. Mg phản ứng chậm với nước nóng (do tạo thành hidroxit khó tan).
Mg + 2H2O → Mg(OH)2 + H2
5.4. Điều chế Mg
Trong công nghiệp, Mg được điều chế bằng cách điện phân nóng chảy MgCl2.
MgCl2 ⟶ Mg + Cl2
6. Tính chất hóa học của HCl
Dung dịch axit HCl có đầy đủ tính chất hoá học của một axit mạnh.
6.1. Tác dụng chất chỉ thị
Dung dịch HCl làm quì tím hoá đỏ (nhận biết axit)
HCl → H+ + Cl-
6.2. Tác dụng với kim loại
Tác dụng với KL (đứng trước H trong dãy Bêkêtôp) tạo muối (với hóa trị thấp của kim loại) và giải phóng khí hidrô (thể hiện tính oxi hóa)
Fe + 2HCl 
2Al + 6HCl 
Cu + HCl → không có phản ứng
6.3. Tác dụng với oxit bazo và bazo
Sản phẩm tạo muối và nước
NaOH + HCl → NaCl + H2 O
CuO + 2HCl 
Fe2 O3 + 6HCl
6.4. Tác dụng với muối (theo điều kiện phản ứng trao đổi)
CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
AgNO3 + HCl → AgCl↓ + HNO3
(dùng để nhận biết gốc clorua )
Ngoài tính chất đặc trưng là axit , dung dịch axit HCl đặc còn thể hiện vai trò chất khử khi tác dụng chất oxi hoá mạnh như KMnO4, MnO2, K2 Cr2O7, MnO2, KClO3 ……
4HCl + MnO2 
K2 Cr2 O7 + 14HCl → 3Cl2 + 2KCl + 2CrCl3 + 7H2 O
Hỗn hợp 3 thể tích HCl và 1 thể tích HNO3 đặc được gọi là hỗn hợp nước cường toan ( cường thuỷ) có khả năng hoà tan được Au ( vàng)
3HCl + HNO3 → 2Cl + NOCl + 2H2O
NOCl → NO + Cl
Au + 3Cl → AuCl3
7. Bài tập vận dụng liên quan
Câu 1. Magie tác dụng với axit clohiđric: Mg + 2HCl → MgCl2 + H2↑. Nếu có 12g Mg tham gia phản ứng. Thể tích khí hiđro thu được ở đktc là
A. 22,4 (lít)
B. 11,2 (lít)
C. 22,4 (lít)
D. 11,2 (lít)
Lời giải:
Đáp án: D
Câu 2. Phản ứng nào dưới đây không phải là phản ứng thế?
A. CuO + H2 → Cu + H2O
B. Mg + 2HCl → MgCl2 + H2
C. Ca(OH)2 + CO2 → CaCO3 + H2O
D. Zn + CuSO4 → ZnSO4 + Cu
Lời giải:
Đáp án: C
Câu 3. Kim loại tác dụng với dung dịch HCl và tác dụng với khí Cl2 đều thu được cùng một muối là
A. Fe
B. Zn
C. Cu
D. Ag
Lời giải:
Đáp án: B
Câu 4. Dãy gồm các chất đều tác dụng được với dung dịch HCl loãng là
A. KNO3, CaCO3, Fe(OH)3
B. NaHCO3, AgNO3, CuO
C. FeS, BaSO4, KOH
D. AgNO3, (NH4)2CO3, CuS
Lời giải:
Đáp án: B
Câu 5. Phản ứng trong đó HCl thể hiện tính khử là
A. HCl + NaOH → NaCl + H2O
B. 2HCl + Mg → MgCl2 + H2
C. MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
D. CaCO3 + 2HCl → CaCl2 + CO2 + H2O\
Lời giải:
Đáp án: C
Câu 6. Phát iểu nào sau đây sai?
A. NaCl được dung làm muối ăn và bảo quản thực phẩm.
B. HCl là chất khí không màu, mùi xốc, ít tan trong nước.
C. Axit clohidric vừa có tính oxi hóa, vừa có tính khử.
D. Nhỏ dung dịch AgNO3 vào dung dịch HCl, có kết tủa trắng.
Lời giải:
Đáp án: B
Câu 7. Trong phản ứng: 4HCl + MnO2 → Cl2 + MnCl2 + 2H2O. Vai trò của HCl là
A. chất oxi hóa .
B. vừa là môi trường vừa là chất khử.
C. chất khử.
D. môi trường.
Lời giải:
Đáp án: B
Câu 8. Phản ứng trong đó HCl thể hiện tính khử là
A. HCl + NaOH → NaCl + H2O
B. 2HCl + Mg → MgCl2 + H2
C. MnO2+ 4HCl → MnCl2 + Cl2 + 2H2O
D. CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Lời giải:
Đáp án: C
Câu 9. Cho các phản ứng sau:
(a) 4HCl + MnO2→ MnCl2 + Cl2 + 2H2O.
(b) 2HCl + Fe → FeCl2 + H2.
(c) 14HCl + K2Cr2O7 → 2KCl + 2CrCl3 + 3Cl2 + 7H2O.
(d) 6HCl + 2Al → 2AlCl3 + 3H2.
Số phản ứng trong đó HCl thể hiện tính oxi hóa là
A. 1
B. 2
C. 3
D. 4
Lời giải:
Đáp án: B