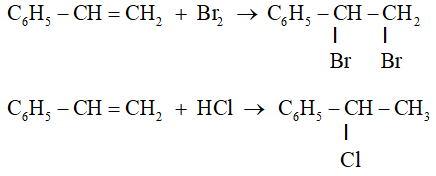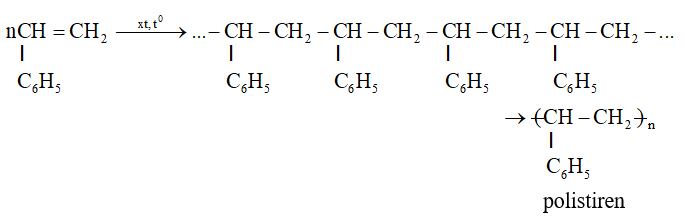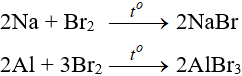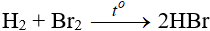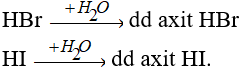C6H5-CH=CH2 + HBr → C6H5-CH2-CH2-Br | C6H5-CH=CH2 ra C6H5-CH2-CH2-Br
Sinx.edu.vn xin giới thiệu phương trình C6H5-CH=CH2 + HBr → C6H5-CH2-CH2-Br là phản ứng cộng. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng C6H5-CH=CH2 + HBr → C6H5-CH2-CH2-Br
1. Phương trình phản ứng C6H5-CH=CH2 + HBr
C6H5-CH=CH2 + HBr → C6H5-CH2-CH2-Br
2. Điều kiện phản ứng xảy ra giữa Stiren và HBr
Nhiệt độ thường
3. Bản chất của C6H5-CH=CH2 (Stiren) trong phản ứng
Stiren thuộc dạng vinylbenzen nên có thể tham gia phản ứng cộng với Br2, H2, HBr, HI, ... vào liên kết đôi.
4. Tính chất hóa học của Stiren
4.1. Phản ứng cộng
Halogen (Cl2, Br2), hiđro halogenua (HCl, HBr) cộng vào nhóm vinyl ở stiren tương tự cộng vào anken.
4.2. Phản ứng trùng hợp và đồng trùng hợp
4.3. Phản ứng oxi hóa
Giống như etilen, stiren làm mất màu dung dịch KMnO4 và bị oxi hóa ở nhóm vinyl, còn vòng benzen vẫn giữ nguyên.
5. Tính chất vật lí và nhận biết stiren
- Stiren là một chất lỏng không màu, nhẹ hơn nước và không tan trong nước.
- Nhận biết: Stiren làm mất màu nước brom và tạo thành hợp chất có công thức C8H8Br2. Ta có thể sử dụng tính chất này để nhận biết stiren.
6. Tính chất hóa học của Br2
6.1. Tác dụng với kim loại
Sản phẩm tạo muối tương ứng
6.2. Tác dụng với hidro
Độ hoạt động giảm dần từ Cl → Br → I
Các khí HBr, HI tan vào nước tạo dung dịch axit.
Về độ mạnh axit thì lại tăng dần từ HCl < HBr < HI.
6.3. Tính khử của Br2, HBr
- Brom thể hiện tính khử khi gặp chất oxi hóa mạnh (như nước clo, …)
Br2 + 5Cl2 + 6H2O → 2HBrO3 (Axit bromic) + 10HCl
- Tính khử của HBr (ở trạng thái khí cũng như trong dd) mạnh hơn HCl. HBr khử được H2SO4 đặc thành SO2.
2HBr + H2SO4đ → Br2 + SO2 + 2H2O
- Dd HBr không màu, để lâu trong không khí trở nên có màu vàng nâu vì bị oxi hóa (dd HF và HCl không có phản ứng này):
4HBr + O2 → 2H2O + 2Br2
7. Câu hỏi vận dụng
Câu 1. Hiđrocacbon nào dưới đây không làm mất màu nước brom?
A. Stiren.
B. Toluen.
C. Axetilen.
D. Etilen.
Lời giải:Đáp án: BGiải thích:
Benzen và các ankyl benzen không làm mất màu dung dịch nước brom=> toluen không làm mất màu dung dịch nước brom
Câu 2. Nhận định nào sau đây sai?
A. Stiren làm mất màu dung dịch brom ở điều kiện thường.
B. Benzen làm mất màu dung dịch brom khi có xúc tác bột sắt.
C. Cumen làm mất màu dung dịch thuốc tím khi đun nóng.
D. Toluen làm mất màu dung dịch thuốc tím khi đun nóng.
Lời giải:Đáp án: B
Câu 3. Stiren không phản ứng được với những chất nào sau đây?
A. dung dịch KMnO4
B. khí H2, Ni, to
C. dung dịch NaOH
D. dung dịch Br2
Lời giải:
Đáp án: C
Giải thích:
C6H5-CH=CH2+ Br2 → C6H5-CHBr-CH2Br
C6H5-CH=CH2 + H2→ C6H5-CH2-CH3.
C6H5-CH=CH2 + 2KMnO4 → C6H5COOK + KOH + MnO2 + H2O + CO2
Câu 4. Ở nhiệt độ thường, chất nào sau đây làm mất màu dung dịch nước Br2?
A. Etilen.
B. Metan.
C. Butan.
D. Benzen
Lời giải:
Đáp án: A
Giải thích:
Eilen làm mất màu dd nước Br2 ở nhiệt độ thường
CH2=CH2 + Br2 → CH2Br-CH2Br