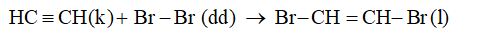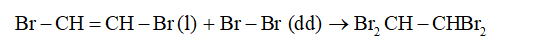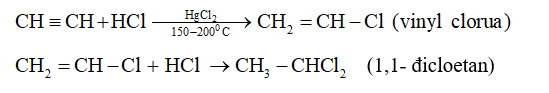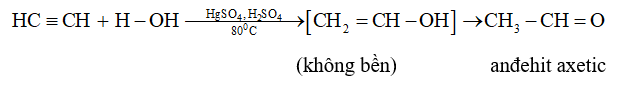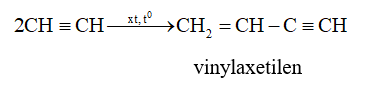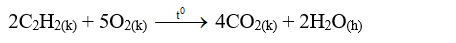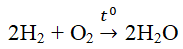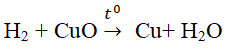C2H2 ra C2H4 l C2H2 + H2 → C2H4 l Axetilen ra Etilen
Sinx.edu.vn xin giới thiệu phương trình C2H2 + H2 → C2H4 là phản ứng cộng. Bài viết này cung cấp đầy đủ thông tin về phương trình hóa học đã được cân bằng, điều kiện các chất tham gia phản ứng, hiện tượng (nếu có), ... Mời các bạn đón xem:
Phản ứng C2H2 + H2 → C2H4
1. Phương trình phản ứng từ C2H2 ra C2H4
C2H2 + H2 C2H4
2. Điều kiện phương trình phản ứng giữa C2H2 + H2
Nhiệt độ: Nhiệt độ
Xúc tác: Palladium (Pd).
3. Hiện tượng nhận biết phản ứng.
Dưới tác dụng của nhiệt và chất xúc tác palladium các ankin có phân tử khối nhỏ bị đề hiđro tạo anken tương ứng (với các anken có phân tử khối nhỏ ở thể khí).
4. Bản chất của C2H2 (Axetilen) trong phản ứng
Do có một liên kết ba giữa hai nguyên tử cacbon trong một phân tử axetilen nên trong những điều kiện thích hợp, axetilen có phản ứng cộng với hidro cùng một số chất khác như HCl,...
5. Điều chế C2H4 trong phòng thí nghiệm
5.1. Hóa chất và dụng cụ
H2SO4 đặc, rượu etylic (C2H5OH), Canxi cacbua (CaC2), Pd, đá bọt ….
Đèn cồn, ống nghiệm, giá đỡ, kẹp, chậu thủy tinh, ống dẫn khí,…
5.2. Phương pháp thu khí etilen
Cách 1: Sử dụng phương pháp đẩy nước, do khí etilen là chất khí ít tan trong nước.
Cách 2: Điều chế khí axetilen từ canxi cacbua, sau đó cho tác dụng với khí Hidro có xúc tác Pd hoặc Pb.
5.3. Điều kiện phản ứng
Nhiệt độ: 170o C; xúc tác: H2SO4 đặc, Pb, Pd
5.4. Cách thực hiện thí nghiệm
Đun nóng hỗn hợp (H2SO4 đặc, rượu etylic (C2H5OH)) đến 170 độ C thì thấy có khí etilen thoát ra có hiện tượng etilen đẩy nước trong ống nghiệm dùng để thu khí etilen. Chờ đến khi lượng etilen đẩy hết lượng nước ra ống nghiệm thì nhanh chóng lấy nút cao su đậy miệng ống nghiệm lại, chú ý là phải đậy miệng ống nghiệm lại mới được lật ống nghiệm lên.
5.5. Phương trình hóa học
Từ phần phương pháp thu khí trên ta có phương trình hóa học xảy ra theo các cách:
Cách 1: Sử dụng phương pháp đẩy nước, do khí etilen là chất khí ít tan trong nước.
C2H5OH → C2H4 + H2O (Xúc tác của H2SO4đặc, nhiệt độ 170o C)
Cách 2: Điều chế khí axetilen từ canxi cacbua, sau đó cho tác dụng với khí Hidro có xúc tác Pd hoặc Pb.
CaC2 + 2H2O → C2H2 + Ca(OH)2
C2H2 + H2 → C2H4 (Xúc tác Pd hoặc Pb)
6. Tính chất của C2H2
6.1 Tính chất hóa học của C2H2
a. Phản ứng cộng
- Cộng brom
Trong liên kết ba của phân tử axetilen có hai liên kém bền. Vì vậy, ta axetilen sẽ làm mất màu dung dịch brom tương tự etilen.
- Dẫn axetilen qua dung dịch brom màu da cam.
+ Hiện tượng: Dung dịch brom bị mất màu.
Axetilen có phản ứng cộng với brom trong dung dịch.
+ Sản phẩm mới sinh ra có liên kết đôi trong phân tử nên có thể cộng tiếp với một phân tử brom nữa:
+ Trong điều kiện thích hợp, axetilen cũng có phản ứng cộng với hiđro và một số chất khác.
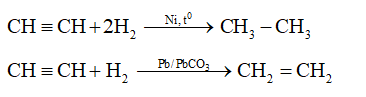
- Cộng hiđro
- Cộng hiđro clorua
- Cộng nước (hiđrat hóa)
b. Phản ứng đime hóa và trime hóa
- Hai phân tử axetilen có thể cộng hợp với nhau tạo thành vinylaxetilen
c. Phản ứng thế bằng ion kim loại
d. Phản ứng oxi hóa
- Axetilen là hiđrocacbon, vì vậy khi đốt, axetilen sẽ cháy tạo ra cacbon Đioxit và nước, tương tự metan và etilen.
- Axetilen cháy trong không khí với ngọn lửa sáng, tỏa nhiều nhiệt.
6.2. Tính chất vật lí của C2H2
Axetilen (C2H2) được biết đến là chất khí hoàn toàn không màu, không mùi, ít tan trong nước và nhẹ hơn không khí. Axetilen trong thực tế môi trường hiện nay sẽ có nhiều mùi khác nhau, nguyên nhân là do các tạp chất gây nên.
7. Tính chất hóa học của H2
Hiđro là phi kim có tính khử. Ở những nhiệt độ thích hợp, hiđro không những kết hợp được với đơn chất oxi mà còn kết hợp được với nguyên tố oxi trong một số oxit kim loại. Các phản ứng này đều tỏa nhiều nhiệt. Cụ thể:
- Hiđro tác dụng với oxi
Hiđro cháy trong oxi theo phương trình hóa học:
Hỗn hợp H2 và O2 là hổn hợp nổ. Hỗn hợp nổ mạnh nhất khi tỉ lệ H2 : O2 là 2:1 về thể tích.
- Hiđro tác dụng với một số oxit kim loại như FeO, CuO, Fe2O3, …
Ví dụ:
Hiđro phản ứng với đồng oxit ở nhiệt độ khoảng 400°C theo phương trình hóa học:
8. Bạn có biết
- Phản ứng trên là phản ứng cộng hợp hidro của ankin.
- Tùy thuộc vào xúc tác sử dụng mà phản ứng cộng H2 vào axetilen xảy ra theo các hướng khác nhau.
- Thường thì phản ứng cộng H2 thường tạo ra hỗn hợp nhiều sản phẩm
- Số mol khí giảm bằng số mol H2 tham gia phản ứng.
9. Bài tập vận dụng
Câu 1: Khi đốt cháy khí etilen thì số mol CO2 và H2O được tạo thành theo tỉ lệ
A. 2 : 1.
B. 1 : 2.
C. 1 : 3.
D. 1 : 1.
Lời giải:
Đáp án: D
Câu 2: Etilen có tính chất vật lý nào sau đây?
A. là chất khí không màu, không mùi, tan nhiều trong nước, nhẹ hơn không khí.
B. là chất khí, không màu, không mùi, ít tan trong nước, nhẹ hơn không khí.
C. là chất khí màu vàng lục, mùi xốc, ít tan trong nước, nặng hơn không khí.
D. là chất khí không màu, mùi hắc, tan trong nước, nặng hơn không khí.
Lời giải:
Đáp án: B
Giải thích:
Etilen là chất khí, không màu, không mùi, ít tan trong nước, nhẹ hơn không khí.
Câu 3: Trong phân tử etilen giữa hai nguyên tử cacbon có
A. hai liên kết đôi.
B. một liên kết đôi.
C. một liên kết đơn.
D. một liên kết ba.
Lời giải:
Đáp án: B
Giải thích:
Trong phân tử etilen giữa hai nguyên tử cacbon có một liên kết đôi.
Câu 4: Trong quá trình chín trái cây đã thoát ra một lượng nhỏ khí nào sau đây?
A. metan.
B. etan.
C. etilen.
D. axetilen.
Lời giải:
Đáp án: C
Giải thích:
Trong quá trình chín trái cây đã thoát ra một lượng nhỏ khí etilen.
Câu 5: Khi sục dòng khí axetilen vào cốc đựng dung dịch brom thì thấy:
A. Màu của dung dịch nhạt dần, có chất lỏng không màu lắng xuống đáy cốc.
B. Màu của dung dịch nhạt dần, có chất rắn không màu kết tủa
C. màu của dung dịch nhạt dần và có khí hidro bromua bay lên
D. màu của dung dịch đậm dần, có chất lỏng không màu lắng xuống đáy cốc
Lời giải:
Đáp án: B
Câu 6. Một trong những ứng dụng của axetilen là làm nhiên liệu trong đèn xì để hàn, cắt kim loại. Khi đốt cháy axetilen từ đèn xì (sinh ra nhờ phản ứng của đất đèn với nước) thấy có mùi rất khó chịu. Đó là do
A. Axetilen cháy sinh ra
B. một số tạp chất chứa photpho, lưu huỳnh có trong đất đèn sinh ra.
C. phản ứng của axetilen với kim loại hàn.
D. phản ứng của kim loại được hàn với các thành phần của không khí.
Lời giải:
Đáp án: A
Giải thích:
Một trong những ứng dụng của axetilen là làm nhiên liệu trong đèn xì để hàn, cắt kim loại. Khi đốt cháy axetilen từ đèn xì (sinh ra nhờ phản ứng của đất đèn với nước) thấy có mùi rất khó chịu. Đó là do Axetilen cháy sinh ra
Phương trình phản ứng hóa học
C2H2 + 52O2→ 2CO2 + H2O
C2H6+ 72O2 → 2CO2 + 3H2O
Ta thấy khi đốt axetilen, lượng nước giải phóng ra ít hơn so với đốt etan. Vì vậy lượng nước thoát ra làm nguội cũng ít hơn. Do đó đốt axetilen nhiệt độ cao hơn
Câu 7. CH4 và C2H4có tính chất hóa học giống nhau là
A. tham gia phản ứng cộng với khí hiđro.
B. tham gia phản ứng cháy với khí oxi sinh ra khí cacbonic và nước.
C. tham gia phản ứng trùng hợp.
D. tham gia phản ứng cộng với dung dịch brom.
Lời giải:
Đáp án: B
Giải thích:
Loại A vì chỉ C2H4 tham gia phản ứng cộng Hidro
C2H4+ H2 ⟶ C2H6
Loại C vì có C2H4 phản ứng
nCH2= CH2 ⟶ (−CH2−CH2−)n (nhiệt độ, xúc tác)
Loại D vì chỉ có C2H4 phản ứng
C2H4 + Br2 → C2H4Br2
Khí CH4 và C2H4 có tính chất hóa học giống nhau là tham gia phản ứng cháy với khí oxi sinh ra khí cacbonic và nước.
Câu 8. Cho H2 và 1 anken có thể tích bằng nhau qua Niken nung nóng ta thu được hỗn hợp A . Biết tỉ khối hơi của A với H2 là 23,2. Hiệu suất phản ứng hidro hóa là 75%. Công thức phân tử của aken là
A. C2H4
B. C3H6
C. C4H8
D. C5H10
Lời giải:
Đáp án: C
Giải thích:
Công thức tổng quát của anken là CnH2n ta có
Theo giả thiết ta chọn: nH2= nCnH2n = 1
Phương trình tổng quát
CnH2n + H2 → CnH2n+2
Theo phương trình, số mol khí giảm chính là số mol của H2
H% = 75%
ngiảm = nH2 phản ứng = 1.0,75 = 0,75 mol
nA = nhỗn hợp ban đầu – ngiảm = 2 – 0,75 = 1,25 mol
Áp dụng định luật bảo toàn khối lượng ta có: mH2 + mCnH2n = mA
=> MA = mA: nA => n= 4=> Olefin là C4H8
Câu 9. Để khử hoàn toàn 100 ml dung dịch KMnO4 0,2M tạo thành chất rắn màu nâu đen cần V lít khí C2H4 (ở đktc). Giá trị tối thiểu của V là:
A. 2,240.
B. 2,688.
C. 0,672.
D. 1,344.
Lời giải:
Đáp án: C
Giải thích:
Phương trình phản ứng
3CH2=CH2 + 2KMnO4 + 4H2O → 3C2H4(OH)2 + 2KOH + 2MnO2
0,03 ← 0,02
→ VC2H4 = 0,03.22,4 = 0,672 (l)
Câu 10. Cho 0,56 lít (đktc) hỗn hợp khí metan và axetilen tác dụng với dung dịch brom dư, lượng brom đã tham gia phản ứng là 5,6 gam. Thành phần phần trăm về thể tích của axetilen trong hỗn hợp ban đầu lần lượt là
A. 20%.
B. 70%.
C. 40%.
D. 60%.
Lời giải:
Đáp án: B
Giải thích:
Số mol của brom là:
nBr2 =5,6/160 = 0,035 (mol)
Phương trình phản ứng hóa học
C2H2 + 2Br2 → C2H2Br4
Theo PT trên, nC2H2 = 1/2.nBr2 = 0,035/2 = 0,0175 (mol)
⇒ VC2H2 = 0,0175.22,4 = 0,392 (lít)
⇒% VC2H2 = 0,392/0,56.100% = 70%